
2020年人教版化学选修四化学反应原理 暑假测试卷含答案
14页1、绝密启用前2020年人教版化学选修四化学反应原理 暑假测试卷本试卷分第卷和第卷两部分,共100分,考试时间150分钟。 分卷I一、单选题(共15小题,每小题4.0分,共60分) 1.我国第五套人民币中的一元硬币材料为钢芯镀镍,依据电镀原理,钢芯镀镍时,钢芯应该做()A 正极B 负极C 阳极D 阴极2.实验室中,要使AlCl3溶液中的Al3全部沉淀出来,最适宜选用的试剂是()A NaOH溶液B Ba(OH)2溶液C 盐酸D 氨水3.下列说法正确的是()A 活化分子一定能发生有效碰撞B 增大反应物浓度,可以提高活化分子百分数C 升高温度,可以降低活化能,加快反应速率D 活化能越小,一般分子就越容易成为活化分子4.如下对“难溶”的理解正确的是()A 在水中难溶的物质,在其他溶剂中也是难溶的B 难溶就是绝对不溶C 难溶就是溶解度相对较小,没有绝对不溶于水的电解质D 如果向某溶液中加入另一种试剂时,生成了难溶性的电解质,则说明原溶液中的相应离子已沉淀完全5.一密闭烧瓶中装有NO2气体,在一定条件下达到化学平衡,现将该烧瓶放在热水中()A 颜色不变B 颜色变浅C 颜色变深D 无法判断6.向一体积不
2、变的密闭容器中充入H2和I2,发生反应H2(g)I2(g)2HI(g)H0C H0D 无法判断12.如图所示的装置中,金属活动性顺序 M位于氢之前,而N位于氢之后。下列叙述中不正确的是( )A N上有气体放出B M为负极,N为正极C 是化学能转变为电能的装置D 导线中有电流通过,电流方向是由M到N13.一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是()A CO2(g)2NH3(g)CO(NH2)2(s)H2O(g)H0C CH3CH2OH(g)CH2CH2(g)H2O(g)H0D 2C6H5CH2CH3(g)O2(g)2C6H5CHCH2(g)2H2O(g)H014.液氨与水的电离相似,存在着微弱的电离:2NH3NH4+NH2-。对该体系的说法中错误的是()A 液氨中含有NH3、NH4+和NH2-等微粒NH4+B 一定温度下,液氨中c(NH4+)与c(NH2-)的乘积为一常数C 液氨的电离达到平衡时,c(NH3)c(NH2-)c(NH4+)D 只要不加入其他物质,液氨中c(NH4+)总是与c(NH2-)相等15.等体积、等物质的量浓度的Na2SO4和Na2CO3溶液中
3、,阴阳离子总数相比()A 前者多B 后者多C 一样多D 无法判断分卷II二、非选择题(共4小题,每小题10.0分,共40分) 16.从NO3-、SO42-、H、Cu2、Ba2、Ag、Cl等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。(1)两极分别放出H2和O2时,电解质的化学式可能是_(至少答一种,下同);(2)若阴极析出金属,阳极放出O2,电解质的化学式可能是_;(3)两极分别放出气体,且体积比为11,电解质的化学式可能是_。17.某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:(1)酸浸后加入H2O2的目的是_,调pH的最适宜范围为_。(2)调pH过程中加入的试剂最好是_。ANaOH BCuO CNH3H2O DCu2(OH)2CO3(3)煮沸CuSO4溶液的原因是_。向CuSO4溶液中加入一定量的NaCl、Na2SO3,可以生成白色的CuCl沉淀,写出该反应的化学方程式_。(4)过滤后的沉淀表面通常附着有一些杂质离子,为得到纯净产物,需要进行洗涤,确定沉淀洗涤干净的操作及现象是_。(5)称取所制备的CuCl样品
《2020年人教版化学选修四化学反应原理 暑假测试卷含答案》由会员jinz****ang分享,可在线阅读,更多相关《2020年人教版化学选修四化学反应原理 暑假测试卷含答案》请在金锄头文库上搜索。

鲁教版(五四制)七年级上册 1.2 图形的全等 学案(无答案)

鲁教版(五四制)七年级上册 1.3 探索三角形全等的条件(第三课时)学案(无答案)
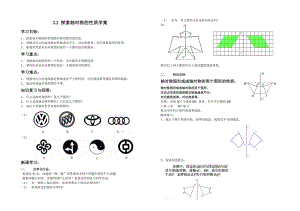
鲁教版(五四制)七年级上册2.2探索轴对称的性质学案(无答案)

鲁教版(五四制)七年级上册第一章 三角形章末复习学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第一课时)学案 (无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第四课时)学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第三课时)学案(无答案)

鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第二课时)学案(无答案)

鲁教版(五四制)七年级上册1.1认识三角形(第二课时)学案

鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第一课时)学案(无答案)

鲁教版(五四制)七年级上册 1.1 认识三角形(第五课时)学案(无答案)

鲁教版(五四制)七年级上册1.4三角形的尺规作图学案(无答案)

鲁教版(五四制)七年级上册1.5利用三角形全等测距离学案(无答案)

鲁教版(五四制)七年级上册2.1轴对称现象学案(无答案)
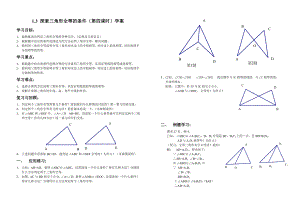
鲁教版(五四制)七年级上册1.3探索三角形全等的条件(第四课时)学案(无答案)

教师版-江苏省盱眙县实验中学苏科版九年级数学上册导学案(训练案)2.2-1圆的对称性

人教版初中化学讲义——16 第六单元 一氧化碳、二氧化碳、制取二氧化碳

教师版-江苏省盱眙县实验中学苏科版九年级数学上册导学案(训练案)2.7弧长及扇形的面积

人教版初中化学讲义——11化合价规律、相对分子质量、质量分数计算

高考 保分班话术
 牛津高一英语(上)单词练习
牛津高一英语(上)单词练习
2023-02-19 8页
 高中生必备的项作技文巧
高中生必备的项作技文巧
2023-11-22 17页
 高中数学《曲线与方程》说课稿新人教A版选修
高中数学《曲线与方程》说课稿新人教A版选修
2024-01-30 8页
 高考复习:满分生传授数学学习秘籍
高考复习:满分生传授数学学习秘籍
2023-12-19 4页
 2022年中考试英语试题(B)缺答案
2022年中考试英语试题(B)缺答案
2023-11-16 10页
 合同书样本北京市经济适用住房买卖合同(99)
合同书样本北京市经济适用住房买卖合同(99)
2023-04-21 5页
 一年级上册拼音1-13课练习题(41)
一年级上册拼音1-13课练习题(41)
2022-11-09 16页
 (5月黄金档)2013高考生物 冲刺秘籍 第五练 遗传、变异和生物的进化练习题
(5月黄金档)2013高考生物 冲刺秘籍 第五练 遗传、变异和生物的进化练习题
2023-07-14 12页
 2022年高中物理 第二章2.1 《光电效应》教案 粤教版选修3-5
2022年高中物理 第二章2.1 《光电效应》教案 粤教版选修3-5
2023-04-07 3页
 数列知识点总结及题型归纳总结
数列知识点总结及题型归纳总结
2023-10-27 25页

