
药品生产过程与GMP管理
61页1、药品生产过程与GMP管理 药品是特殊商品 具有特殊性 既要安全又要有效如何实现安全有效 实行GMP管理 药品生产质量管理规范2010版 药品生产质量管理规范 2010年修订 已于2010年10月19日经卫生部部务会议审议通过 现予以发布 自2011年3月1日起施行 新版GMP正文十三章 附录一章 共十四章节 三百一十三条 GMP目录 目录 目录 新版GMP认识 新版GMP认识 质量源于设计生产重现质量体系保证质量临床实现质量注册与现实工艺的一致性 GMP目标 防止污染 交叉污染 混淆 减少差错 产品 工艺设计厂房设计设备选取选型 人为差错 一种产品装入另外一种包装 生产产品的各种信息错误 标签 说明书 将不合格的产品混入了合格产品 错误的计算过程导致结果判定错误 称量等 污染的可能性 污染 包括微生物 其他活性成分 你的清洁操作彻底么 设备难清洁部位重点清洁了么 外来人员进入生产现场你严格控制了么 你是否从来不带饰物进入生产区 你是否从来不将非工作物质带入生产区 建立严格的质量保证体系 确保产品质量 由于生产药品存在很多风险 所以我们必须建立严格的质量管理体系 应该作什么What 为什
2、么这样做Why 什么时候做When谁来做Who在哪做Where 应该如何作Howto 成本Howmuch工作量Howmany 人员 最重要的一环 最重要的资源 最大的风险人合格了 产品才能合格人员培训技能培训GMP QA培训卫生培训产品培训其他 人员要求 第十六条企业应当建立与药品生产相适应的管理机构 并有组织机构图 第十八条企业应当配备足够数量并具有适当资质 含学历 培训和实践经验 的管理和操作人员 应当明确规定每个部门和每个岗位的职责 岗位职责不得遗漏 交叉的职责应当有明确规定 每个人所承担的职责不应当过多 组织机构图 第二十条关键人员应当为企业的全职人员 至少应当包括企业负责人 生产管理负责人 质量管理负责人和质量受权人 质量管理负责人和生产管理负责人不得互相兼任 质量管理负责人和质量受权人可以兼任 应当制定操作规程确保质量受权人独立履行职责 不受企业负责人和其他人员的干扰 第二十一条企业负责人企业负责人是药品质量的主要责任人 全面负责企业日常管理 为确保企业实现质量目标并按照本规范要求生产药品 企业负责人应当负责提供必要的资源 合理计划 组织和协调 保证质量管理部门独立履行其职
3、责 第二十二条生产管理负责人 一 资质 生产管理负责人应当至少具有药学或相关专业本科学历 或中级专业技术职称或执业药师资格 具有至少三年从事药品生产和质量管理的实践经验 其中至少有一年的药品生产管理经验 接受过与所生产产品相关的专业知识培训 第二十三条质量管理负责人 一 资质 质量管理负责人应当至少具有药学或相关专业本科学历 或中级专业技术职称或执业药师资格 具有至少五年从事药品生产和质量管理的实践经验 其中至少一年的药品质量管理经验 接受过与所生产产品相关的专业知识培训 第二十五条质量受权人 一 资质 质量受权人应当至少具有药学或相关专业本科学历 或中级专业技术职称或执业药师资格 具有至少五年从事药品生产和质量管理的实践经验 从事过药品生产过程控制和质量检验工作 质量受权人应当具有必要的专业理论知识 并经过与产品放行有关的培训 方能独立履行其职责 二 主要职责 1 参与企业质量体系建立 内部自检 外部质量审计 验证以及药品不良反应报告 产品召回等质量管理活动 2 承担产品放行的职责 确保每批已放行产品的生产 检验均符合相关法规 药品注册要求和质量标准 3 在产品放行前 质量受权人必须
4、按照上述第2项的要求出具产品放行审核记录 并纳入批记录 QP责任 QP释放产品需要考虑的正式的产品批记录审核 评估支持数据中控测试最终检验环境数据 偏差 变化 是否始终符合所有注册要求 人员培训 第二十六条企业应当指定部门或专人负责培训管理工作 应当有经生产管理负责人或质量管理负责人审核或批准的培训方案或计划 培训记录应当予以保存 第二十七条与药品生产 质量有关的所有人员都应当经过培训 培训的内容应当与岗位的要求相适应 除进行本规范理论和实践的培训外 还应当有相关法规 相应岗位的职责 技能的培训 并定期评估培训的实际效果 第二十八条高风险操作区 如 高活性 高毒性 传染性 高致敏性物料的生产区 的工作人员应当接受专门的培训 人员部分文件 组织机构管理规程上岗证管理规程员工培训管理规程员工体检管理规程外来人员参观管理规程 记录表格 员工登记表员工上岗证员工送外培训记录员工培训记录表 年度培训计划员工培训卡员工培训签到表健康档案人员健康汇总表车间外来人员登记表 人员卫生 第二十九条所有人员都应当接受卫生要求的培训 企业应当建立人员卫生操作规程 最大限度地降低人员对药品生产造成污染的风险 第
5、三十条人员卫生操作规程应当包括与健康 卫生习惯及人员着装相关的内容 生产区和质量控制区的人员应当正确理解相关的人员卫生操作规程 企业应当采取措施确保人员卫生操作规程的执行 第三十一条企业应当对人员健康进行管理 并建立健康档案 直接接触药品的生产人员上岗前应当接受健康检查 以后每年至少进行一次健康检查 第三十二条企业应当采取适当措施 避免体表有伤口 患有传染病或其他可能污染药品疾病的人员从事直接接触药品的生产 第三十三条参观人员和未经培训的人员不得进入生产区和质量控制区 特殊情况确需进入的 应当事先对个人卫生 更衣等事项进行指导 第三十四条任何进入生产区的人员均应当按照规定更衣 工作服的选材 式样及穿戴方式应当与所从事的工作和空气洁净度级别要求相适应 第三十五条进入洁净生产区的人员不得化妆和佩带饰物 第三十六条生产区 仓储区应当禁止吸烟和饮食 禁止存放食品 饮料 香烟和个人用药品等非生产用物品 第三十七条操作人员应当避免裸手直接接触药品 与药品直接接触的包装材料和设备表面 卫生管理规程 人员卫生管理规程厂区环境卫生管理规程工作服的管理规程废弃物的管理规程一般生产区环境卫生管理规程一般生产
《药品生产过程与GMP管理》由会员87641****q.com分享,可在线阅读,更多相关《药品生产过程与GMP管理》请在金锄头文库上搜索。

sap发票校验两个常用的用户参数

2-质量管理访谈提纲(质量管理)

MCPC-SAP-萌蒂制药现状与需求调研-Ver20

SAP文档_PWC给大唐电讯的SAP系统实施项目建议书

SAP-S4HANA-L1forIT-ChineseSimplified
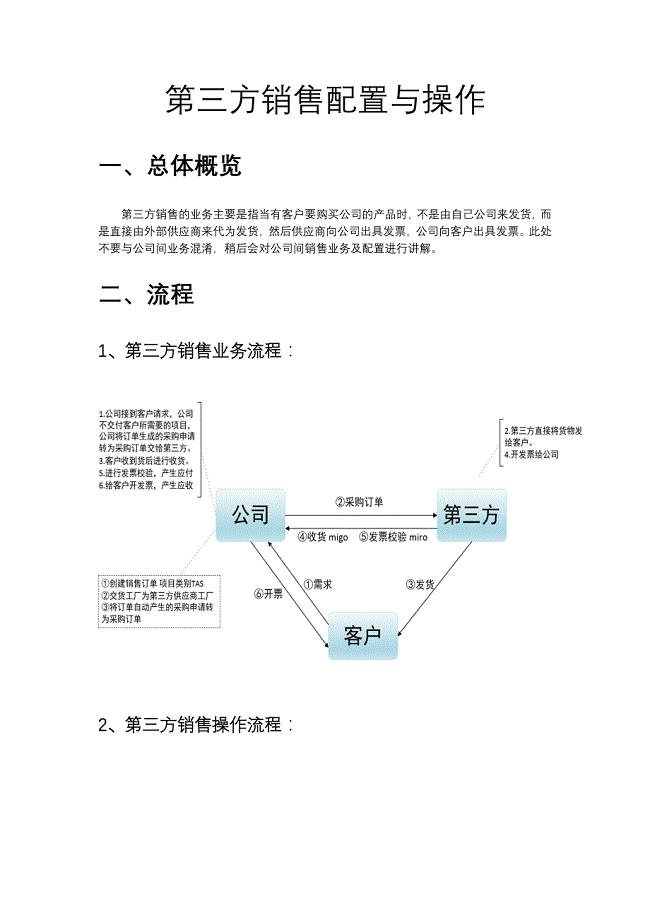
SAP文档_(原创)_第三方销售配置与操作

SAP文档(原创)_定义合作伙伴(供应商)的后台配置及前台操作

江山制药ERP咨询项目_主计划流程v2.2

SAP文档_毕博PPT图库

SAP-S4HANA-Fin-Fiori

ERP与条码接口解决方案

ERP标准业务流程

SAP-医药行业解决方案

SAP-MRP-logic

条码管理信息化解决方案

药品生产过程与GMP管理

江山制药ERP咨询项目_退货处理交流v1.5

sap需求管理(计划策略)

%92%A8询项目_招标文件第三卷_招标文件附件v1.1

条码管理系统解决方案(初稿第一版)
 SPC统计制程控制运用实务(DOC 106)
SPC统计制程控制运用实务(DOC 106)
2023-03-09 106页
 大数据中心建设思路(电网方案 81P PPT)
大数据中心建设思路(电网方案 81P PPT)
2023-02-20 81页
 SPC统计制程控制运用实务(DOC 106)(1)
SPC统计制程控制运用实务(DOC 106)(1)
2023-02-20 106页
 柏维公司员工手册行为准则(doc 38页)
柏维公司员工手册行为准则(doc 38页)
2023-02-20 130页
 500强企业绩效考核指标汇总(ppt3个doc1个chm1个)9
500强企业绩效考核指标汇总(ppt3个doc1个chm1个)9
2023-02-20 68页
 MBTI性格的管理测验(doc 82页)
MBTI性格的管理测验(doc 82页)
2023-02-20 82页
 绩效管理系统 (3)
绩效管理系统 (3)
2022-07-12 66页
 绩效管理与工作分析的理论与实践)
绩效管理与工作分析的理论与实践)
2022-07-12 178页
 管理工作培训
管理工作培训
2022-07-12 67页
 某公司职能部门岗位说明与KPI考核指标)
某公司职能部门岗位说明与KPI考核指标)
2022-07-12 198页

