
精修版高考化学一轮总复习练习:第10章 化学实验 第3节 含答案
7页1、精品文档高考化学第一部分第十章第三节一、选择题1(2015山东淄博模拟)下列制取二氧化碳的装置中,不能做到“随时控制反应的发生与停止”的是 ()解析:A项装置当关闭止水夹时,继续反应生成的气体不能将盐酸完全排到漏斗中,反应物之间不能分离,反应不会停止,故不是“随时控制反应的发生与停止”的制气装置。答案:A2(2015辽宁抚顺二中期中)下列仪器和装置,用橡胶管经过简单连接,可制备收集多种不同的纯净、干燥的气体(考虑有毒尾气吸收)。关于这些装置的连接,下列说法正确的是 ()A制备收集Cl2:连接afcedB制备收集H2:连接bcgC制备收集CO2:连接bdeD制备收集NH3:连接bdec解析:B项,用排水法收集不到干燥的气体,故该项不正确;CO2不能用碱石灰来干燥,故C项不正确;由于氨气极易与浓硫酸反应,吸收尾气时导管插入液面下易发生倒吸,故D项不正确。答案:A3(2015安徽江南十校联考)用下图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是 ()选项甲乙丙试管中现象A浓盐酸二氧化锰石蕊试液先变红后褪色B浓氨水生石灰AlCl3溶液先沉淀后消失
2、C醋酸碳酸钙BaCl2溶液变浑浊D浓硝酸铜水试管口出现红棕色解析:浓盐酸与二氧化锰制备氯气需要加热,此装置没加热无法制得氯气,A错误;B项生成的氢氧化铝沉淀不溶于氨水,B错误;二氧化碳与BaCl2溶液不反应,无浑浊出现,C错误;浓硝酸与铜反应产生二氧化氮,二氧化氮与水反应产生一氧化氮,一氧化氮易被氧化为二氧化氮,故试管口出现红棕色,D正确。答案:D4(2015湖南衡阳模拟)用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述中正确的是 ()A若A为浓盐酸,B为MnO2,C中盛品红溶液,证明氯气具有“漂白性”B若A为醋酸,B为贝壳,C中盛氯化钙溶液,证明醋酸的酸性比碳酸强C若A为浓氨水,B为生石灰,C中盛AlCl3溶液,证明氢氧化铝能溶于碱性溶液D实验仪器D可以起到防止溶液倒吸的作用解析:浓盐酸和MnO2反应制取氯气需在加热条件下进行,故A项不正确;二氧化碳不与氯化钙反应,无法用氯化钙溶液证明有二氧化碳生成,故B项不正确;氢氧化铝不溶于氨水等弱碱溶液,故C项不正确。答案:D5(2016届黑龙江省哈尔滨第六中学高三上期中)下列各图所示的实验原理、方法、装置或操作,其中正确的是 ()解析
3、:A.向容量瓶中转移溶液时需要玻璃棒引流,A错误;B.该装置可以用于中和热的测定,B正确;C.SO2是酸性氧化物,应该用浸有氢氧化钠的棉花放在试管口,C错误;D.由于草酸易挥发,与氢氧化钙反应生成醋酸钙也是白色沉淀,会干扰乙二酸晶体受热分解生成的CO2,D错误,答案选B。答案:B6(2016届江西省余江县第一中学高三二模)现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:有关说法错误的是 ()A反应原理为CO2NH3NaClH2O=NaHCO3NH4ClB向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3C反应生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱DCO2的结构式为O=C=O,其中碳氧原子均满足8电子稳定结构解析:饱和氯化钠中通入氨气和二氧化碳生成碳酸氢钠沉淀和氯化铵,碳酸氢钠受热分解生成碳酸钠和二氧化碳和水。A.由发生的反应可知反应原理为CO2NH3NaClH2O=NaHCO3NH4Cl,故A正确;B.氯化钠饱和溶液中二氧化碳的浓度较小,所以应该向饱和氯化钠溶液中先通入足量的氨气,后通入足量的二氧化碳,错误,选B;C.根据反应生成的沉淀,经过过滤、洗涤、
4、煅烧可得到纯碱,正确,不选C;D.在二氧化碳分子中碳原子和氧原子之间形成两对共用电子对,所以结构式为O=C=O,碳原子和氧原子都满足8电子结构,正确,不选D。答案:B7(2016届广西省钦州港经济技术开发区中学高三上学期期中)下列根据实验操作和现象所得出的结论不正确的是 ()选项实验操作实验现象结论A向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去2 min后,试管里出现凝胶酸性:盐酸硅酸B在酒精灯上加热铝箔铝箔熔化但不滴落熔点:氧化铝铝C常温下,向浓硫酸中投入铁片铁片不溶解常温下,铁不与浓硫酸反应D向某溶液中先滴加KSCN溶液,再滴加少量氯水先无明显现象,后溶液变成血红色溶液中含有Fe2,没有Fe3解析:考查了化学实验方案的设计的相关知识。A.试管里出现凝胶,说明生成硅酸,根据强酸制备弱酸的原理可知酸性:盐酸硅酸,故A正确;B.铝箔熔化但不滴落,原因是表面生成氧化铝膜,熔点较高,即熔点:氧化铝铝,故B正确;C.铁与浓硫酸发生钝化反应,而不是不反应,原因是在表面生成一层致密的氧化物膜而阻碍反应的进行,故C错误;D.先无明显现象,后溶液变成血红色,说明溶液中含有Fe2,没有Fe3
《精修版高考化学一轮总复习练习:第10章 化学实验 第3节 含答案》由会员壹****1分享,可在线阅读,更多相关《精修版高考化学一轮总复习练习:第10章 化学实验 第3节 含答案》请在金锄头文库上搜索。

科长上任表态讲话材料模板(2篇)

全县经济工作会议上县委书记讲话稿

加强环境监测全过程质量管理全面提升环境监测水平

金蝶K3产品性能稳定性优化指导手册

201X学年学生会外联部工作总结【可编辑版】.doc

八年级上册第五课

小学数学案例与反思 (2)

控股公司章程

(精选模板)2022情人节活动策划方案范文集锦八篇
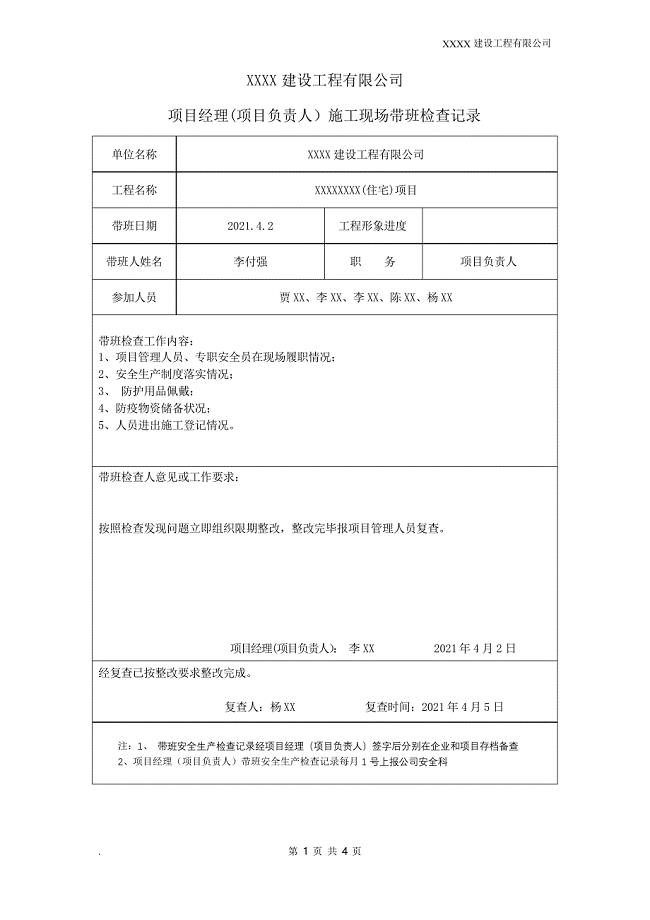
项目施工现场带班检查记录

幼儿园小班班级工作总结

防汛减灾工作总结(4篇).doc

房地产物业维修服务管理流程

在职考研-面对工作和学习该如何处理

在科学课中培养学生观察能力“四步曲”

如皋市培育新型消费项目申请报告_参考模板

读《做最好的自己》有感1000字

活动的计划
![福建厦门工学院政务处专员公开招聘1人模拟试卷【附答案解析】[5]](https://union.152files.goldhoe.com/2022-9/13/0fd6ef5a-bbb1-43ba-b236-f6c1226d7020/pic1.jpg)
福建厦门工学院政务处专员公开招聘1人模拟试卷【附答案解析】[5]

2022年毕业班学生演讲稿精选五篇简短范文
 【最新教材】数学同步优化指导北师大版选修22练习:第3章 2.2 最大值、最小值问题 活页作业14 Word版含解析
【最新教材】数学同步优化指导北师大版选修22练习:第3章 2.2 最大值、最小值问题 活页作业14 Word版含解析
2023-11-17 8页
 第三章3噪声教科版八年级物理上册检测
第三章3噪声教科版八年级物理上册检测
2023-06-23 6页
 2022年危险化学品生产单位主要负责人资格证考试内容及题库模拟卷31【附答案】
2022年危险化学品生产单位主要负责人资格证考试内容及题库模拟卷31【附答案】
2023-05-15 18页
 常规压力对采用非牛顿学流体润滑的光滑碟片
常规压力对采用非牛顿学流体润滑的光滑碟片
2023-03-14 27页
 2022年建筑施工专职安全员【安全员C证】全国通用考试历年真题汇总含答案参考69
2022年建筑施工专职安全员【安全员C证】全国通用考试历年真题汇总含答案参考69
2023-09-15 21页
 大班科学教案纸的力量
大班科学教案纸的力量
2023-11-09 4页
![初中化学实验题汇编[1]](/Images/s.gif) 初中化学实验题汇编[1]
初中化学实验题汇编[1]
2024-01-24 10页
 第三章空气氧气燃烧2012-9-19周三班学生版
第三章空气氧气燃烧2012-9-19周三班学生版
2022-08-26 9页
 认识时间参考教案2
认识时间参考教案2
2023-08-10 6页
 空浴式汽化器使用说明书
空浴式汽化器使用说明书
2023-09-27 8页

