
药品生产质量管理规范-细胞治疗产品附录
23页1、药品生产质量管理规范-细胞治疗产品附录第一章 范 围第一条【范围】 本附录所述的细胞治疗产品(以下简称细胞产品)是指人源的活细胞产品,包括经过或未经过基因修饰的细胞,如自体或异体的免疫细胞、干细胞、组织细胞或细胞系等产品,不包括输血用的血液成分、已有规定的移植用造血干细胞、生殖相关细胞,以及由细胞组成的组织、器官类产品等。第二条【适用范围】 本附录适用于细胞产品从供者材料的运输、接收、产品生产和检验到成品放行、储存和运输的全过程。直接用于细胞产品生产的基因修饰载体或其他起始生物材料(包括:病毒、质粒、RNA、抗原肽、抗原蛋白、蛋白-RNA复合体等)的生产、检验和放行等过程应符合现行版药品生产质量管理规范正文及其相关附录以及本附录的要求。第三条【通用要求】 因细胞产品的供者材料来源于人体,其生产还应当符合国家相关规定,防止引入或传播传染病病原体。第二章 原 则第四条【特殊性】 细胞产品具有以下特殊性:【供者材料的安全性】 供者材料来源于人体,可能含有传染病病原体;【生产工艺特点】 供者材料的质量受其来源、类型、特性等因素影响,具有差异性。受其影响,产品生产工艺可能需要根据供者材料的质量差
2、异,并在产品注册批准的范围内进行必要的调整;【生产批量特点】 受供者材料来源及使用范围的限制,产品生产批量通常较小,生产组织模式相对灵活,生产与临床需求结合更为紧密;【温度的影响】 温度对供者材料和产品的质量具有更为显著的影响;【防止污染和交叉污染】 供者材料采集后的生产过程,由于产品为活细胞,容易受到微生物污染或交叉污染,且污染物不易去除;【防止混淆和差错】 自体细胞产品或采用异体供者材料生产的需与患者配型使用的产品,一旦发生混淆,造成供者材料或细胞与患者之间的不匹配,可能会对患者产生危及生命的严重后果。第五条【特殊控制】 鉴于细胞产品的以上特殊性,企业应当对供者材料采集和产品生产的全过程采取特殊控制措施,至少包括:对产品及其从供者材料的接收直至成品储存运输的全过程进行风险评估,制定相应的风险控制策略,以保证产品的安全、有效和质量可控;建立生物安全管理制度和记录,具有保证生物安全的设施、设备,预防和控制产品生产过程中的生物安全风险,防止引入、传播病原体;在供者材料运输、接收及产品生产、储存、运输全过程中监控产品或生产环境的温度及操作时限,确保在规定的温度和时限内完成相应的操作;产品生
3、产全过程应当尤其关注防止微生物污染或交叉污染,包括载体的生产过程可能对产品带来的交叉污染,以及不同载体生产过程中可能存在的交叉污染等;从供者材料采集到患者使用的全过程中,产品应当予以正确标识且可追溯,防止混淆和差错。第三章 人 员第六条【关键人员资质】 生产管理负责人、质量管理负责人和质量受权人应当具有相应的专业知识(微生物学、生物学、免疫学、生物化学、生物制品学等),并能够在生产、质量管理中履行职责。第七条【人员安全防护培训】 从事细胞产品生产、质量保证、质量控制及其他相关人员(包括清洁、维修人员)应当经过生物安全防护的培训,尤其是预防经供者材料传播传染病病原体的相关知识培训,所有培训内容应符合国家关于生物安全的相关规定。第八条【人员活动限制】 生产期间,未按规定采取有效的去污染措施,从事载体生产的人员不得进入细胞产品的生产区域,接触含有传染病病原体供者材料的人员不得进入其他生产区域。第四章 厂房、设施与设备第九条【厂房分区设计】 直接用于细胞产品生产的基因修饰病毒载体应与细胞产品及其他载体或生物材料分别在各自独立的生产区域进行,并配备独立的空调净化系统。第十条【含有传染病病原体的供
4、者材料生产厂房要求】 使用含有传染病病原体的供者材料生产细胞产品时,其生产操作应当在独立的专用生产区域进行,并采用独立的空调净化系统,保持产品暴露于环境的生产区域相对负压。第十一条【密闭系统】 宜采用密闭系统或设备进行细胞产品的生产操作;密闭系统或设备放置环境的洁净度级别可适当降低。第十二条【生产操作环境的洁净度级别】 细胞产品、直接用于细胞产品生产的基因修饰载体或其他起始生物材料,其生产操作环境的洁净度级别可参照表格中的示例进行选择。洁净度级别细胞产品生产操作示例B级背景下的A级1.处于未完全密闭状态下的生产操作和转移;2.无法除菌过滤的溶液、培养基的配制;3.载体除菌过滤后的分装。C级背景下的局部A级1.生产过程中采用注射器对处于密闭状态下的产品和生产用溶液进行取样;2.病毒载体生产用细胞的传代操作;3.可除菌过滤的溶液和培养基的配制;4.载体的除菌过滤。C级1.采用非密闭系统(如使用透气盖的细胞培养瓶等)在培养箱中培养;2.载体的纯化操作。D级1.采用密闭管路转移产品、溶液或培养基;2.采用密闭系统或设备进行细胞产品、载体的生产操作(如在隔离器中进行产品的无菌分装)、取样;3.质
《药品生产质量管理规范-细胞治疗产品附录》由会员AL****EE分享,可在线阅读,更多相关《药品生产质量管理规范-细胞治疗产品附录》请在金锄头文库上搜索。

二零二二年版化妆品生产质量管理规范

药品生产质量管理规范-细胞治疗产品附录
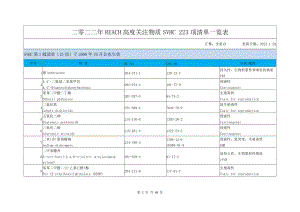
二零二二年REACH高度关注物质SVHC 223项清单一览表

BIQS-供应商BIQ策略-2分层审核专题培训教材
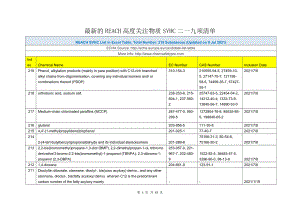
最新的REACH高度关注物质SVHC二一九项清单
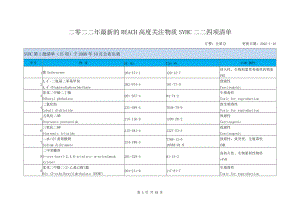
二零二二年最新的REACH高度关注物质SVHC二二四项清单

化妆品生产电子记录要求及化妆品生产车间环境要求

降低汽车冲压模具成本的措施分析

2022年春运工作的要求

消防设备设施维护保养标准要求

学习解读新食品生产经营监督检查管理办法

人员密集场所消防管理标准要求

学习解读二零二二年新食品生产经营监督检查管理办法

公司EHS检查记录表

2021-2025年残疾预防行动计划

共同富裕是社会主义的本质要求

食品安全HACCP认证的文件要求清单

食品企业厂房建设卫生设计的原则

最新的公共场所新型冠状病毒感染的肺炎卫生防护指南

注塑机电磁阀的安装要求作业指引
 八一广场心得体会(大全15篇)
八一广场心得体会(大全15篇)
2024-04-28 23页
 企业法务工作总结汇报(实用8篇)
企业法务工作总结汇报(实用8篇)
2024-04-28 21页
 关于专项整治整改及感悟
关于专项整治整改及感悟
2024-04-28 34页
 主题银行案防述职怎么写
主题银行案防述职怎么写
2024-04-28 4页
 主题评估土地承包金申请书及感悟(5篇)
主题评估土地承包金申请书及感悟(5篇)
2024-04-28 18页
 倾听心声心得体会(通用10篇)
倾听心声心得体会(通用10篇)
2024-04-28 19页
 主题能力作风建设年学习体会范文(七篇)
主题能力作风建设年学习体会范文(七篇)
2024-04-28 32页
 亲子合作协议书(优质10篇)
亲子合作协议书(优质10篇)
2024-04-28 19页
 企业混改协议书(模板8篇)
企业混改协议书(模板8篇)
2024-04-28 37页
 主题窗口人员业务不精整改措施报告(四篇)
主题窗口人员业务不精整改措施报告(四篇)
2024-04-28 32页

