
河南省南阳市高三上学期期中化学试卷
9页1、河南省南阳市高三上学期期中化学试卷姓名:_ 班级:_ 成绩:_一、 选择题 (共7题;共14分)1. (2分) (2018高一下泰州期末) 下列有关物质的性质与用途具有对应关系的是( ) A . 二氧化锰具有较强的氧化性,可作H2O2分解的氧化剂B . 铝能置换出氧化铁中的铁,可用于钢铁工业中大量冶炼铁C . AlCl3是电解质,可电解熔融AlCl3制铝D . 油脂能在碱性条件下水解,可用于工业上制取肥皂2. (2分) 同温同压下,a g甲气体和2a g乙气体所占的体积之比为1:2,根据阿伏伽德罗定律判断,下列叙述不正确的是( ) A . 同温同压下甲和乙的密度之比为1:1B . 等质量的甲和乙中的原子数之比为1:1C . 同温同体积下等质量的甲和乙的压强之比为1:1D . 甲与乙的相对分子质量之比为1:13. (2分) (2016高三上厦门期中) 下列实验中,对应的现象及结论都正确且存在因果关系的是( ) 选项实验现象结论A加热莫尔盐(NH4)2Fe(SO4)26H2O,产生的气体通过装有无水硫酸铜的干燥管干燥管中白色粉末先变成天蓝色,后又变成深蓝色温度较低时莫尔盐分解产生水蒸气,温
2、度稍高时分解产物中有氨气B向KMnO4溶液中通入SO2气体溶液紫红色褪去SO2具有漂白性C向某溶液中先滴加稀硝酸,再滴加Ba(NO3)2溶液出现白色沉淀溶液中一定含有SO42D取1mL 20%的蔗糖溶液,加入35滴稀硫酸水浴加热5min后取少量溶液,加入少量新制Cu(OH)2 , 加热4min未产生砖红色沉淀蔗糖不能水解生成葡萄糖A . AB . BC . CD . D4. (2分) (2018高三下城中开学考) 下列指定反应的离子方程式正确的是( ) A . 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4 + 8H+= Fe2+ + 2Fe3+ + 4H2OB . 向Na2O2中加入足量水:2Na2O22H2O = 4Na4OHO2C . 少量CO2通入苯酚钠溶液:2C6H5OCO2H2O 2C6H6OCO32D . 用醋酸溶解大理石:CaCO32H+ = Ca2+H2OCO25. (2分) (2016高一上辽源期中) 对于某些离子的检验及结论一定正确的是( ) A . 向某溶液中加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32B . 向某溶液中加
3、入氯化钡溶液有白色沉淀产生,再加稀硝酸,沉淀不消失,则原溶液中一定有Ag+C . 向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生,则原溶液中一定有SO42D . 向某溶液中加入加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液一定有Ba2+6. (2分) (2018高三上周口开学考) NA表示阿伏加德罗常数的值,下列说法正确的是( ) A . 标准状况下,11.2 L水中含有分子的数目为0.5NAB . 100 mL 0.2 molL1的FeCl3溶液中,含Fe3数为0.02NAC . 1 mol Cl2与足量的NaOH溶液反应,转移的电子数为1NAD . 在密闭容器中加入0.5 mol N2和1.5 mol H2 , 充分反应后可得到NH3分子数为NA7. (2分) (2019高二上奉贤期中) 已知下列三个反应:2Fe2+Cl22Fe3+2Cl- 2Fe3+Cu2Fe2+Cu2+ Fe+Cu2+Fe2+Cu试推断结论:具有还原性物质的还原性强弱:FeCuFe2+Cl- Cl-Fe2+FeCu具有氧化性物质的氧化性强弱:Fe3+Cl2Fe2+Cu2
《河南省南阳市高三上学期期中化学试卷》由会员pu****.1分享,可在线阅读,更多相关《河南省南阳市高三上学期期中化学试卷》请在金锄头文库上搜索。

AES加密算法在用户信息管理模块中的应用毕业设计论文

东北大学21春《公路勘测与设计原理》离线作业2参考答案71

市政基础设施工程施工技术文件—2

行政主管个人年终工作总结模板(5篇)

油库设备安装施工方案

数列题型错位相减法

一创建绿色校园,从我做起

关于公司年会策划汇总8篇

高效率恒流源电路的设计

贷款优先等级知识

山中访友读后感小学生文档山中访友读后感小学生文档大全

注册会计师《财务成本管理》考前(难点+易错点剖析)押密卷答案参考6
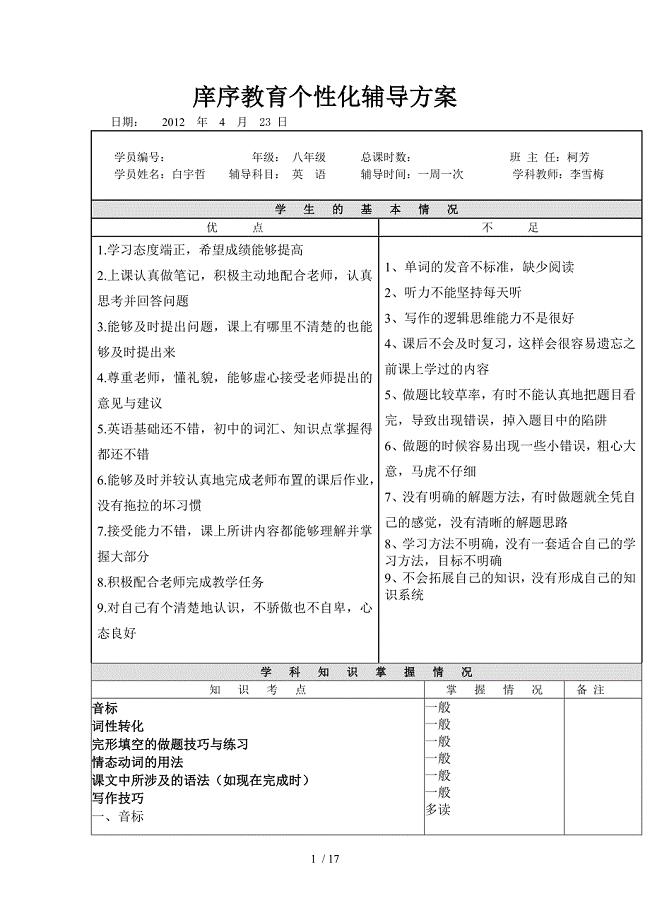
白宇哲个性化辅导方案

“六一”活动总结

网络多媒体信息发布系统NMIDS

励志演讲稿范文:这里有我们的梦

2023年四川省资阳市雁江区祥符镇祥符寺社区工作人员考试模拟试题及答案

光棍节励志语录

云遮不断归途-1500字

掌声2(教育精品)
 高一(上)化学期末试题双向细目表
高一(上)化学期末试题双向细目表
2022-08-20 2页
 2014年安徽高考数学(理)卷文档版(有答案)
2014年安徽高考数学(理)卷文档版(有答案)
2023-04-12 10页
 新课标高三语文模拟题(含详细答案)Word版
新课标高三语文模拟题(含详细答案)Word版
2023-05-05 20页
 2022高考数学一轮复习课时规范练39平行关系文含解析北师大版
2022高考数学一轮复习课时规范练39平行关系文含解析北师大版
2022-11-11 10页
 高一物理第一次月考
高一物理第一次月考
2022-08-17 5页
 打造高中英语高效课堂
打造高中英语高效课堂
2023-10-02 7页
 备考高考作文素材精美哲理散文十
备考高考作文素材精美哲理散文十
2023-01-04 11页
 高考数学导数题型归纳
高考数学导数题型归纳
2023-10-02 12页
 江苏省高一化学 周练一 物质的分类与转化 物质的量
江苏省高一化学 周练一 物质的分类与转化 物质的量
2023-09-11 3页
 2022年高三第一次月考(化学)(II)
2022年高三第一次月考(化学)(II)
2022-11-27 7页

