
(重庆专用)2014届高考化学二轮复习 第7讲 水溶液中的离子平衡训练试题
8页1、第7讲水溶液中的离子平衡(时间:45分钟分值:100分)一、选择题(共7个小题,每小题6分,共42分)1(2013潍坊高三模拟)下列溶液一定呈中性的是()。Ac(H)c(OH)106 molL1的溶液BpH7的溶液C使石蕊试液呈紫色的溶液D酸与碱恰好完全反应生成正盐的溶液解析当温度为100 时,pH6时呈中性,pH7的溶液呈碱性,B错;石蕊呈紫色时,pH为58,此时溶液可能呈酸性、中性或碱性,C错;CH3COOH与NaOH恰好反应生成的CH3COONa水解使溶液显碱性,D错;只有c(H)c(OH)的溶液一定呈中性。答案A2(2013重庆市高三模拟)下列说法正确的是()。A0.1 molL1的醋酸溶液加水稀释,减小B体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),后者用时少C向水中加入少量固体硫酸氢钠,c(H)增大,KW变大D常温下,V1 L pH11的NaOH溶液与V2 L pH3的HA溶液混合,若混合液显中性,则V1V2解析向水中加入少量固体硫酸氢钠,c(H)增大,但KW只与温度有关,故KW保持不变,C错;若HA为强酸,则V1V2,若HA为弱酸,则V1V2,D错。答案A3(2
2、013天津化学,5)下列有关电解质溶液的说法正确的是()。A在蒸馏水中滴加浓H2SO4,KW不变BCaCO3难溶于稀硫酸,也难溶于醋酸C在Na2S稀溶液中,c(H)c(OH)2c(H2S)c(HS)DNaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同解析浓H2SO4溶于水,放热,温度升高,KW增大,A错误;CaCO3能与CH3COOH发生反应:CaCO32CH3COOH= Ca(CH3COO)2CO2H2O,生成了易溶于水的乙酸钙,所以CaCO3能溶于醋酸,B错误;在Na2S溶液中存在着电荷守恒:c(H)c(Na)c(OH)c(HS)2c(S2)和物料守恒:c(Na)2c(S2)c(HS)c(H2S)可得c(H)c(OH)2c(H2S)c(HS),C正确;由于CH3COO和NH的水解促进了水的电离且促进程度相同,而Na和Cl不发生水解,故NaCl溶液中水的电离程度小于CH3COONH4溶液中水的电离程度,D错误。答案C4(2013湖南十二校第一次联考,5)下列说法正确的是()。A在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大B可用碱式滴定管量取1
3、3.50 mL高锰酸钾溶液CFeCl3溶液蒸干灼烧,得到纯净的FeCl3晶体D常温下,0.1 molL1的溶液中,Na、K、CO、NO可大量共存解析Ksp只与难溶物的性质、温度有关,A错误;高锰酸钾溶液具有氧化性,所以不能用碱式滴定管量取,B错误;FeCl3溶液加热时发生水解反应,生成Fe(OH)3,灼烧后,Fe(OH)3分解生成Fe2O3,不能得到FeCl3晶体,C错误;该溶液呈碱性,各离子可以大量共存,D正确。答案D5(2013武隆高三检测)25 时,5种银盐的溶度积常数(Ksp)分别是:AgClAg2SO4Ag2SAgBrAgI1.810101.41056.310507.710138.511016下列说法正确的是()。A氯化银、溴化银和碘化银的溶解度依次增大B将硫酸银溶解于水后,向其中加入少量硫化钠溶液,不可能得到黑色沉淀C在5 mL 1.8105 molL1的NaCl溶液中,加入1滴(1 mL约20滴)0.1 molL1的AgNO3溶液,不能观察到白色沉淀D将浅黄色溴化银固体浸泡在饱和氯化钠溶液中,可以有少量白色固体生成解析A选项在组成类型相同时,可以利用Ksp直接比较盐的溶解
4、度,Ksp值越小越难溶,所以氯化银、溴化银、碘化银溶解度依次减小,错误;B选项硫酸银的Ksp大于硫化银的Ksp,因此会有更难溶的黑色硫化银生成,错误;C选项,c(Ag)0.001 molL1,Qc0.001 molL11.8105 molL11.8108 mol2/L2,大于氯化银的Ksp,故会有白色沉淀生成,错误;D选项在氯化钠的饱和溶液中,氯离子的浓度大约是8 molL1,溴化银固体浸泡在其中,会使氯离子与银离子离子积大于其溶度积,所以会有少量白色固体生成,D正确。答案D6(2013重庆理综,2)下列说法正确的是()。AKClO3和SO3溶于水后能导电,故KClO3和SO3为电解质B25 时,用醋酸溶液滴定等浓度NaOH溶液至pH7,V醋酸VNaOHC向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成DAgCl沉淀易转化为AgI沉淀且K(AgX)c(Ag)c(X),故K(AgI)K(AgCl)解析A项,SO3为非电解质,错误。B项,若V醋酸VNaOH,则pH7,若pH7,应醋酸过量,V醋酸应大于VNaOH,错误。C项,向NaAlO2溶液中滴加NaHCO3溶液,仅有沉淀生成,
《(重庆专用)2014届高考化学二轮复习 第7讲 水溶液中的离子平衡训练试题》由会员s9****2分享,可在线阅读,更多相关《(重庆专用)2014届高考化学二轮复习 第7讲 水溶液中的离子平衡训练试题》请在金锄头文库上搜索。

中国石油大学华东21春《混凝土与砌体结构》离线作业一辅导答案75

湖南省浏阳一中、攸县一中高三上学期期中联考语文 试题及答案

2023年医院药剂师个人年终总结报告(4篇).doc

FCZ磁力驱动反应釜使用规程

2023学年第一学期二年级数学教学工作总结(4篇).doc

小桥流水人家

外墙真石漆劳务合同(2)

农业产业化龙头企业工作总结
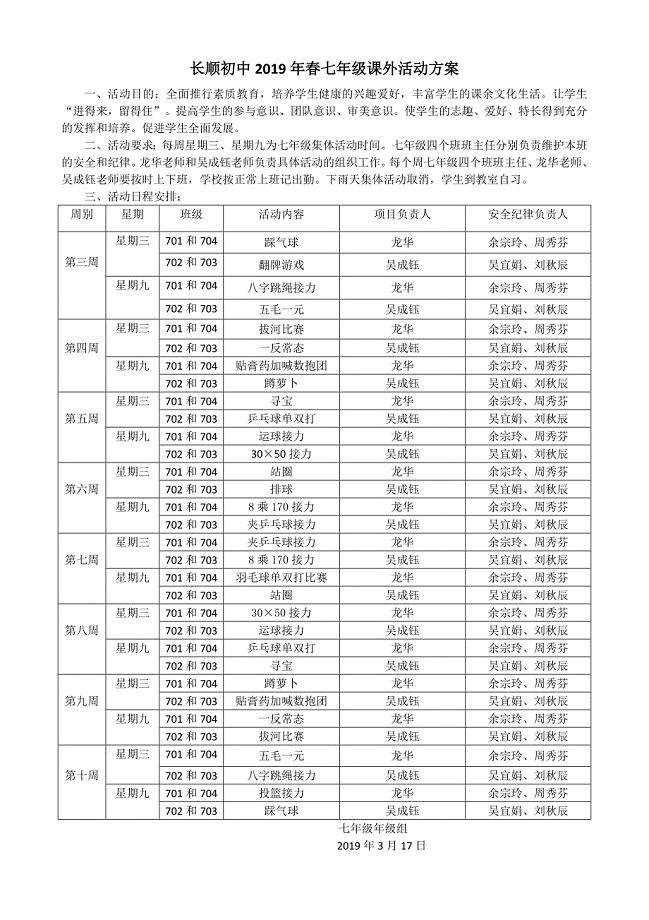
长顺初中2019年春七年级课外活动方案

志向点亮人生演讲稿

(完整word版)锅炉安全知识培训题

2013年上海高考物理试题以及答案详细解析版
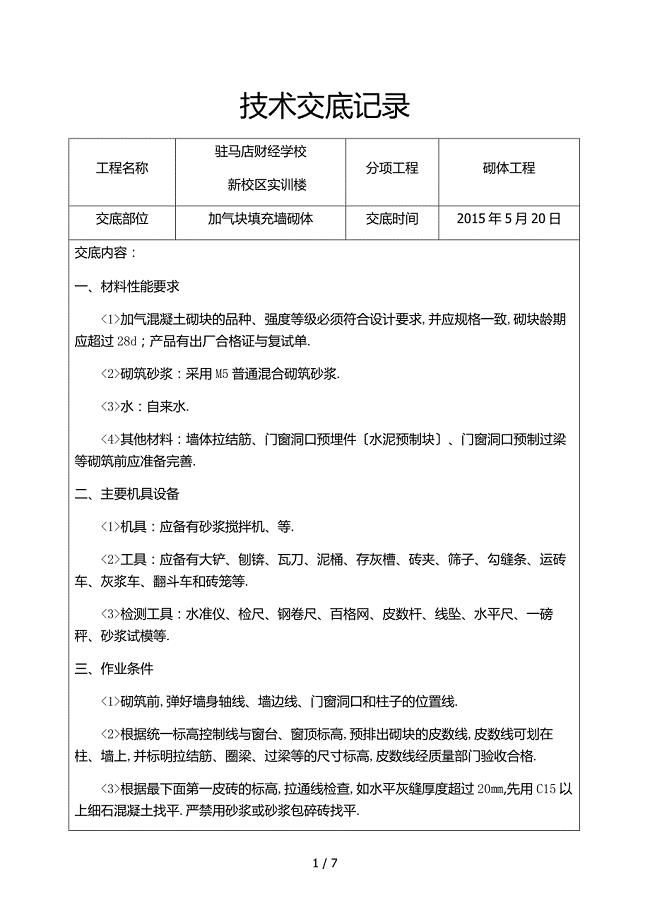
加气块砌体技术交底

教学设计-苏文平

依托绘本阅读进行创意写作的理论探索

2022出纳半年工作总结范文

如何培养学生的朗读能力

保洁年终工作总结范文(三篇).doc

适合小学生表演的相声没考好

超星尔雅-2019年批创思维导论考试满分答案(共19页)
 安徽省宿松县凉亭中学2016届高三地理上学期第二次月考试卷
安徽省宿松县凉亭中学2016届高三地理上学期第二次月考试卷
2022-10-11 8页
 高二英语下册Unit18单元教案Word版
高二英语下册Unit18单元教案Word版
2023-01-11 14页
 江苏专版2022年高考生物一轮复习鸭部分现代生物科技专题课时跟踪检测四十三胚胎工程及生物技术的安全性和伦理问题
江苏专版2022年高考生物一轮复习鸭部分现代生物科技专题课时跟踪检测四十三胚胎工程及生物技术的安全性和伦理问题
2023-04-28 6页
 2019-2020学年高中数学第二章基本初等函数Ⅰ2.1.1.2指数幂及运算课后课时精练新人教A版必修
2019-2020学年高中数学第二章基本初等函数Ⅰ2.1.1.2指数幂及运算课后课时精练新人教A版必修
2022-07-24 5页
 2010年上海市高三物理教学质量抽样分析试卷
2010年上海市高三物理教学质量抽样分析试卷
2022-08-14 9页
 2022年高三第三次模拟考试word版(英语)
2022年高三第三次模拟考试word版(英语)
2024-02-12 11页
 高中化学竞赛必备-化学初赛模拟试卷
高中化学竞赛必备-化学初赛模拟试卷
2022-11-06 8页
 高二学生提升英语水平的几点建议
高二学生提升英语水平的几点建议
2023-10-15 2页
 2014届高三上学期联考生物试题
2014届高三上学期联考生物试题
2022-10-22 11页
 2013年上海高考物理试题以及答案详细解析版
2013年上海高考物理试题以及答案详细解析版
2024-01-07 14页

