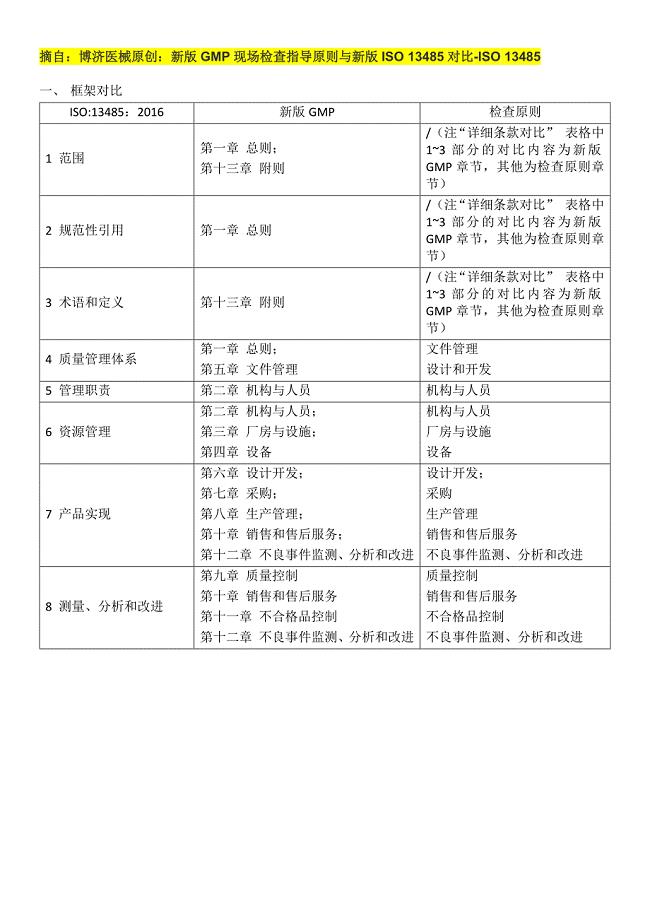
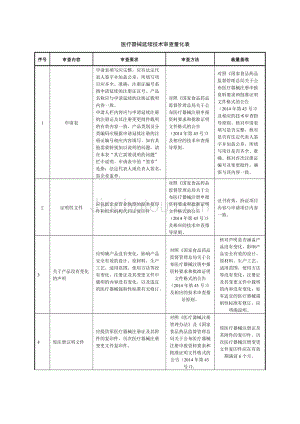
医疗器械延续技术审查量化表
4页1、医疗器械延续技术审查量化表序号审查内容审查要求审查方法裁量基准1申请表申请表填写应完整,应有法定代表人签字并加盖公章,所填写项目应齐全、准确。注册证编号系指申请延续的注册证证号。产品名称应与申请延续的注册证载明内容一致。申请人栏内容应与申请延续注册的注册证及其注册变更批件载明的有效内容一致。产品类别及分类编码应根据申请延续注册的注册证编号相应内容填写。如有其他需要特别加以说明的问题,请在本表“其它需要说明的问题”栏中说明。申请表中的“签章”是指:法定代表人或负责人签名,加企业盖章。对照国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)及相应的技术审查指导原则。对照国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)及相应的技术审查指导原则。核对申请表填写是否完整,核对是否有法定代表人签字并加盖公章,所填写项目是否齐全、准确。核对首次注册证编号及变更批件,确保与其内容一致。2证明性文件应包括企业营业执照的副本复印件和组织机构代码证复印件对照国家食品药品监督管理总局关于公布医疗器械注册申报
2、资料要求和批准证明文件格式的公告(2014年第43号)及相应的技术审查指导原则。证书有效,持证项目内容与申请项目内容一致。 3关于产品没有变化的声明应明确产品没有变化,影响产品安全有效的设计、原材料、生产工艺、适用范围、使用方法等没有变化,注册证及其变更文件中载明的内容没有变化,以及适宜的医疗器械强制性标准有无修订。对照国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)及相应的技术审查指导原则。核对声明是否涵盖产品没有变化,影响产品安全有效的设计、原材料、生产工艺、适用范围、使用方法等没有变化,注册证及其变更文件中载明的内容没有变化;如有适宜的医疗器械强制性标准有修订,应明确说明。4原注册证明文件应提供原医疗器械注册证及其附件的复印件、历次医疗器械注册变更文件复印件。 对照医疗器械注册管理办法及国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)。原医疗器械注册证及其附件的复印件、历次医疗器械注册变更文件复印件应在有效期满前6个月。5注册证有效期内产品分析报告产品分析报告应包括:(一)
3、产品临床应用情况,用户投诉情况及采取的措施。(二)医疗器械不良事件汇总分析评价报告,报告应对本产品上市后发生的可疑不良事件列表、说明在每一种情况下生产企业采取的处理和解决方案。对上述不良事件进行分析评价,阐明不良事件发生的原因并对其安全性、有效性的影响予以说明。(三)在所有国家和地区的产品市场情况说明。(四)产品监督抽验情况(如有)。(五)如上市后发生了召回,应当说明召回原因、过程和处理结果。(六)原医疗器械注册证中载明要求继续完成工作的,应当提供相关总结报告,并附相应资料。对照医疗器械注册管理办法及国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)。(一)核对企业是否跟踪记录了售后临床使用情况,是否收集了用户投诉,针对企业投诉是否采取了有效的措施。(二)核对企业是否跟踪了记录了产品上市后的情况,是否收集了上市后发生的可疑不良事件。是否对发生的不良事件进行分析,阐明原因,评价研究,对其安全性、有效性的影响是否予以说明,并采取有效的处理措施和方案。核对申报产品的不良事件内容是否真实完整,查询网址:广东省不良事件上报系统:http:/ (二)所提交资料真实性的自我保证声明。对照医疗器械注册管理办法及国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)。核对声明是否涵盖医疗器械监督管理条例(国务院令第650号)医疗器械注册管理办法(国家食品药品监督管理总局令第4号)、国家食品药品监督管理总局关于公布医疗器械注册申报资料要求和批准证明文件格式的公告(2014年第43号)、医疗器械技术要求编写指导原则、医疗器械说明书和标签管理规定;声明是否涵盖现行国家标准、行业标准,标准查询见6审查方法内容,并提供符合标准的清单。是否涵盖提交材料真实性声明。8其他如在原医疗器械注册证有效期内发生了涉及产品技术要求变更的,应当提交依据注册变更文件修改的产品技术要求一式两份。按照医疗器械技术要求编写指导原则1、核对格式是否符合医疗器械技术要求编写指导原则2、内容是否依据提交的注册变更文件修改。注:医疗器械相关标准目录见网址:http:/
《医疗器械延续技术审查量化表》由会员伟、分享,可在线阅读,更多相关《医疗器械延续技术审查量化表》请在金锄头文库上搜索。
 认识实习报告范文3000字
认识实习报告范文3000字
2023-06-15 29页
 2022年关于保育员年终工作总结模板汇总5篇
2022年关于保育员年终工作总结模板汇总5篇
2023-11-06 23页
 2023年出租房房屋租赁合同14篇
2023年出租房房屋租赁合同14篇
2023-08-18 62页
 保护眼睛的演讲稿合集6篇
保护眼睛的演讲稿合集6篇
2023-09-05 12页
 【计量标准】JJG 6692003 称重传感器 检定规程
【计量标准】JJG 6692003 称重传感器 检定规程
2022-11-14 81页
 关于羽毛球比赛作文400字集锦七篇
关于羽毛球比赛作文400字集锦七篇
2022-08-14 8页
 户型二次结构作业指导
户型二次结构作业指导
2023-10-12 7页
 《星星离我们有多远》读书心得范文5篇
《星星离我们有多远》读书心得范文5篇
2023-12-28 9页
 伤感让人流泪的说说(模板)
伤感让人流泪的说说(模板)
2023-10-05 15页
 2352710944中国青少年高尔夫球锦标赛冠名赞助招商方案中国冠名方案高尔夫球招商方案高尔夫比赛冠名赞助全国少年锦标赛高尔夫
2352710944中国青少年高尔夫球锦标赛冠名赞助招商方案中国冠名方案高尔夫球招商方案高尔夫比赛冠名赞助全国少年锦标赛高尔夫
2023-02-01 8页