
【化学】无机非金属材料-硅二氧化硅硅酸硅酸盐课件 2023-2024学年高一下学期人教版(2019)必修第二册
33页1、第五章化工生产中的重要非金属元素第三节无机非金属材料硅硅 二氧化硅二氧化硅 硅酸硅酸 硅酸盐硅酸盐想一想:它们用到哪些材料?列举生活中有哪些材料?材料按照化学组成和特性来分:复合材料:由两种或两种以上的材料按照一定方式组成的材料。高分子材料:纤维、橡胶、树脂、塑料材料金属材料:纯金属材料和合金材料无机非金属材料:传统和新型无机非金属材料三大传统硅酸盐材料:玻璃、陶瓷、水泥传统无机非金属材料-硅酸盐材料结构:在硅酸盐中,Si和O构成了硅氧四面体。性质:硬度大、熔点高、难溶于水、化学性质稳定等。硅酸盐概念:由硅、氧和金属组成的化合物的总称玻璃制备原理:SiO2+Na2CO3Na2SiO3+CO2SiO2+CaCO3CaSiO3+CO2纯碱、石灰石、石英沙(SiO2)Na2SiO3、CaSiO3和SiO2建筑材料、光学仪器、各种器皿、玻璃纤维原料:成分:用途:性能:透光性好、硬度大、无固定熔点水泥黏土和石灰石,适量石膏(调节水泥硬化速率)水泥回转窖(复杂的物理和化学变化)设备:原料:水泥、沙子和碎石等与水混合可以得到混凝土,大量用于建筑和水利工程用途:成分:硅酸盐,包括硅酸三钙(3CaOSi
2、O2)硅酸二钙 (2CaOSiO2)、铝酸三钙(3CaOAl2O3)小杨老师 15521324728版权归属于微信公众号:杨sir化学侵权必究环节2、知识精讲黏土(含水的铝硅酸盐)高温烧结(复杂的物理和化学变化)建筑材料、绝缘材料、日用器皿、卫生洁具原料:条件:用途:陶瓷我国具有悠久的陶瓷制造历史,在新石器时代,我们的祖先已能烧制我国具有悠久的陶瓷制造历史,在新石器时代,我们的祖先已能烧制陶器,至唐宋时期,我国的陶瓷制品已经享誉海内外。陶器,至唐宋时期,我国的陶瓷制品已经享誉海内外。玻璃,水泥,陶瓷的原料有哪些区别?组成成分上玻璃与水泥和陶瓷相比有什么不同?成分:含水的铝硅酸盐玻璃的成分含有二氧化硅1湖南省博物院被国家文物局列为首批“国家一级博物馆”,现有院藏文物18万余件。下列文物的主要成分为硅酸盐材料的是C2“九秋风露越窑开,夺得千峰翠色来”是赞誉越窑秘色青瓷的诗句,描绘我国古代精美的青瓷工艺品。玻璃、水泥和陶瓷均为硅酸盐制品,下列有关说法正确的是()A玻璃是人类最早使用的硅酸盐制品B制水泥的原料为纯碱、石灰石和石英C硅酸盐制品的性质稳定、熔点较高D沙子和黏土的主要成分均为硅酸盐C
3、硅谷最早是研究和生产以硅谷最早是研究和生产以硅硅为基础的为基础的半导体芯片半导体芯片的地方,因此得名。的地方,因此得名。新型无机非金属材料硅在地壳中的含量:地壳中含量前五位的元素氧、硅、铝、铁、钙仅次于氧,排在第二位。一.硅1.硅的存在:硅是亲氧元素,没有游离态,只有化合态。硅在自然界中主要以:硅酸盐(如地壳中的大多数矿物)和氧化物(如水晶、玛瑙)的形式存在。硅酸盐硅酸盐石榴石石榴石氧化物氧化物水晶水晶是构成矿物和岩石的基本元素。氧化物氧化物沙子沙子硅元素位于元素周期表第三周期、第A族。处于金属和非金属的过渡位置,导电能力介于导体和绝缘体之间,是良好的半导体材料1.硅硅是信息技术的关键材料。半导体材料Si+148 42+642C硅的化学性质不活泼,主要形成四价化合物单质硅是灰黑色具有金属光泽的固体,结构类似金刚石,熔沸点很高、硬度大2.硅的物理性质硅的类型:分为晶体硅和不定型硅晶体硅不定型硅正正四四面面体体形形网网状状结结构构的的晶晶体体,与金刚石结构相似与金刚石结构相似并并非非所所有有的的原原子子都都与与其其它它原原子子严严格格地地按按照照正正四四面面体体排排列列 (不不稳定性稳定性
4、)3.硅单质的化学性质(1)常温下,硅的化学性质不活泼,除氢氟酸、氟气、强碱外不跟其他物质反应。与氟气反应:Si+2F2=SiF4与氢氟酸反应:Si+4HF=SiF4+2H2与强碱溶液反应:Si+2NaOH+H2O=Na2SiO3+2H2(2)加热条件下,硅也能和一些非金属反应。Si+2Cl2 SiCl4Si+O2 SiO2Si+C SiC高温3.硅的用途良好的半导体材料可制成硅芯片和太阳能电池极板半导体发光二极管半导体发光二极管思考:如何理解工业上的“从沙滩到用户”?怎么获得高纯硅呢?SiO22C Si2CO4.高纯硅的制备其中涉及的主要化学反应为_制备原理:用焦炭还原石英砂,得到含少量杂质的粗硅,然后转化为三氯硅烷,再经氢气还原。能否能否通过该反应证明通过该反应证明C C、SiSi的的还还原原性性强弱?强弱?氧化性、还原性的强弱,必须是在通氧化性、还原性的强弱,必须是在通常的情况下发生的反应,上述反应是常的情况下发生的反应,上述反应是在高温条件下发生的,故不能比较还在高温条件下发生的,故不能比较还原性的强弱。原性的强弱。SiO2是硅的重要化合物,地球上存在的天然二氧化硅约占地壳质量
5、的12,其存在形态有结晶形和无定形两大类,通称硅石。二,二氧化硅玛瑙玛瑙水晶水晶石英石英结晶形无定形2.SiO2的结构空间构型:硅氧四面体(空间网状)物理性质:难溶于水,熔点高,硬度大 化学性质:化学稳定性好1mol SiO2中含4mol Si-O键SiO2是不是分子式,SiO2是由原子组成的,没有SiO2分子 二氧化硅中二氧化硅中氧原子与硅原子个数比为氧原子与硅原子个数比为2:1,用,用SiO2来表示二氧化硅的组成,表示来表示二氧化硅的组成,表示O与与Si的原子个数比,的原子个数比,不是分子式不是分子式是化学式是化学式 导入:导入:光导纤维被认为是光导纤维被认为是20世纪最伟大的发明之一,它使信息高速公路在世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展。光导纤维的主要成分是全球迅猛发展。光导纤维的主要成分是SiO2,碱性环境下,光导纤维为什么,碱性环境下,光导纤维为什么会失去传播信号的能力?会失去传播信号的能力?思考:SiO2具有酸性氧化物的通性,你能否说出CO2能与哪类物质发生反应?CO2能与水反应,与碱反应,与碱性氧化物反应,SiO2能与这些物质反应吗?a.酸性氧化物 与碱
《【化学】无机非金属材料-硅二氧化硅硅酸硅酸盐课件 2023-2024学年高一下学期人教版(2019)必修第二册》由会员s****6分享,可在线阅读,更多相关《【化学】无机非金属材料-硅二氧化硅硅酸硅酸盐课件 2023-2024学年高一下学期人教版(2019)必修第二册》请在金锄头文库上搜索。

【化学】原子结构 课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】元素周期律课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】元素周期表课件 2023-2024学年高一下鲁科版(2019)必修第二册

【化学】有机物分子中共面问题课件 2023-2024学年高二下学期化学鲁科版(2019)选择性必修3

【化学】烯烃炔烃的性质课件 2023-2024学年高二下学期化学鲁科版(2019)选择性必修3

【化学】微项目 课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】微项目 补铁剂中铁元素的检验——利用配合物进行物质检验课件 高二下鲁科版(2019)选择性必修2
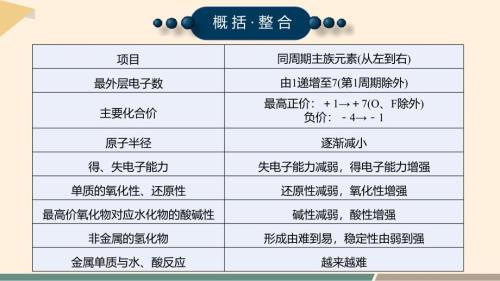
【化学】同主族元素的相似性和递变性课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】认识同周期元素性质的递变规律件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】醛和酮 糖类和核酸课件 2023-2024学年高二化学人教版(2019)选择性必修2
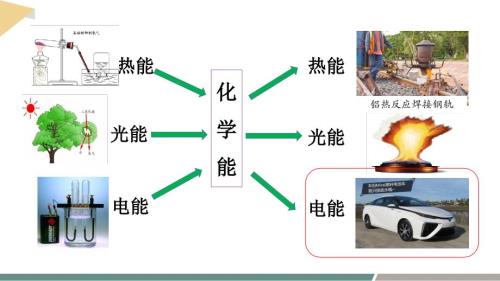
【化学】能量转化的应用——化学电池课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】化学键与物质构成课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】化学反应与能量转化 化学能与热能课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】化学反应的限度课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】化学反应的快慢课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【化学】分子间作用力课件 2023-2024学年高二下学期化学鲁科版(2019)选择性必修2

【化学】电极方程式书写课件 2023-2024学年高一下学期化学鲁科版(2019)必修第二册

【地理】服务业区位因素及其变化 教学设计2023-2024学年高中地理人教版(2019)必修二

【化学】盐化肥检测题-2023-2024学年九年级化学人教版下册

【化学】金属和金属材料测试题----2023-2024学年九年级化学人教版下册
 【课件】2024届高考政治二轮复习要点及策略 课件
【课件】2024届高考政治二轮复习要点及策略 课件
2024-05-22 149页
 【课件】2024届高三化学二轮复习 有机化学命题特点与复习策略报告课件
【课件】2024届高三化学二轮复习 有机化学命题特点与复习策略报告课件
2024-05-22 62页
 2024届高三英语一轮复习名词性从句课件
2024届高三英语一轮复习名词性从句课件
2024-05-22 61页
 定语从句课件-2024届高三英语二轮复习
定语从句课件-2024届高三英语二轮复习
2024-05-22 54页
 2024届高考现代文阅读Ⅰ考情分析及备考策略+课件
2024届高考现代文阅读Ⅰ考情分析及备考策略+课件
2024-05-22 55页
 2024年中考语文总复习:古诗文默写课件
2024年中考语文总复习:古诗文默写课件
2024-05-22 108页
 第5讲+古代希腊民主政治+课件--2024届高三人民版历史必修1一轮复习
第5讲+古代希腊民主政治+课件--2024届高三人民版历史必修1一轮复习
2024-05-22 57页
 第8讲美国联邦制的建立+课件--2024届高三人民版历史必修1一轮复习
第8讲美国联邦制的建立+课件--2024届高三人民版历史必修1一轮复习
2024-05-22 60页
 2024届高考地理一轮复习课件自然地理环境差异性高考真题
2024届高考地理一轮复习课件自然地理环境差异性高考真题
2024-05-22 55页
 +非谓语动词(三)课件-2024届高考英语一轮复习
+非谓语动词(三)课件-2024届高考英语一轮复习
2024-05-22 55页

