
化学平衡图像--基本图像(共8页)
8页1、精选优质文档-倾情为你奉上化学平衡图像专题解题思路:一看轴(纵、横坐标的意义),二看线(线的走向和变化趋势),三看点(起点、折点、交点、终点、零点的意义),四看要不要作辅助线(等温线、等压线、平衡线),五看量的变化(如浓度变化、温度变化等),六想规律(外界条件对反应速率的影响规律和化学平衡移动规律)1. 速率-时间图1. 对于达平衡的可逆反应XY WZ,增大压强则正、逆反应速度(v)的变化如上图,分析可知X,Y,Z,W的聚集状态可能是( )。(A)Z,W为气体,X,Y中之一为气体(B)Z,W中之一为气体,X,Y为非气体(C)X,Y,Z皆为气体,W为非气体(D)X,Y为气体,Z,W中之一为气体2. 在一定条件下,反应A(g)B(g)C(g)(正反应为放热反应)达到平衡后,根据下列图象判断 A B C D E(1)升温,达到新的平衡的是()(2)降压,达到新的平衡的是()(3)减少C的量,移向新平衡的是()(4)增加A的量,移向新平衡的是()(5)使用催化剂,达到平衡的是()2. 浓度(物质的量)-时间图3. 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如右图,下列表
2、述中正确的是( )A反应的化学方程式为:2 MNBt2时,正逆反应速率相等,达到平衡 Ct3时,正反应速率大于逆反应速率 D.t1时,N的是M浓度的2倍3. 含量-时间-温度(压强)图4. 可逆反应m A(s)n B(g) e C(g)f D(g),反应过程中,当其它条件不变时,C的百分含量(C)与温度(T)和压强(P)的关系如下图:下列叙述正确的是( )。(A)达平衡后,加入催化剂则C增大(B)达平衡后,若升温,平衡左移(C)化学方程式中n e+f(D)达平衡后,增加A的量有利于平衡向右移动5. 在密闭容器中进行下列反应:M(g)N(g) R(g)2L此反应符合下面图像,下列叙述是正确的是( )(A) 正反应吸热,L是气体(B) 正反应吸热,L是固体(C) 正反应放热,L是气体(D) 正反应放热,L是固体或液体6. 可逆反应m A(s) + n B(g) p C(g) + q D(g)反应过程中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如图(T2T1),根据图中曲线分析,判断下列叙述中正确的是( )(A)到达平衡后,若使用催化剂,C的质量分数增大(B)平衡后,若升
3、高温度,平衡则向逆反应方向移动(C)平衡后,增大A的量,有利于平衡向正反应方向移动(D)化学方程式中一定np+q8. 在容积固定的密闭容器中存在如下反应:A(g)3B(g)2 C(g)(正反应放热),某研究小组研究了其它条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出右边关系图。下列判断一定错误的是( )A、图研究的是不同催化剂对反应的影响且乙使用的催化剂效率较高。B、图研究的是压强对反应的影响,且甲的压强较高。C、图研究的是温度对反应的影响,且甲的温度较高。D、图研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高。4. 恒压(温)线9. 如上图所示,反应:X(气)+3Y(气) 2Z(气)(正反应为放热反应),在不同温度、不同压强(p1p2)下,达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )10. 反应aA(g)+bB(g) cC(g),生成物C的质量分数与压强P和温度的关系如图,方程式中的系数和Q值符合图象的是( )(A)a+bc 正反应为放热反应 (B)a+bc 正反应为吸热反应(C)a+bc 正反应为吸热反应 (D)a+b=c 正反应为放热反应11
4、. 某可逆反应L(s)+G(g)3R(g) (正反应为吸热反应),本图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示( )(A)平衡混合气中R的质量分数(B)达到平衡时G的转化率(C)平衡混合气中G的质量分数(D)达到平衡时L的转化率12. 图中表示外界条件(T、P)的变化对下列反应的影响:L(s)G(g) 2R(g)(正反应为吸热反应),y 轴表示的是( )(A) 平衡时,混合气中R的百分含量(B) 平衡时,混合气中G的百分含量(C) G的转化率(D) L的转化率13.A为气态反应物在平衡体系中的百分含量,符合曲线的反应是( )(A)N2(g)3H2(g)2NH3(g)(正反应放热) (B)C(s)CO2(g) 2CO(g)(正反应吸热) (C)N2(g)O2(g) 2NO(g)(正反应吸热) (D) CaCO3(s) CaO(s)CO2(g)(正反应为吸热)14. 在可逆反应mA(g)+nB(g) pC(g) (正反应为放热反应)中m、n、p为系数,且m + np。分析下列各图,在平衡体系中A的质量分数与温度toC、压强P关系正确的是( )15. 能正确反映出
《化学平衡图像--基本图像(共8页)》由会员M****1分享,可在线阅读,更多相关《化学平衡图像--基本图像(共8页)》请在金锄头文库上搜索。

2022年小学数学一年级上册教案-分类

广州版英语四年级下册单词表

公司年会主持词模板锦集6篇

客户回访具体实施方案及流程

我的特长是卖花生

2022中学教师教学工作总结

教师节征文活动方案

六年级数学统计与概率练习题

湖南通信磁性元器件项目可行性研究报告

壶口壶口阅读答案
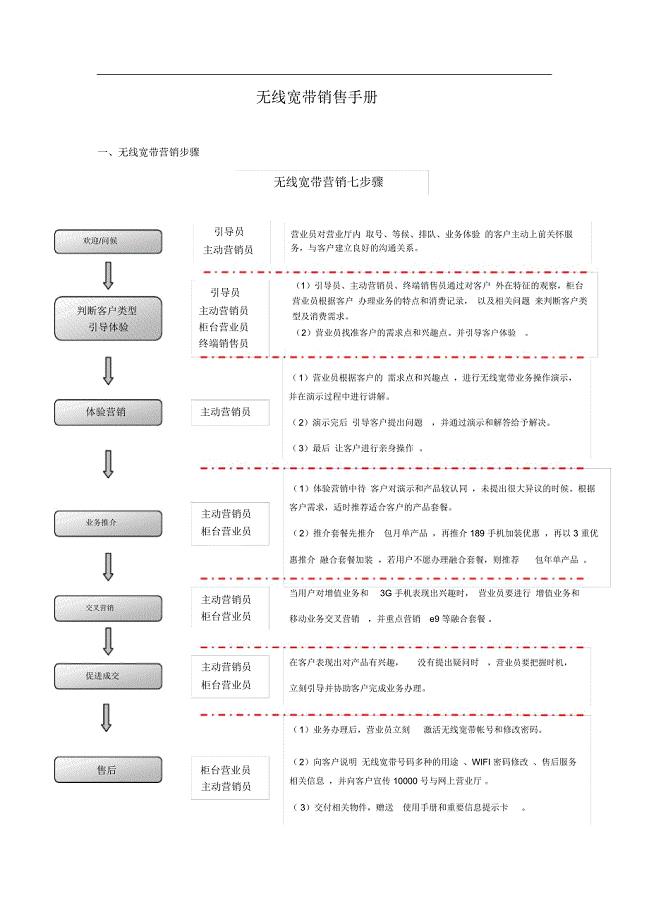
无线宽带销售手册(简版end)终稿

职称英语 卫生类 B级 完形填空 考试押题 小抄版【必考】

信息系统监理师16

公司员工试用期工作总结参考版(3篇).doc

文通中学度八年级语文上册期末试题及答案

精选暑假日记小学日记集锦7篇

2023年依法治校实施方案
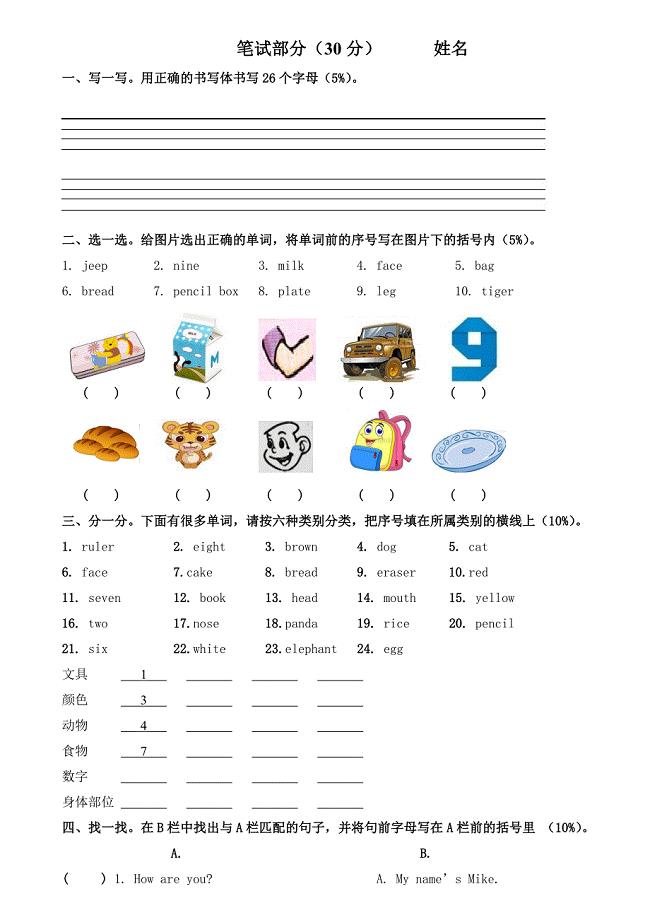
三年级上英语1
![[人教版]小学一年级上数学期末测试题](https://union.152files.goldhoe.com/2023-12/16/69b811fd-32b9-44d2-834a-4338381e4b2a/pic1.jpg)
[人教版]小学一年级上数学期末测试题

技术管理工作规划
 优质课-22.2平行四边形判定2教学设计(共7页)
优质课-22.2平行四边形判定2教学设计(共7页)
2023-02-24 8页
 水电站大作业(共18页)
水电站大作业(共18页)
2023-10-17 18页
 优秀路政员先进事迹材料
优秀路政员先进事迹材料
2024-01-23 13页
 某制药企业清洁生产审核报告(共85页)
某制药企业清洁生产审核报告(共85页)
2023-07-12 87页
 心肺复苏考试题及答案(DOC 3页)
心肺复苏考试题及答案(DOC 3页)
2023-06-17 5页
 人教版一年级道德与法治下册教学设计(共30页)
人教版一年级道德与法治下册教学设计(共30页)
2023-04-14 31页
 党校学习后写的党性分析材料范例
党校学习后写的党性分析材料范例
2023-09-27 18页
 人教版三年级上册数学期末试卷期末试卷及答案5套
人教版三年级上册数学期末试卷期末试卷及答案5套
2023-11-06 30页
 小米公司CIS设计(共5页)
小米公司CIS设计(共5页)
2023-05-04 6页
 高三生物第一轮复习---必修二--第三章《基因的本质》单元测试卷-Hooker(共5页)
高三生物第一轮复习---必修二--第三章《基因的本质》单元测试卷-Hooker(共5页)
2023-01-24 3页

