
cmde动物源性医疗器械产品注册申报资料相关技术要求(zsda美化)
49页1、动物源性医疗器械产品注册申,报资料相关技术要求,国家食品药品监督管理局医疗器械技术审评中心,审评二处,赵鹏,SFDACMDE, ,来源于脊椎动物: 胶原止血/填充材料、生物敷料、羊肠缝线、生物瓣膜 、生物补片、骨填充材料、硫酸软骨素、透明质酸钠、含 羊毛脂的医疗器械、带肝素涂层的医疗器械等; 本身不属于器械但与动物源有关的:酶、抗体、培养 基等。 来源于非脊椎动物:,壳聚糖(虾、蟹等)、骨蜡(蜜蜂)、蚕丝。 动物源性医疗器械产品举例 SFDACMDE, ,动物源性医疗器械产品注册申报资料指导原则 范围, 全部或部分采用无生命动物组织制成的或取材于动物组 织的医疗器械产品(体外诊断用医疗器械除外)。 采用动物组织衍生物或由动物体自然获取物质(例如: 牛奶、羊毛等)制成的医疗器械产品。 生产过程中使用或接触了动物源性材料的医疗器械。 动物源性医疗器械产品 SFDACMDE, ,动物:任何脊椎或无脊椎动物包括两栖动物、节肢动物 (如甲壳纲动物)、鸟、珊瑚、鱼、爬行动物、软体动物 和哺乳动物,不包括人(智人)。 衍生物:通过制造工艺从动物材料中获得的物质。,术语 SFDACMDE, ,病毒感染
2、风险 动物源材料的来源控制 病毒灭活工艺及有效性验证 终产品的残留病毒标准及检测(未强制) 免疫原性风险, 免疫原性降低工艺 终产品的免疫原性相关指标控制标准及检测 动物源性医疗器械的主要风险控制措施 SFDACMDE,病毒灭活,终产品检测,来源控制,病毒 动物源材料,病毒 动物源材料,病毒感染风险涉及的方面 病毒 感 染,病毒 动物源材料,生产工艺A,病毒感染风险 SFDACMDE,病毒感染风险涉及的方面,病毒 动物源材料 终产品检测,病毒 动物源材料 来源控制,生产工艺B 病毒灭活?,病毒感染风险 SFDACMDE,对于感染病毒和传染性病原体的风险控制需至少从,源头控制和病毒灭活两方面着手,仅依靠源头控制 或仅依靠病毒灭活都无法确保风险降至最低。 病毒感染风险 SFDACMDE,病毒灭活,终产品检测,来源控制,病毒 动物源材料,病毒 动物源材料,病毒感染风险涉及的方面 病毒 感 染,病毒 动物源材料,生产工艺A,病毒感染风险 SFDACMDE,病毒灭活,终产品检测,来源控制?,病毒 动物源材料,病毒 动物源材料,病毒感染风险涉及的方面 病毒 感,染,病毒 动物源材料,生产工艺A,病
3、毒感染风险 SFDACMDE,动物源材料的来源控制, 种群来源 饲养(场地、饲料、免疫、防疫) 屠宰 取材(部位、组织性质、取材方式) 处理 储存运输 可追溯性 病毒感染风险 SFDACMDE,种群来源控制方面, 动物种类 动物的地理来源 动物年龄 取材部位 取材部位的组织性质 病毒感染风险 SFDACMDE,所用牛、羊源性材料应符合国食药监械2006407号关于含有牛、羊,源性材料医疗器械注册有关事宜的公告 发生下列情况之一的不予受理: 1. 牛/羊来自疫区 2. 牛/羊来自非疫区,但医疗器械的实际生产场所为疫区 1)牛/羊与疫区牛/羊一起圈养 2)牛/羊喂养动物蛋白质饲料 注:疫区的范围以质检总局网站为准 牛、羊源性材料的源头控制 SFDACMDE, ,为确保风险的可控性,企业需建立起一套追溯体系, 以便在发现不良事件时能够及时查出原因并采取措施 以防止类似不良事件的发生。 定点饲养、定点采购、定点屠杀,以及根据国家相关,规定进行动物防疫、检疫,都是降低病毒和传染性病 原体传播风险的必要手段。 动物源材料的来源控制 SFDACMDE,病毒灭活方法(举例) 钴60辐照法, 干热法 巴
4、氏消毒法 有机溶剂/去污剂(S/D)处理法 酸处理、碱处理 强氧化剂、强还原剂处理, 高温闪灭,等 注意:以上方法均需验证试验或提供相关研究资料。 病毒灭活工艺有效性验证 SFDACMDE,注意:生产企业需充分评 估其对产品的不利影响, 以保证产品最终能够安全 有效地使用。,动物源材料,动物源材料,指示病毒 106/mL,动物源材料,指示 病毒,病毒灭活工艺有效性验证 指示病毒 106/mL 病毒灭活,工艺,Log(初始病毒数量),Log(灭活后病毒数量),病毒灭活工艺有效性验证 SFDACMDE,指示病毒的选择, 需要选择与生产过程中采用的原材料可能含有病毒种类的 相关病毒,不能用相关病毒的,要选择与其理化性质尽可 能相似的指示病毒; 所选择的病毒理化性质需有代表性(病毒大小、核酸类型 以及有无包膜),其中至少需包括一种对物理和/或化学处 理有明显抗性的病毒; 指示病毒滴度需要尽可能高(病毒滴度一般需106/mL) 。 病毒灭活工艺有效性验证 SFDACMDE,至少四种:,RNA 有包膜, ,DNA 有包膜 RNA 无包膜 DNA 无包膜,同时满足:, ,大小: 直径 20200nm
《cmde动物源性医疗器械产品注册申报资料相关技术要求(zsda美化)》由会员suns****4568分享,可在线阅读,更多相关《cmde动物源性医疗器械产品注册申报资料相关技术要求(zsda美化)》请在金锄头文库上搜索。

土地管理与地籍测量---第八章界址点测量
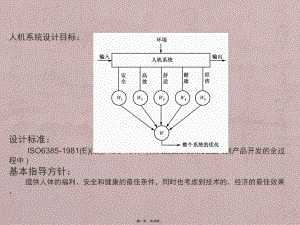
人机工程学案例分析(2)

工程安全培训_201303

第9章房地产投资决策分析

第2章房地产经纪制度

ACM程序设计-东北林业大学acm05

《亲爱的汉修先生》读书交流会

中原_深圳新世界尖岗山项目市场汇报_40P_2012年_别墅_项目分析_量价走势

五年级数学质量分析演示文稿

人工智能小镇-智慧小镇建设20180525

景观基本知识及发展历程

建设工程信息管理(2)

机电驱动技术第二章步进驱动技术
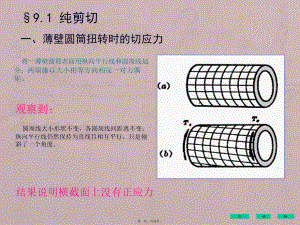
工程力学-第9章圆轴扭转时的应力变形分析与强度刚度设计

第一章第二节幼儿园文化环境建设的原则

第一章检测技术的基础知识

第一章__现代表面工程技术

第六章钢结构工程

第9节项目试运行管理

班主任工作经验交流课件(4)
 大班韵律 忐忑 课件
大班韵律 忐忑 课件
2023-11-14 7页
 人教版六年级下册数学课件四、2比例的基本性质
人教版六年级下册数学课件四、2比例的基本性质
2023-02-28 15页
 Linux第三章
Linux第三章
2023-02-20 60页
 ch7振幅调制与解调
ch7振幅调制与解调
2023-02-20 52页
 部编版语文三年级下册训练题之修改符号修改病句
部编版语文三年级下册训练题之修改符号修改病句
2023-01-31 8页
 部编版小学语文六年级上册《只有一个地球》说课稿课件
部编版小学语文六年级上册《只有一个地球》说课稿课件
2022-12-27 23页
 经验分享工作培训动态PPT模板
经验分享工作培训动态PPT模板
2022-11-29 36页
 管理培训课件:龟兔赛跑解析
管理培训课件:龟兔赛跑解析
2022-11-28 41页
 企业复工与新冠病毒防护攻略(详细)
企业复工与新冠病毒防护攻略(详细)
2022-11-16 26页
 建筑施工大型设备设施安全管理
建筑施工大型设备设施安全管理
2022-11-09 71页

