
高中化学课时跟踪检测十五钠的重要化合物新人教版必修1
10页1、课时跟踪检测(十五)钠的重要化合物A级基础全面练1 . NaO和N&Q在下列哪一点性质上是相似的 ()A.颜色B.水溶液的酸碱性C.氧化性D.漂白性解析:选B NaO是白色固体,一般认为它无氧化性;N*Q是淡黄色固体,有强氧化性和漂白性;二者溶于水都生成NaOH2 .小明同学用洁净的钳丝蘸取某无色溶液,在无色火焰上灼烧,火焰呈黄色,通过该实验现象,下列四位同学对该溶液中存在的金属离子的判断正确的是()只有Na可能有Na, 也可能有K解析:选D钠的焰色是黄色,K的焰色是紫色,观察 K的焰色时需要透过蓝色钻玻璃,以滤去黄色光的干扰,该实验中没有透过蓝色钻玻璃观察,说明一定含有Na+,不能确定是否含有Ko3 .下列关于 NaO和N&Q的叙述正确的是()A.都是白色固体B.都是碱性氧化物C.都能和水反应形成强碱溶液D.都是强氧化剂解析:选C虽然两种氧化物的组成元素相同,但其结构、性质上的差异很大。NaO是白色粉末,NkQ是淡黄色粉末。NkO是碱性氧化物,NmQ是过氧化物。它们都能和水反应形成 氢氧化钠溶液。N&O中氧元素价态为最低价(2价),无氧化性,NaQ中氧元素价态为中间价 (1价),具有
2、氧化性、还原性,是强氧化剂。4.可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是()A.加热时无气体放出B.滴加盐酸时有气泡放出C.溶于水后滴加稀 BaCl2溶液有白色沉淀生成D.溶于水后滴加澄清石灰水有白色沉淀生成解析:选C Na2CO和NaHC0tl澄清石灰水反应, 两者都会产生白色沉淀,因此不能鉴别;而滴加BaCl2溶液,现象不同,有 NaCO时产生BaCOM淀。5 .飞船内安装盛有 N*Q的装置,它的用途是产生氧气。下列关于NaO的叙述正确的是()A. NaQ中阴、阳离子的个数比为1 : 1B. NaQ分别与水及CO反应产生相同量的 Q时,需要水和 CO的质量相等C. NaQ分别与水及CO反应产生相同量的 Q时,转移电子的物质的量相等D. N&Q属于碱性氧化物解析:选C A项,NaQ中阴、阳离子的个数比为 1 : 2,错误;B项,NaQ分别与水及 CO反应产生相同量的 Q时,需要水和CO的物质的量相等,但质量不相等,错误; C项,NS2C2 分别与水及CO反应产生相同量的 Q时,转移电子的物质的量相等,正确;D项,NS2Q不属于碱性氧化物,错误。6 .下列说法不正确的是()A.用
3、加热法可除去 NaCO中的NaHCOB. NaCO的热稳定性大于 NaHCOC.可用石灰水区分 NaCO与NaHCOB液D. NaCO和NaHCO勺水溶液均显碱性解析:选C A项,碳酸氢钠受热分解生成碳酸钠、水和CO,所以用加热法可除去 NaCO中的NaHCO,正确;B项,N&CO的热稳定性大于 NaHCO正确;C项,氢氧化钙与碳酸钠、 碳酸氢钠溶液均反应生成白色沉淀碳酸钙,因此不能用石灰水区分NaCO与NaHCO溶液,错误;D项,NaCO、NaHCO勺水溶液均显碱性,正确。7 .下列关于Na。N&Q的比较,正确的是()A. NaQ、NkO都是钠的氧化物,都是碱性氧化物B. NaQ、NkO都是可溶于水(或能与水反应)的白色固体C. NS2O2在和CO的反应中,既是氧化剂,又是还原剂D. NaQ与水反应时,1 mol Na 2O2转移2 mol电子解析:选C A项,N*Q与水反应除了生成 NaOH7卜,还有 Q生成,所以NaO2只是钠的氧 化物,但不是碱性氧化物; B项,Na2Q是淡黄色固体;C项,NaQ与CO反应时电子转移关系: 失去2 X eI12N5+2C52Na2CO3+O2,得
4、到2乂厂变成了一 2价的O和零价的O,正确;D项,NaO2与H2O反应时,NaO中一1价白O O变成了一 2价的O和零价的0,故1 mol Na 2Q转移 1 mol电子,错误。8 .纯碱和小苏打都是白色晶体,在日常生活中都可以找到。若要在家中将它们区分开来,卜面的方法中可行的是()A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀D.分别放在炒锅中加热,观察是否有残留物解析:选A A项,碳酸钠与酸反应首先产生碳酸氢钠和氯化钠,然后是碳酸氢钠与酸反 应产生碳酸钠、二氧化碳和水,而碳酸氢钠中加入酸立即放出气体,所以根据反应放出气体 的快慢可区分碳酸钠和碳酸氢钠,正确;B项,纯碱和小苏打都是钠盐,焰色反应火焰都为黄色,不能区别二者,错误; C项,二者都能与氢氧化钙溶液发生反应产生碳酸钙白色沉淀,不 能区别它们,错误;D项,碳酸钠稳定,受热不易分解,碳酸氢钠不稳定受热分解产生碳酸钠、 二氧化碳和水,也有固体残留物,所以不能区分二者,错误。9 .除去下列物质中
《高中化学课时跟踪检测十五钠的重要化合物新人教版必修1》由会员cl****1分享,可在线阅读,更多相关《高中化学课时跟踪检测十五钠的重要化合物新人教版必修1》请在金锄头文库上搜索。

建筑工地卫生管理制度
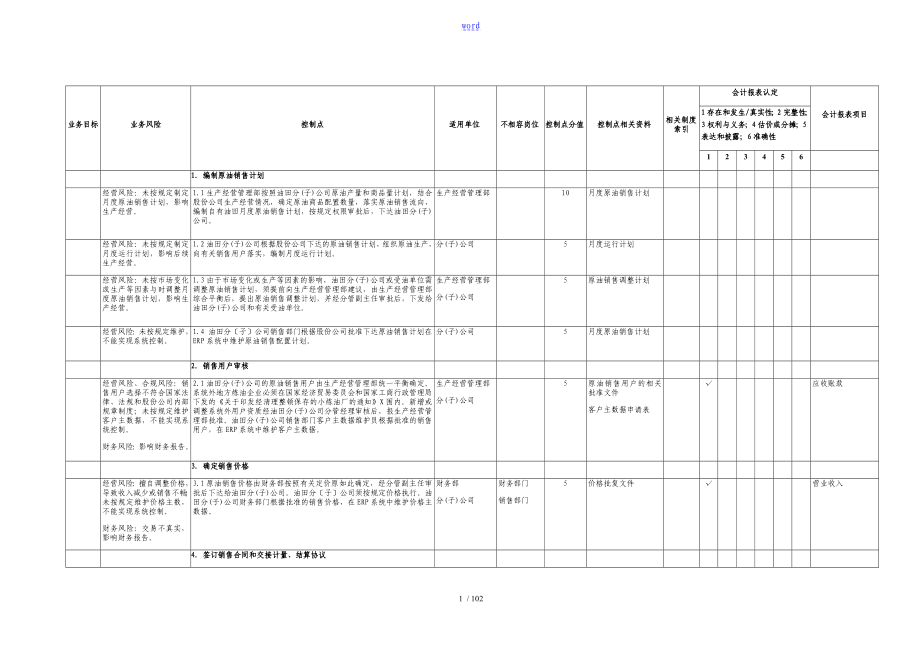
中石化全套内部控制系统规章制度销售管理系统体系文件资料

2023年甘肃省张掖市甘州区大满镇社区工作人员考试模拟试题及答案
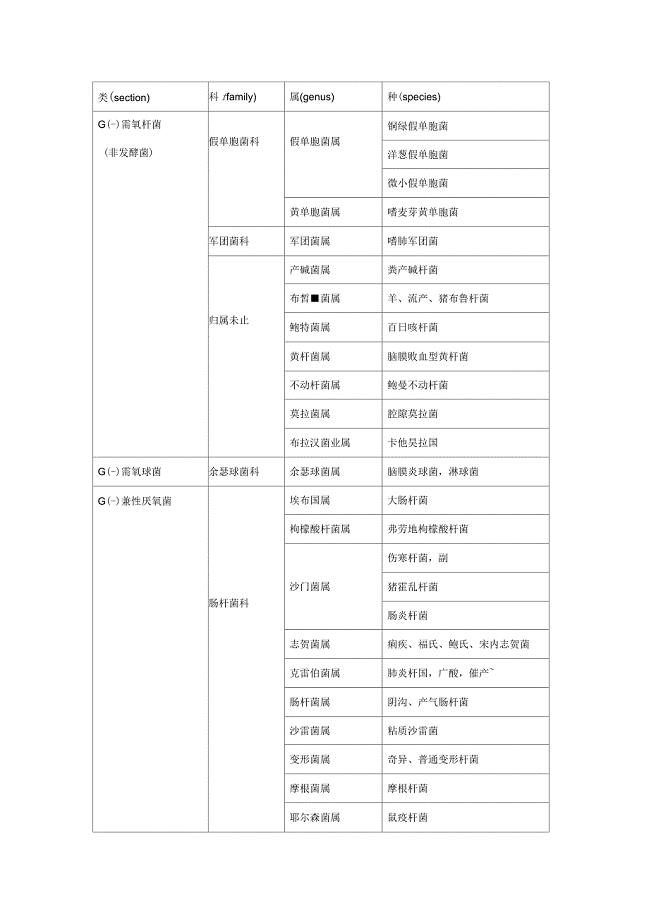
常见致病菌的分类

2022年12月试用期满转正工作总结

八年级语文下册 阅读理解《生命的选择》

企业战略世界最具竞争力企业的经营绝招

如何让客户说竞品的坏话

四人合伙协议书模板

《交通管理与控制》思考题与习题

民办幼儿园年检情况通报

【可编辑】2022年寒假社会实践日记4篇

2012高考英语作文巧应对

中高层管理者继任计划方案

初中九年级数学下册《何时获得最大利润》

代理记账业务规范

地理教师工作计划教学(13篇)

专家讲课劳务合同

总结2020展望2021话题作文600字五篇材料

2022年金属非金属矿井通风资格证书考试内容及模拟题带答案点睛卷29
 摆闸翼闸使用说明书
摆闸翼闸使用说明书
2024-01-05 22页
 二年级下学期班主任计划
二年级下学期班主任计划
2023-08-05 7页
 插花艺术试卷B代答案
插花艺术试卷B代答案
2023-10-06 7页
 电大会计本科学位英语复习资料0804
电大会计本科学位英语复习资料0804
2022-10-07 37页
 常用装饰材料用量计算
常用装饰材料用量计算
2023-07-28 4页
 材料工程基础答案
材料工程基础答案
2022-12-04 17页
 上学期美术学院学生会学习部工作总结范文
上学期美术学院学生会学习部工作总结范文
2023-07-01 3页
 办公楼幕墙装饰工程施工部署
办公楼幕墙装饰工程施工部署
2022-11-12 6页
 人力资源管理相关人物调查问卷访谈录
人力资源管理相关人物调查问卷访谈录
2022-08-17 40页
 银行中英文术语及解释
银行中英文术语及解释
2023-09-09 5页

