
高一化学第一章知识导航与能力提升
43页1、,高一第一章 知识导航与能力提升 物质提纯与物质的量,书写化学式(基本化学术语) 学好化学的基础,硫酸铁、硫酸铝、磷酸铵、磷酸钙、磷酸氢二铵、二氧化硅、亚硫酸钠、硫酸亚铁、碱式碳酸镁、醋酸、乙醇、尿素,必备知识,书写化学式,纯碱、小苏打、磷酸钙、磷酸二氢钙、氧化铁、亚硝酸钠、氯酸铵、氨、硫化氢、丙氨酸、葡萄糖、葡萄糖酸锌、羟基磷酸钙,葡萄糖C6H12O6=CH2(OH)CH(OH)4CHO 葡萄糖酸C6H12O7=CH2(OH)CH(OH)4COOH 葡萄糖酸根CH2(OH)CH(OH)4COO CH2(OH)CH(OH)4COO2Zn (C6H11O7)2Zn 羟基磷酸钙Ca10(OH)2(PO4)6 Ca(OH)23Ca3(PO4)2,黄山巨人教育 胡征善 二0一九年九月,物质分离提纯、检验,物质(混) 分离、提纯 物质(纯) 自然界 人工,溶解过滤、结晶(蒸发、冷却)、萃取(提取)、分液、蒸馏、加热(升华、分解)、洗气、渗析、电解精炼、盐析,检验,过滤:分离对象?要固体还是要液体? 洗涤、干燥 仍是混合物 一般不不蒸发至干 蒸发,Cl、Br、I、 CO32、SO42、Al3+、F
2、e3+、Na+、K+,过滤,一、热过滤 将短颈玻璃漏斗放置于铜制的热漏斗内,热漏斗内装有热水以维持溶液的温度。内部的玻璃漏斗的颈部要尽量短些,以免过滤时溶液在漏斗颈内停留过久,散热降温,析出晶体使装置堵塞。,知识延伸,二、减压过滤,抽 气 机,结晶,结晶蒸发结晶、冷却结晶、重结晶 加热蒸发溶剂:要求溶质受热不反应 冷却结晶:溶质随温度变化S变化要求要大 重结晶 固体混合物(杂质或被提纯的物质)在某溶剂中随温度变化一种变化很大,一种变化不大(溶解度差别大) 包含热过滤和冷过滤2个过程,分离在不同且互不相溶的液体溶剂中溶解度不同的混合物,萃取剂的选择要求,检查上口瓶塞 关闭活塞,向分液漏斗中注入少量水,塞好瓶塞,用手心托住瓶塞,另一只手握住活塞部位,把分液漏斗倒立过来,观察瓶塞处是否渗水,如不渗水,将分液漏斗正立后并将瓶塞旋转180塞紧,重复上述操作,如不渗水,证明瓶塞部位不漏水 检查活塞部位同上,如何检查是否漏液?,提取(固-液萃取),中草药有效成分的提取、油料中“油”的提取 拯救了数百万生命、中国首位自然科学(生理学或医学奖)诺奖获得者屠呦呦(2015年) 用乙醚从青蒿中提取青蒿素 温
3、度高破坏了青蒿素。乙 醚沸点34,提取青蒿素 后34是蒸馏分离出青蒿 素,其药性没有被破坏。,核心素养,东晋葛洪肘后备急方记述“青蒿一握,以水二升渍,绞取汁,尽服之”,分离沸点差较大(一般要求沸点差30)的液体混合物或固液混合物得到纯净的液体,吸收部分,加热部分,分馏柱,关键能力,1、气体的净化洗气,洗什么?装置?吸收剂的选 择?连接次序? H2或CO2中混有HCl、H2O,除O2、CO、H2等,化学上常用的物理量 物质的量,物质的量是国际单位制中7个基本物理量之一,是专用计量微观粒子的物理量。 最新定义 1 mol为精确包含6.022140761023个原子或分子等基本单元的系统的物质的量,符号为n 表示某粒子物质的量时,用化学式指明粒子,物质的量,外文名 amount of substance 中文名建议参考台湾的名称“物量” 进行修改 若是用“物量” 名称,就有: 物量质量M,物量浓度c(B), 气体物量体积Vm,偏物量焓 物量消光(吸光)系数、物量吸收系数 这样就用“物理量”而不用单位“摩尔”了,2019年5月20日起正式生效,2019年5月20日起正式生效,2019年5月20
4、日起正式生效 不再用“0.012 kg12C中的12C原子数 ”,化学计量数之比:,x=6.021023时:阿伏加德罗常数NA,单位mol1 ,近似值取此值,2 6.02 1023 1 6.02 1023 2 6.02 1023,物质的量之比:,2 mol 1 mol 2 mol,分子数之比: 2 1 2 2x x 2x(x1的整数),1 mol,微粒数之比=物质的量之比:N1/N2=n1/n2,:,:,:,:,:,:,:,:,严格地说: 阿伏加德罗常量,关键能力,常用符号 物质的量:n 物质的质量:m 摩尔质量:M 粒子数:N 阿伏伽德罗常数:NA 相对原子质量:Ar 相对分子质量:Mr 质量分数: 气体的体积分数: 气体摩尔体积:Vm 在0、101千帕Vm=22.4L/mol 物质的量浓度:c(B),1.物质的量(n)、物质的质量(m)之间的关系: 物质的量n(mol)= m g/M gmol1 摩尔质量:单位物质的量的物质的质量 常用单位为M gmol1 M (gmol1) = m g/n mol M (gmol1) = m gn mol1,2.物质的量(n)、粒子数(N)之间的
《高一化学第一章知识导航与能力提升》由会员hz****0分享,可在线阅读,更多相关《高一化学第一章知识导航与能力提升》请在金锄头文库上搜索。
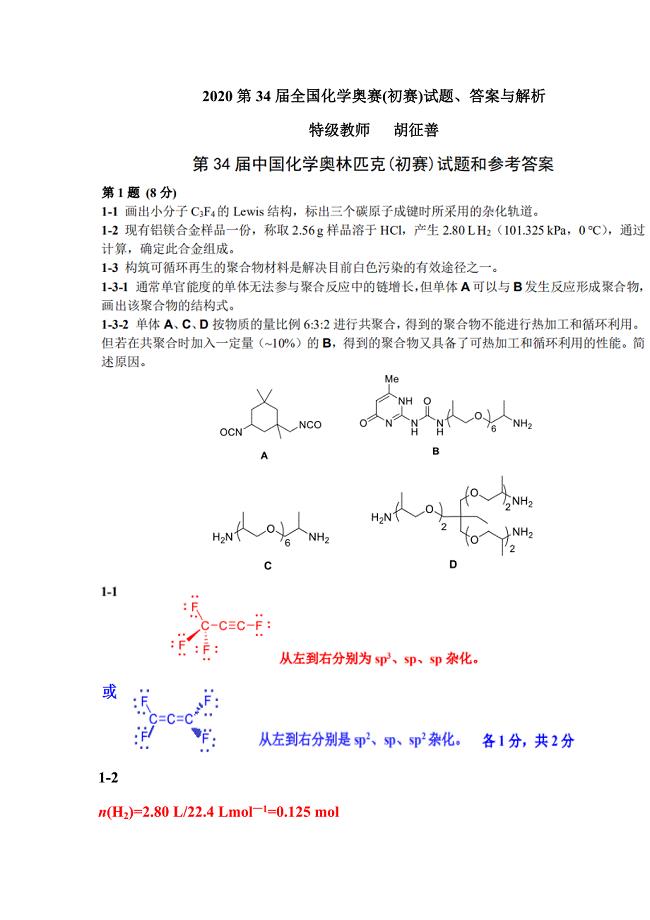
2020第34届全国化学奥赛(初赛)试题、答案与解析

高考《晶体结构》:内容向纵深突进

但愿高考命题更上一层楼1

精选科技成果切入命题 落实“四层四翼”评价要求

第33届中国化学奥林匹克(初赛)试题答案与详解

2019命题特色 2020备考策略

灿烂中华化学史 人类文明世界殊

高考:高中与高校 学习:态度与方法

高一化学第一章知识导航与能力提升

化学竞赛、高校自主招生考试——电化学专题

重视基础 推陈出新 彰显主旨 考查素养——2018年高考化学题赏析

特级教师文库 • 酸性与酸度

特级教师文库 •学习2017年版普通高中化学课标课程的体会

特级教师文库•2019年高考命题预测:我国古代科技在化学上的贡献

特级教师文库•化学学科高考预测:2019年的命题趋势

特级教师文库•高考化学学科:从2018看2019年的命题趋势

特级教师文库•磷和碳究竟谁的非金属性强?

特级教师文库•铁与空气作用生成什么氧化物?

特级教师文库•浓硫酸不能干燥气态烯烃

远逝的记忆
 【专业成长】做一名幸福、快乐、有成就的班主任(29张PPT)课件
【专业成长】做一名幸福、快乐、有成就的班主任(29张PPT)课件
2024-04-27 29页
 【高中语文】《望海潮》课件+统编版+高中语文选择性必修下册
【高中语文】《望海潮》课件+统编版+高中语文选择性必修下册
2024-04-27 47页
 【高中语文】《烛之武退秦师》课件+统编版+高中语文必修下册
【高中语文】《烛之武退秦师》课件+统编版+高中语文必修下册
2024-04-27 42页
 【高中语文】小说阅读+心理描写(课件)+备战高考语文+专题复习(新高考卷区通用)
【高中语文】小说阅读+心理描写(课件)+备战高考语文+专题复习(新高考卷区通用)
2024-04-27 45页
 【高中语文】《烛之武退秦师》公开课第二课时课件+统编版高中语文必修下册
【高中语文】《烛之武退秦师》公开课第二课时课件+统编版高中语文必修下册
2024-04-27 19页
 【高中语文】《说“木叶”》课件+统编版+高中语文必修下册
【高中语文】《说“木叶”》课件+统编版+高中语文必修下册
2024-04-27 37页
 【高中语文】《庖丁解牛》课件+统编版+高中语文必修下册 (1)
【高中语文】《庖丁解牛》课件+统编版+高中语文必修下册 (1)
2024-04-27 40页
 【高中语文】《庖丁解牛》课件+统编版++高中语文必修下册
【高中语文】《庖丁解牛》课件+统编版++高中语文必修下册
2024-04-27 36页
 【高中语文】《拿来主义》课件+统编版高中语文必修下册
【高中语文】《拿来主义》课件+统编版高中语文必修下册
2024-04-27 20页
 【高中语文】《庖丁解牛》课件+统编版+高中语文必修下册
【高中语文】《庖丁解牛》课件+统编版+高中语文必修下册
2024-04-27 38页

