
中考化学第一轮复习考点分析:物质的构成
6页1、物质的构成 一、基本考点考点1原子的构成原子原子核核外电子:每个电子带一个单位的负电荷质子:每个质子带一个单位的正电荷中子:不显电性(1)原子结构。不同种类的原子,核内的质子数不同,核外的电子数也不同。在原子中,核电荷数=质子数=核外电子数。原子核内的质子数不一定等于中子数,由于原子核所带电量和核外电子所带电量相等,且电性相反,因此,整个原子呈电中性。并不是所有原子的原子核都是由质子和中子两种微粒构成的,在所有原子中,普通氢原子的原子核内只有质子,没有中子。(2)相对原子质量:相对原子质量的定义:以碳12(含有6个质子和6个中子的碳原子)原子质量的作为标准,其他原子的质量与它相比较所得的比,就是该种原子的相对原子质量。计算公式:相对原子质量的符号为Ar,相对原子质量(Ar)=;相对原子质量质子数+中子数。注意问题:a相对原子质量是个比值,单位为“1”(通常省略不写),它不表示原子的实际质量。b由于质子和中子的质量近似相等,都约为一个电子质量的1836倍,故电子的质量可以忽略不计,原子的质量主要集中在原子核上。c原子的实际质量与相对原子质量成正比。相对原子质量与原子的质量的比较(见表4-
2、10-1):表4-10-1原子质量相对原子质量来源测定出来的比较出来的性质绝对的相对的数值非常小1,大多数为整数单位kg单位是1以碳12为例1.99310-26kg12联系相对原子质量=原子的质量一个碳12原子质量的1/12(原子的质量越大,其相对原子质量也越大)考点2元素与元素符号(1)元素:定义:具有相同核电荷数(即核内质子数)的一类原子的总称。性质:a. 元素是个宏观概念,它只能组成物质而不能构成分子或原子;b. 元素只讲种类不讲个数;c. 化学变化中,元素的种类和质量保持不变。分类:元素可分为金属元素、非金属元素和稀有气体元素三大类。含量:a. 在地壳中,氧元素最多,其次为硅、铝、铁等元素;b. 在空气中,氮元素最多,其次是氧元素;c. 在生物体中,氧元素最多,其次是碳元素和氢元素。决定:质子数决定了元素的种类,不同元素的区别是因为它们的质子数不相同。(2)元素与原子的区别(见表4-10-2);表4-10-2项 目元 素原 子定义具有相同核电荷数(即核内质子数)的一类原子的总称化学变化中的最小粒子区别含义宏观概念,只表示种类不表示个数微观概念,既表示种类又表示个数使用范围表示物
《中考化学第一轮复习考点分析:物质的构成》由会员桔****分享,可在线阅读,更多相关《中考化学第一轮复习考点分析:物质的构成》请在金锄头文库上搜索。

安全应急演练的讲话稿

料斗秤控制器说明书
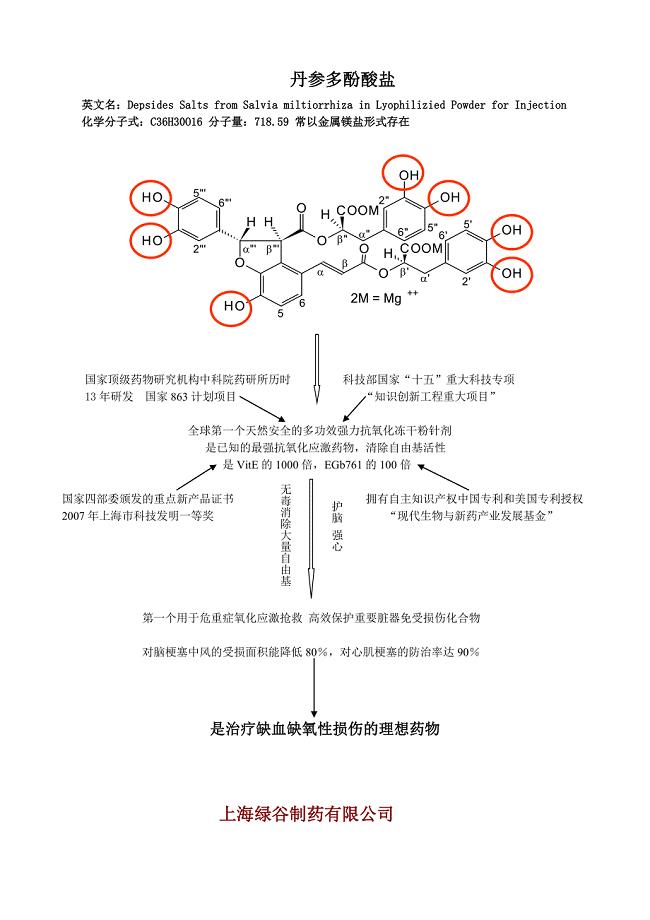
丹参多酚酸盐抗氧化资料电子版-丹参多酚酸盐

主题班会教案主题班会告别坏习惯养成好习惯
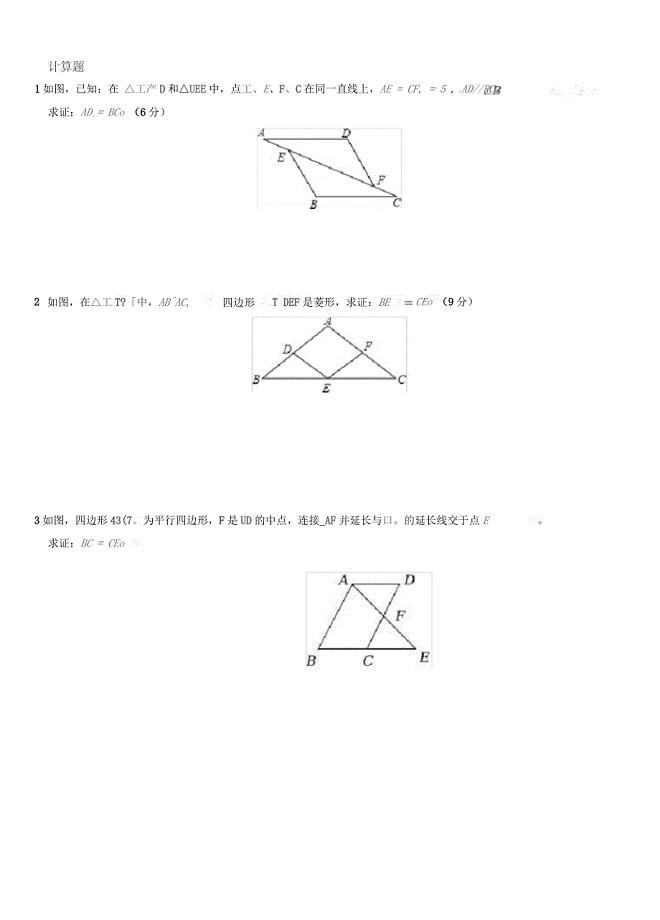
证明三角形全等专项练习

关于房屋租赁合同标准模板(7篇).doc

商务礼仪心得体会
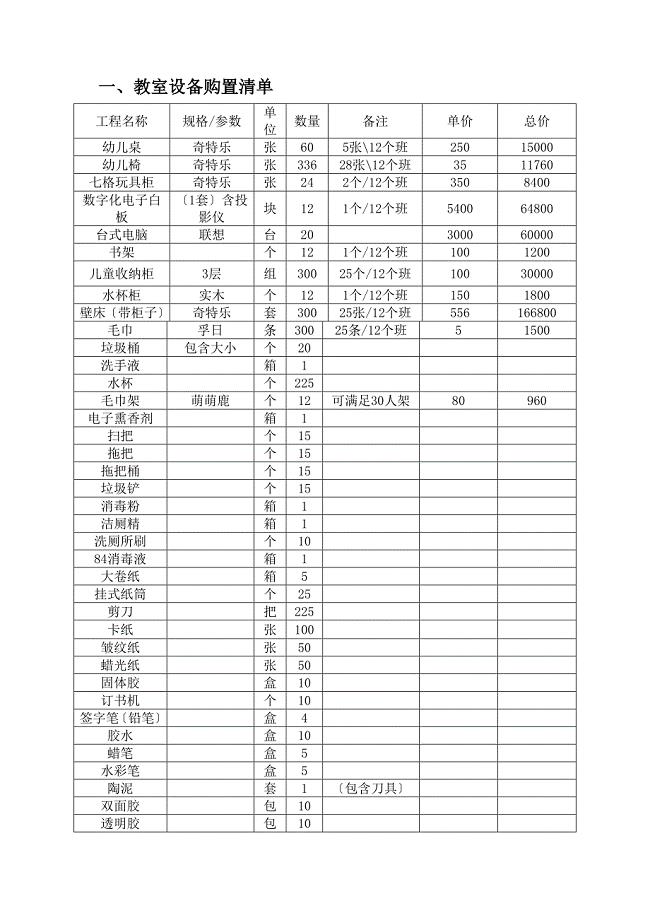
幼儿园活动室设备采购清单

六年级下学期数学期末测试一

争吵教学反思

活动合作协议标准范本(七篇).doc

安全系统管理系统人员资格证书复审复习资料

2018年学校元旦晚会主持词

unit 10 can you play the guitar 教案5(人教新目标七年级)doc--初中英语

感恩父母演讲稿

关于农村收入调查报告(实用)

班主任新学期工作目标计划范文(七篇).doc

阿昔洛韦片说明书用法用量及适应症

抵押车辆长期借款合同(四篇).doc

川农21秋《园林工程专科》在线作业一答案参考20
 2022年高中历史第二单元古代希腊罗马的政治制度第5课古代希腊民主政治练习新人教版必修
2022年高中历史第二单元古代希腊罗马的政治制度第5课古代希腊民主政治练习新人教版必修
2023-09-26 5页
 2022年高中英语必修四教案:Unit2 Word power教案
2022年高中英语必修四教案:Unit2 Word power教案
2023-11-16 2页
 高三地理世界地理试题
高三地理世界地理试题
2023-01-10 9页
 广东省揭阳市2012-2013学年高二理综下学期学业水平考试试题
广东省揭阳市2012-2013学年高二理综下学期学业水平考试试题
2022-07-26 15页
 高中生物必三好题2(含详细解析)
高中生物必三好题2(含详细解析)
2024-01-09 5页
 江苏省徐州市2020-2021学年高二生物上学期期中试题选修
江苏省徐州市2020-2021学年高二生物上学期期中试题选修
2023-08-04 10页
 2022年高考物理一轮复习第九章磁场微专题69带电粒子在圆形边界磁场中的运动备考精炼
2022年高考物理一轮复习第九章磁场微专题69带电粒子在圆形边界磁场中的运动备考精炼
2024-02-13 8页
 盐城市2013届高三第二次模拟考试语文试题及参考答案
盐城市2013届高三第二次模拟考试语文试题及参考答案
2023-06-09 11页
 高三课案非谓语
高三课案非谓语
2024-01-18 17页
 七年级 语文期中试卷(一)
七年级 语文期中试卷(一)
2022-09-06 2页

