
第二组阳离子分析
26页1、第三节第二组阳离子的分析(重点)本组包括PtT、Bi3+、CiT cd+、Hg、 mv) sbmv)、Sn (口寸)离子,称为铜锡组。它们的共同特 点是不被HCI溶液沉淀(PtT是很少量的(小于1mg- mLi),不能被HCI沉淀),但在0.3mol L-1HCI 溶液中,可与HS反应生成硫化物沉淀。按照本组分出的顺序,称为第二组;按照所用的组试剂, 称为硫化氢组。第二组阳藕子主要性废时Bi-Cd:lliei.Aidll. V)|ShllL VSn (【1、IV :1颇色匚L式91A-fft=_ X _ _ _ _B OCHn1S tKK f i HWl 1 Fl1 KitcOHK 1 巴络舍 物Ril ;(Rih .略棕)鉴足R产Cui MH 理蛀甘离初H ( u_CuL)_掩贼CdlNll J?掩亲隹1研(尢色;PM价石礼H AsO ; ws冏;P SnC哄J-ClSnClJ-父第化 还KittBii -Bi l战鉴定Bi1d心3He? - lit?*n l 蟹AsA AsmZ * J弘1&打HS;反闻PbS 1* rCuS JdS IAd : I谀苗1舄乂还贩心70SfcQ (f
2、t fl Sh.S, 罹红 问时TShASb-5n$ 1 17 J A ShS 1 X U D . Sn UJKSnaH-t Xrb 7 机谨里求的酸度L曲简辛解晶破坏H)O,状剧成腔体、本组离子的分析特性1. 离子的颜色本组离子中,除CiT为蓝色外,其余均无色2. 离子的存在形式铅、铋、铜、镉、汞具有显著的金属性质,在水溶液中主要以金属阳离子的形式存在;而砷、 锑、锡三种元素则表现出不同程度的非金属性质,它们在溶液中的主要存在形式随酸碱环境而不同, 主要以阴离子形式存在于溶液中。但由于存在下述平衡AsO 33-+6H= As3+3HOSbCl6 = Sb3+ 6C1-SnCI 42- = SrT+4C溶液中也或多或少地存在着简单阳离子,并能生成相应的硫化物(如SnS、AS2S3等),所以这些元素还是作为阳离子来研究。鉴定时并不严格区分它们的存在形式,只是泛指该元素,书写时只标出其氧化数,而不 具体指明其存在形式。3. 加水稀释Bi3+、sb )、Sn(“)离子(见前表) vn4. 络合物本组离子一般都能生成多种络合物。其中最常见的是氯络离子,因而大量CI-存在时可影响到各 简单离子的
3、浓度。另外,CiT、CcT等能生成氨或氰络离子:Cu(NH)42+、Cd(NH)42+、Cu(CN2+、Cd(CN2+,它们在CiT Cd+的分离和鉴定上有很多应用。Bi3+与I-生成黄色的BiI 4;用 于铋的鉴定。CiT、PtT和Bi3+能与甘油生成络离子;Hga与I-生成无色的Hg,它与KOH 一起的溶 液,可用于NM的鉴定,称为奈氏试剂。这些都具有一定的分析应用价值。5. 氧化还原性质砷、锑、锡三元素的离子具有两种比较稳定的价态,它们在分析上都具有重要的意义。例如,As(v)在冷而稀的HCI溶液中,与S通过一系列的反应,最终得到的是AS2S4,但这个过 程速率较慢,为了加速反应,先将As(v)还原为As(,)。通常使用NHI来还原。另外,Sn()还原性较强,很容易被氧化为Sn(叫。而且SnS不溶于NaS而SnS能溶于NaS,这 n样在进一步分组时,把一种元素分在两个组中,将Sn(I)归于uA而Sn)归于uB组,将使操作不便,故一般在进行沉淀之前加入Q将Sn(n)全部氧化成Sn,并加热将剩余的Q除去。锑的罗丹明B试法只对sb)有效,若溶液中的锑为三价则必须事先氧化。此外,将 还原
4、为Bi v金属Bi是铋的重要鉴定反应之一6. 与HHS的反应及本组硫化物性质PbSBi2S3CuSCdSHgSAS2S3SbSaSnSSnS颜色四八、黑褐四八、:黄四八、黄PT-桔红棕黄稀硝酸VVVVp T土水VVVVV TT浓盐酸VVVV稀盐酸V()VNqS:HgS2AsS3-SbS3SnS2-(NH4)-VVP TVRNaOHAsO3- + As3SVV氨水V极微 溶(NH4)V2C沉淀的性状:易成胶体沉淀的溶解度:CdS最大。二、组试剂与分离条件本组与第三、四组离子分离的依据是其硫化物溶解度有显著的差异。事实上,除本组能形成MS 沉淀,第三组大多数离子也能沉淀为硫化物。如何使本组沉淀完全,又不使第三组离 子混入?这就 是要讨论的分离条件一一组试剂的作用条件。通过对溶解度进行比较可以得出,第二组中溶解度最大的硫化物沉淀是CdS( KSP=7.1 X10-28),第三组中溶解度最小的硫化物沉淀是Zn S(KSp=1.2 x 10-23),比第二组大了大约五个数 量级,因此,按照沉淀规律,溶解度小的首先沉淀,溶解度大的不沉淀而留在溶液中,从而达到分 离的目的。也就是说:当第二组中最难沉
《第二组阳离子分析》由会员大米分享,可在线阅读,更多相关《第二组阳离子分析》请在金锄头文库上搜索。

造价工程师工作总结开头及(二篇).doc

三年级语文五册词语积累

最新 高中化学课时跟踪检测九离子键配位键与金属键鲁科版选修3

公务员的职业精神修炼题库

【施工管理】电气工程施工工艺标准(DOC 31页)

人教版小学数学五年级下册分数的基本性质教学设计

临床生物化学及检验教学大纲本科

混凝土路面工程监理实施细则
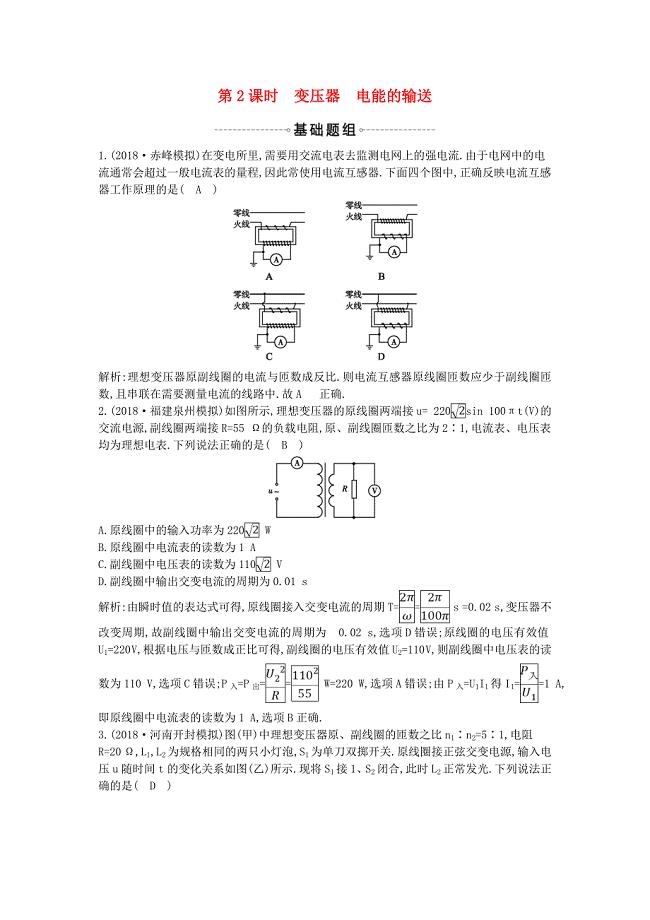
2019年高考物理总复习第十一章交变电流传感器第2课时变压器电能的输送课时训练教科版

玉米期货行情分析

沿河道截污专项施工方案

上半年社会保险工作总结
《鱼我所欲也》课堂教学设计(2课时)

现代酒店安全部应急能力浅析

2022年专接本-民法考前模拟强化练习题92(附答案详解)

郑州轻工业学院国家开发银行助学贷款管理

建筑实习生自我鉴定10篇

商法价值功能定位--兼史际春陈岳琴商榷

让高贵与高贵相遇阅读答案2

幼儿服务意识的培养
 浅谈农村公路发展
浅谈农村公路发展
2024-01-26 15页
 详解“首阴反包”战法精准捕捉强势股一抓一个准
详解“首阴反包”战法精准捕捉强势股一抓一个准
2023-06-13 5页
 美术教室的装备要求
美术教室的装备要求
2023-09-25 6页
 宇宙物质起源心得体会
宇宙物质起源心得体会
2022-12-17 15页
 对环境治理问题的看法
对环境治理问题的看法
2023-06-15 2页
 山东2013年会计从业资格《电算化》全真模拟题库一
山东2013年会计从业资格《电算化》全真模拟题库一
2022-12-19 18页
 伏笔与铺垫的区别
伏笔与铺垫的区别
2024-02-10 3页
 铝板幕墙构造原理与实例分析
铝板幕墙构造原理与实例分析
2022-08-23 13页
 增值税税收筹划
增值税税收筹划
2022-12-27 5页
 二级建造师考试工程施工管理重点内容归纳
二级建造师考试工程施工管理重点内容归纳
2022-08-03 65页

