
(中考化学)考点 21 金属的化学性质(解析版)
183页1、考点 21 金属的化学性质 (解析版)学霸笔记考点归纳【有笔记归纳、易错点、容量大试题、随时可用】归纳1 金属的三条化学性质归纳2 置换反应归纳3 金属活动性顺序归纳4 中考解题技巧与易错点:探究金属活动性、金属除杂、金属优先反应顺序归纳5 中考技巧性解答思路归纳( 金属活动性顺序的判断、鉴别和除杂、滤渣和滤液成分的判断、金属反应后溶液质量的变化、金属与酸反应数据和图像分析)归纳6 2022年、2021年、2020年、 2019年、2018年五年化学中考试题金属的化学性质汇编 (容量大、一次下载、值得拥有)(可供考生、教师:暑期自学、学霸笔记、备课、新课、期中复习、期末复习、重点高中自主招生考试、中考备考复习、组卷等等所用)考点归纳归纳1金属的三条化学性质1.与氧气反应金属化学方程式现象及解释Al4Al3O2=2Al2O3铝制品常温下缓慢氧化Fe3Fe2O2Fe3O4在氧气中剧烈反应、火星四射、生成黑色固体 Cu2CuO22CuO在空气中,不能燃烧,加热时,生成黑色固体Mg2MgO22MgO发出耀眼的白光,生成一种白色固体2.与稀盐酸、稀硫酸反应(1)条件:金属活动性必须排在氢之前。(
2、2)通式:金属酸盐氢气金属化学方程式现象及解释MgMg2HCl=MgCl2H2MgH2SO4=MgSO4H2剧烈反应,产生大量气泡ZnZn2HCl=ZnCl2H2ZnH2SO4=ZnSO4H2反应比较剧烈,产生大量气泡FeFe2HCl=FeCl2H2FeH2SO4=FeSO4H2反应缓慢,产生气泡,溶液由无色变为浅绿色Cu不反应3.与某些可溶性盐溶液的反应(1)条件:位于前面的金属把后面的金属从它的盐溶液(必须可溶)中置换出来。(2)通式:金属盐新金属新盐化学方程式现象及解释活动性FeCuSO4=FeSO4Cu铁表面有红色的物质生成,溶液由蓝色变为浅绿色FeCuCu2AgNO3=Cu(NO3)22Ag铜的表面有银白色的物质生成,溶液由无色变为蓝色CuAg2Al3CuSO4=Al2(SO4)33Cu铝表面有红色的物质生成,溶液由蓝色变为无色AlCu特别提醒:铁与酸反应生成的盐为亚铁盐(铁的化合价为2价);金属单质与盐反应,“盐”是指可溶性盐,不溶性盐不能发生反应,如:CuAgCl不反应。归纳2置换反应1.概念:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,叫置换反应。(
3、表达式:ABC=BAC)2.特点:反应物为单质和化合物,生成物为单质和化合物。反应前后化合价一定发生变化。3.置换反应类型: 金属+酸金属化合物+H2 金属+金属化合物另一金属+另一金属化合物C+金属氧化物金属单质+CO2 H2+金属氧化物金属单质+H2O(注意:CO+金属氧化物金属单质+CO2 该反应不属于基本反应) 化合反应:多变一 CO2+H2O = H2CO34.化学反应基本类型 分解反应:一变多H2CO3 = CO2+H2O置换反应:单化生化单C + 2CuO2Cu+CO2 复分解反应:归纳3 金属活动性顺序1.常见金属的活动性顺序 (巧记:捡个大美女;身体细纤轻;总共一百斤)钾 钙 钠 镁 铝 锌 铁 锡 铅 (氢) 铜 汞 银 铂 金K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au2.金属活动性顺序前面的金属比后面的金属活泼,位置越靠前,活动性越强。位于氢前面的金属能置换盐酸、稀硫酸中的氢。位于前面的金属能把位于后面的金属从它们的化合物的溶液里置换出来归纳4 中考解题技巧与易错点:探究金属活动性、金属除杂、金属优先反应顺序1.探究金
4、属活动性(1)“用酸”及控制变量法探究金属活动性(不与酸反应的金属至多一种): 请设计实验探究铝、铁、氢、铜的活动性,答出实验操作、现象和结论。 用试管各取少量盐酸分别加入足量铝铁铜丝,铜不反应说明三者中铜最不活泼。拿出铁丝后向余下溶液中加入足量铝丝,出现黑色固体,浅绿色溶液消失,说明铝比铁活泼。从而证明活动性从强到弱顺序为铝、铁、H、铜。“用盐溶液”探究金属活动性:例:设计实验探究Cu、Fe、Ag活动性顺序,答出操作、现象和结论。法一:串联式FeCuAg:将铁丝放入硫酸铜溶液中,出现红色金属说明铁比铜活泼;将铜丝放入硝酸银溶液中,出现银白色金属说明铜比银活泼。所以强弱顺序为FeCuAg。Cu法二:反证法排序后,“中间金属取单质”,两侧金属取盐溶液,Fe、 、Ag:将铜丝分别放入硫酸亚铁溶液和硝酸银溶液中,硫酸亚铁溶液中无变化,硝酸银溶液中的铜丝表面出现银白色金属,说明强弱顺序为FeCuAg。AgFe法三:反证法排序后,“中间金属取盐溶液”,两侧金属取单质, 、Cu、 :将铁丝、银丝分别放入硫酸铜溶液中,银丝无变化,铁丝表面出现红色金属,说明强弱顺序为FeCuAg。2.利用金属活动性除
《(中考化学)考点 21 金属的化学性质(解析版)》由会员厚***分享,可在线阅读,更多相关《(中考化学)考点 21 金属的化学性质(解析版)》请在金锄头文库上搜索。

(中考化学)考点 10 自然界的水 (学生版)

(中考物理)考点 24 溶液的溶质质量分数(解析版)

(中考化学)考点 12 质量守恒定律(学生版)

(中考化学)考点 01 化学使世界变得更加绚丽多彩 (解析版)

(中考化学)考点 29人类重要的营养元素(学生版)

(中考化学)考点 06 氧气制取(学生版)

(中考化学)考点 18 燃烧与灭火(学生版)

(中考物理)考点 22 溶液及其及配制(解析版)

(中考化学)考点 11 化合价与化学式 (解析版)

(中考物理)考点 22 溶液及其及配制(学生版)

(中考化学)考点 12 质量守恒定律(解析版)

(中考化学)考点 21 金属的化学性质(解析版)

(中考化学)考点 09 元素(学生版)

(中考化学)考点 21 金属的化学性质(学生版)
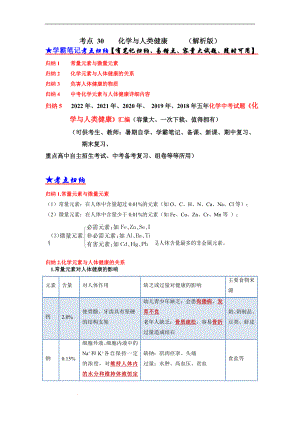
(中考化学)考点 30化学与人类健康 (解析版)

(中考化学)考点 07 分子和原子 (解析版)

(心理主题班会)放飞梦想,做主青春

(中考化学)考点 15 碳单质 (解析版)

(中考化学)考点 03 走进化学实验室 (学生版)
中考化学大一轮单元总复习 第十一单元 盐 化肥
 2018年安徽省中考化学试卷【含答案】.doc
2018年安徽省中考化学试卷【含答案】.doc
2023-09-15 6页
 2018年广东省中考语文试卷【含答案】.doc
2018年广东省中考语文试卷【含答案】.doc
2023-01-19 9页
 2019年天津市中考语文试题【含答案】.docx
2019年天津市中考语文试题【含答案】.docx
2023-12-25 13页
 2021年天津市中考化学试卷【含答案】.doc
2021年天津市中考化学试卷【含答案】.doc
2023-01-24 12页
 2019年天津市中考化学试卷【含答案】.doc
2019年天津市中考化学试卷【含答案】.doc
2023-09-30 8页
 第一次政治选择:晚清的开明专制化及其失败.doc
第一次政治选择:晚清的开明专制化及其失败.doc
2024-03-04 10页
 2022年湖北省中考生物试卷真题解析版Word版(8份打包).docx
2022年湖北省中考生物试卷真题解析版Word版(8份打包).docx
2023-01-14 59页
 2022年黑龙江中考物理试卷解析版Word版(4份打包).docx
2022年黑龙江中考物理试卷解析版Word版(4份打包).docx
2023-02-15 39页
 2019年广东省中考数学试卷【含答案】.docx
2019年广东省中考数学试卷【含答案】.docx
2023-11-01 20页
 2019年上海市中考物理试卷【含答案】.docx
2019年上海市中考物理试卷【含答案】.docx
2022-11-26 9页

