ISO13485:2016医疗器械质量体系管理手册
42页1、 *有限公司文件编号HH-QM-01版 本A1类别医疗器械质量管理手册生效日期20XX-01-27一级文件页 次Page 42 of 42医疗器械质量管理手册(符合ISO9001:2015和YY/T0287-2017/ISO13485:2016标准要求)制定部门制 定 / 日 期审核 / 日 期批准 / 日 期体系部文 件 发 行 栏采购部 PMC部 工程部 生产部 人力资源部 体系部 业务部 品管部 物管部 人力资源部 财务部 总经理 管理者代表其他:修 改 履 历序号章节版 次制定或修改內容日 期1全部A02016新版制定2017-7-282附录2A1职责分配表2021-01-26组织架构图 0目录0.2 前言及简述 50.3 管理者代表任命书 60.4 质量手册发布令 71. 范围 81.1 总则81.2 应用82. 引用标准 83. 术语 84 .质量管理体系 94.1 总要求94.2 文件要求 95.管理职责 125.1 管理者承诺125.2 以顾客为关注焦点125.3 质量方针125.4 策划135.5 职责、权限和沟通145.6 管理评审176 .资源管理 186.1 资
2、源提供186.2 人力资源186.3 基础设施186.4 工作环境和污染控制197 .产品实现 197.1 产品实现的策划197.2 与顾客有关的过程217.3 设计和开发227.4 采购237.5 生产和服务提供257.6 监视和测量设备的控制298 .测量、分析和改进 298.1 总则298.2 监视和测量308.3 不合格品控制338.4 数据分析348.5 改进34附录1质量目标 36附录2 职责分配表: 36附录3 程序文件清单 37附录4 组织架构图 38附录5 YY/T 0287-2017 和GB/T19001-2016 对应关系表 380.2、前言及简述本文件为*有限公司之医疗器械质量手册,详述本公司为符合顾客之要求所提供之质量、保证。为顺应世界潮流,迈向国际化,维持市场竟争力,满足客户及法律法规的要求,提高质量、管理与技术水准,改善管理及优化运作流程,建立以体系为主导,而非依靠个人的运作模式, 降低质量检验频率及费用,减少工作的偏差和提高效率,通过过程管理模式,持续改进,有效的帮助体制的改善,故依据ISO9001:2015质量管理体系要求、YY/T0287-2017/
3、ISO13485:2016医疗器械质量管理体系用于法规的要求、MDD/93/42EEC医疗器械指令和 FDA Quality system regulation(QSR 820)及医疗器械生产质量管理规范建立质量管理体系等相关要求,严格按质量、管理体系的要求进行全面的质量,达到甚至超越客户的要求。公司简介:*有限公司成立于2007年,属于外商独资企业。工厂坐落于*。公司主要经营硅橡胶制品及模切制品的生产与销售。产品广泛应用于电子电器业、五金塑胶业、运动器材等。公司成立至今一直坚持以“群策群力,品质至上;精益求精,客户满意”的品质方针及“不断开拓,不断研究,不断进取”的精神为客户提供最好的产品及服务。0.3、管理者代表为了贯彻执行ISO9001:2015质量管理体系要求、YY/T0287-2017/ISO13485:2016医疗器械质量管理体系用于法规的要求、MDD/93/42EEC医疗器械指令和 FDA Quality system regulation(QSR 820)及医疗器械生产质量管理规范加强对质量管理体系工作的领导。(管理者代表任命书见附件)其职责为:a) 协助总经理建立并保
《ISO13485:2016医疗器械质量体系管理手册》由会员体****识分享,可在线阅读,更多相关《ISO13485:2016医疗器械质量体系管理手册》请在金锄头文库上搜索。
 G312线奎屯-独山子经济技术开发区段公路建设项目环评报告
G312线奎屯-独山子经济技术开发区段公路建设项目环评报告
2024-05-29 37页
 G579线库车-拜城-玉尔滚公路建设(一期)工程环评报告
G579线库车-拜城-玉尔滚公路建设(一期)工程环评报告
2024-05-29 46页
 G218线霍尔果斯口岸段公路工程环评报告
G218线霍尔果斯口岸段公路工程环评报告
2024-05-29 32页
 压力管道工程施工常见技术要求知识点
压力管道工程施工常见技术要求知识点
2024-05-10 7页
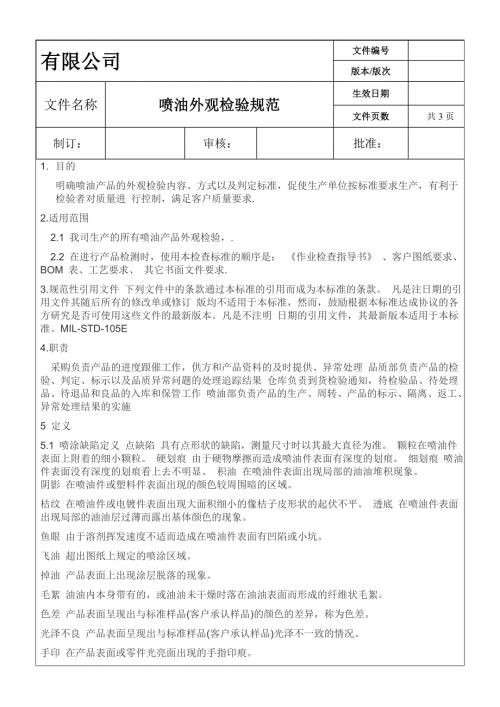
 喷油外观检验标准
喷油外观检验标准
2024-05-06 3页
 中天建设泽信青城一期临电专项施工方案
中天建设泽信青城一期临电专项施工方案
2024-05-06 105页
 中天建设石狮国工程临电专项施工方案
中天建设石狮国工程临电专项施工方案
2024-05-06 98页
 中天建设福建高层住宅工程临电专项施工方案
中天建设福建高层住宅工程临电专项施工方案
2024-05-06 98页
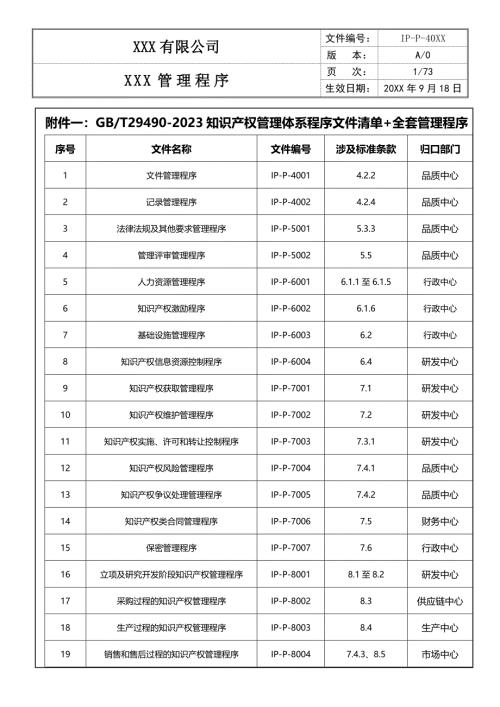
 知识产权管理体系全套程序文件+目录清单(29490-2023)
知识产权管理体系全套程序文件+目录清单(29490-2023)
2024-05-05 73页
 北京新机场防洪工程水土保持方案
北京新机场防洪工程水土保持方案
2024-05-05 253页