
原电池原理分析
13页1、原电池结构分析及相关考点练习考点一 原电池及其工作原理夯实基础1概念把转化为的装置。2形成条件(1) 一看反应:看是否有能自发进行的发生。(2) 二看两电极:一般是。(3) 三看是否形成闭合回路,形成闭合回路需三个条件:;。3工作原理(以下图铜锌原电池为例)电极材料锌铜电极名称电极反应反应类型电子流向电子从流出经外电路流入离子流向阳离子流向极,阴离子流向极思考:(1) 原电池内部阴、阳离子如何移动?为什么?(2) 两个半电池构成的原电池中,盐桥的作用是什么?考点练习:一、对原电池构成条件的考查A2Ag(s)Cd2(aq)=2Ag(aq)Cd(s)BCo2(aq)Cd(s)=Co(s)Cd2(aq)C2Ag(aq)Cd(s)=2Ag(s)Cd2(aq)D2Ag(aq)Co(s)=2Ag(s)Co2(aq)、对原电池工作原理的考查3. 如下图是Zn和Cu组成的原电池示意图,某小组做完该实验后,在读书卡片上作了如下记录,其中合理的是()稀硫酸卡片:No.10 Date: 20143 11实验记录:导线中电流方向:锌一铜。 铜极上有气泡产生。 锌片变薄。实验结论:Zn为正极,Cu为负极。 铜比
2、锌活泼。 H+向铜片移动。A.B.C.D.4. 如右图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡,小心地从烧杯中央滴入CuSO4溶液,片刻后可观察到的现 象是()A.铁圈和银圈左右摇摆不定B.保持平衡C.铁圈向下倾斜D.银圈向下倾斜小结: 原电池中的三个方向(1) 电子方向:电子从负极流出经外电路流入正极;(2) 电流方向:电流从正极流出经外电路流入负极;(3) 离子的迁移方向:电解质溶液中,阴离子向负极迁移,阳离子向正极迁移三、对原电池正、负极判断的考查5如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,由此判断表中所列M、N、P 物质,其中可以成立的是()MNPAZnCu稀 H2SO4BCuFe稀HC1CAgZnAgNO3溶液DZnFeFe(NO3)3 溶液B. 中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2 fC. 中Fe作负极,电极反应式为Fe-2e-=F+D. 中Cu作正极,电极反应式为2H+2e-=Hj 小结:原电池正、负极的判断方法说明:原电池的正极与负极与电极材料的性质有关,也与电解质溶液有关,不要形成活泼电极一定
3、作负极的思维定势。考点二 原电池工作原理的四大应用夯实基础1设计制作化学电源(1) 首先将氧化还原反应分成两个半反应。(2) 根据原电池的反应特点,结合两个半反应找出正、负极材料和电解质溶液。 2比较金属活动性强弱两种金属分别作原电池的两极时,一般作的金属比作的金属活泼。3加快氧化还原反应的速率一个进行的氧化还原反应,设计成原电池时反应速率。例如,在Zn与稀H2SO4反应时 加入少量CuSO4溶液能使产生H2的反应速率加快。4用于金属的防护使被保护的金属制品作原电池正极而得到保护。例如,要保护一个铁质的输水管道或钢铁桥梁等,可用导线将其与一块锌块相连,使锌作原电池的负极。思考:(1) X、Y两种金属用导线连接置于稀H2SO4中,发现X极溶解,Y极上有气泡产生,则X、Y 的活动性谁强?(2) 为了保护海水中的钢铁闸门,需要连接某种金属,你认为该金属的活动性应比铁的活动性强还是弱?(3) 依据原电池原理将反应Fe + 2FeCl3=3FeCl2设计成一个原电池。考点练习:3.把适合题意的图像填在横线上(用 A、B、C、D 表示)ABCD(1) 将等质量的两份锌粉a、b分别加入过量的稀硫酸,
4、同时向a中加入少量的CuSO4溶1.某原电池总反应为:Cu+2Fe3+=nCd2 +2Fe2 +,下列能实现该反应的原电池是()ABCD电极材料Cu、ZnCu、CFe、ZnCu、Ag电解液叫Fe(NO3)2CuSO”4Fe(SO)o2、“32电工经常说的一句口头禅:“铜接铝,瞎糊弄”,所以电工操作上规定不能把铜导线与铝导线连接在一起使用,说明原因:液,产生H2的体积V(L)与时间t (min)的关系是。(2) 将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是。(3) 将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图像是小结: 改变Zn与H+反应速率的方法(1) 加入Cu或CuSO4,形成原电池,加快反应速率,加入Cu不影响Zn的量,但加入 CuSO4,Zn的量减少,是否影响产生H2的量,应根据Zn、H+的相对量多少判断。(2) 加入强碱弱酸盐,由于弱酸根与H +反应,使c(H+)减小,反应速率减小,但不影响 产生h2的量。考点三 化学电源夯实基础1 . 一次电池(碱性锌锰干电池) 碱性
《原电池原理分析》由会员ni****g分享,可在线阅读,更多相关《原电池原理分析》请在金锄头文库上搜索。

中新社雅加达4月9日电

2021-2022年苏教版科学六年级下册《4.1寻找生物的家园》2课时教案

交通规划实习报告

工程经济与管理形成性考核册答案汇总

山东省淄博市临淄区边河乡中学八年级语文上学期期中试题新人教版06085

淄博高纯氢项目招商引资方案

2023家庭夫妻和平离婚协议书模板(二篇)

佛山半导体器件销售项目商业计划书范文模板

2021中秋节促销活动方案

2023年儿科护士工作总结

酒店营销部年度工作总结范文
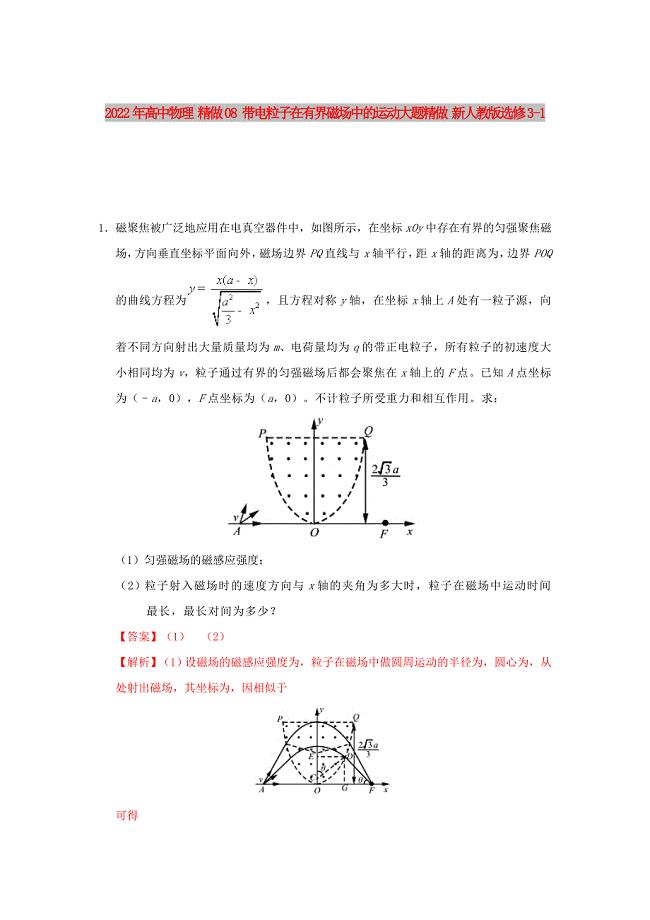
2022年高中物理 精做08 带电粒子在有界磁场中的运动大题精做 新人教版选修3-1

高考政治复习策略

九上圆复习提纲

植物体的结构与功能

2022年山西省建筑施工企业项目负责人(安全员B证)安全生产管理人员资格证书考核(全考点)试题附答案参考87

c程序设计练习题

产品初始污染菌和微粒污染控制验证方案

2015年学院工作要点

外科护理个人工作总结
 通用管理平台用户需求规格说明书
通用管理平台用户需求规格说明书
2023-10-04 40页
 小班音乐欣赏活动详案《咿呀咿呀哟》
小班音乐欣赏活动详案《咿呀咿呀哟》
2022-09-21 4页
 人教版七年级上册英语单词默写标准模板
人教版七年级上册英语单词默写标准模板
2022-07-31 26页
 秦岭终南山隧道2014版
秦岭终南山隧道2014版
2023-04-13 14页
 气支撑计算
气支撑计算
2023-11-03 2页
 微藻能源规模化制备的科学基础
微藻能源规模化制备的科学基础
2022-10-15 23页
 保温节能施工方案完成
保温节能施工方案完成
2023-06-09 25页
 反映企业经营状况的财务分析方法
反映企业经营状况的财务分析方法
2023-12-21 11页
 危废管理计划
危废管理计划
2023-05-04 22页
 数值比较器的设计与仿真
数值比较器的设计与仿真
2023-11-14 7页

