
1.1类化学药品从研发到上市
12页1、1.1类化学药品研究:从研发到上市1.1类化学药品,指未在国内外上市销售的药品,通过合成或者半合成的方法制得的原料药及其制剂。新药从研发到上市的过程中需进行的工作包括:(1)药物临床前研究(药物的合成工艺、提取方法、理化性质、纯度、剂型选择、处方筛选、制备工艺、检验方法、质量指标、稳定性)(2)药理、毒理、动物药代动力学研究等(3)申请获得临床试验批件(4)进行临床试验(包括生物等效性试验)研究(5)新药申请、获得新药证书和药品批准文号(6)药品生产上市,上市后监测具体需进行的工作如下:1. 药学研究包括:合成工艺、剂型选择、处方筛选、结构确证、质量研究和质量标准制定、稳定性研究等1.1 原料药的制备研发及生产工艺研究原料药制备研发过程一般包括以下六个阶段:1、确定目标化合物;2、设计合成路线;3、制备目标化合物;4、结构确证;5、工艺优化;6、中试研究和工业化生产。原料药生产工艺的研究:包括工艺流程和化学反应式、起始原料和有机溶媒、反应条件(温度、压力、时间、催化剂等)和操作步骤、精制方法、主要理化常数及阶段性的数据积累结果等,并注明投料量和收得率以及工艺过程中可能产生或引入的杂质或
2、其他中间产物,及工艺验证。1.2 制剂处方及工艺研究应包括起始物料、处方筛选、生产工艺及验证。制剂研究的基本内容一般包括以下方面:1、剂型选择;2、处方研究;3、制剂工艺研究;4、药品包装材料(容器)的选择;5、质量研究和稳定性研究。1.3 确证化学结构或组份根据化合物(药物)的结构特征制订科学、合理、可行的研究方案,制备符合结构确证研究要求的样品,进行有关的研究,对研究结果进行综合分析,确证测试品的结构;该过程主要包括化合物的名称,样品的制备,理化常数的研究,样品的测试及综合解析等;常用的分析测试方法有紫外可见吸收光谱、红外吸收光谱、核磁共振谱、质谱、比旋度、X-射线单晶衍射或/和X-射线粉末衍射、差示扫描量热法、热重等。1.4 质量研究原料药的质量研究应在确证化学结构或组份的基础上进行,一般研究项目包括:性状(外观、色泽、臭、味、结晶性、引湿性等;溶解度;熔点或熔距;旋光度或比旋度;吸收系数等)、鉴别(化学反应法、色谱法和光谱法等)、检查(一般杂质;有关物质,是在生产过程中带入的起始原料、中间体、聚合体、副反应产物,以及贮藏过程中的降解产物等;残留溶剂;晶型;粒度;溶液的澄清度与颜
3、色、溶液的酸碱度;干燥失重和水分;异构体等)和含量测定等几个方面。药物制剂的质量研究,通常应结合制剂的处方工艺研究进行,质量研究的内容应结合不同剂型的质量要求确定。与原料药相似,制剂的研究项目一般亦包括性状(考察样品的外形和颜色)、鉴别(一般至少采用二种以上不同类的方法,如化学法和HPLC法等)、检查(含量均匀度;溶出度;释放度;杂质;脆碎度;pH值;异常毒性、升压物质、降压物质;残留溶剂等)和含量测定等几个方面。方法学验证内容,包括方法的专属性、线性、范围、准确度、精密度、检测限、定量限、耐用性和系统适用性等。1.5 建立药品质量标准质量标准应当符合中国药典现行版的格式,并使用其术语和计量单位。所用试药、试液、缓冲液、滴定液等,应当采用现行版中国药典收载的品种及浓度,有不同的,应详细说明。标准品或对照品,说明其来源、理化常数、纯度、含量及其测定方法和数据。药品标准起草说明应当包括标准中控制项目的选定、方法选择、检查及纯度和限度范围等的制定依据。1.6 药物稳定性研究稳定性研究内容可分为影响因素试验(一般包括高温、高湿、光照试验)、加速试验(在超常条件下进行)、长期试验(在上市药品规定
4、的贮存条件下进行)等。通过对影响因素试验、加速试验、长期试验获得的药品稳定性信息进行系统的分析,确定药品的贮存条件、包装材料/容器和有效期。2. 药理毒理研究包括:药效学、作用机制、一般药理、毒理、药代动力学等2.1 主要药效学试验2.2 一般药理学试验目的:确定药物可能关系到人的安全性的非期望药理作用;评价药物在毒理学和/或临床研究中所观察到的药物不良反应和/或病理生理作用;研究所观察到的和/或推测的药物不良反应机制。选用的模型:整体动物、离体器官及组织、体外培养的细胞、细胞片段、细胞器、受体、离子通道和酶等。整体动物常用小鼠、大鼠、豚鼠、家兔、犬等,动物选择应与试验方法相匹配,同时还应注意品系、性别及年龄等因素。安全药理学的核心组合实验用于研究受试物对重要生命功能的影响,包括对中枢神经系统、心血管系统、呼吸系统通等重要器官系统的研究。2.3 急性毒性试验研究动物一次或24小时内多次给予受试物后,一定时间内所产生的毒性反应。一般应选用一种啮齿类动物加一种非啮齿类动物至少两种哺乳动物,雌雄各半,不同给药途径进行急性毒性试验。给药后,一般连续观察至少14天,观察的间隔和频率应适当,以便能
《1.1类化学药品从研发到上市》由会员s9****2分享,可在线阅读,更多相关《1.1类化学药品从研发到上市》请在金锄头文库上搜索。

新材料作文审题立意十大方法

教科版五年级科学下册第一单元测试卷及答案.docx

人教版七年级上册语文作业本答案

荔波漳江导游词

电子技术课程设计报告硬件超声波测距仪模板

春季开学典礼学生演讲稿
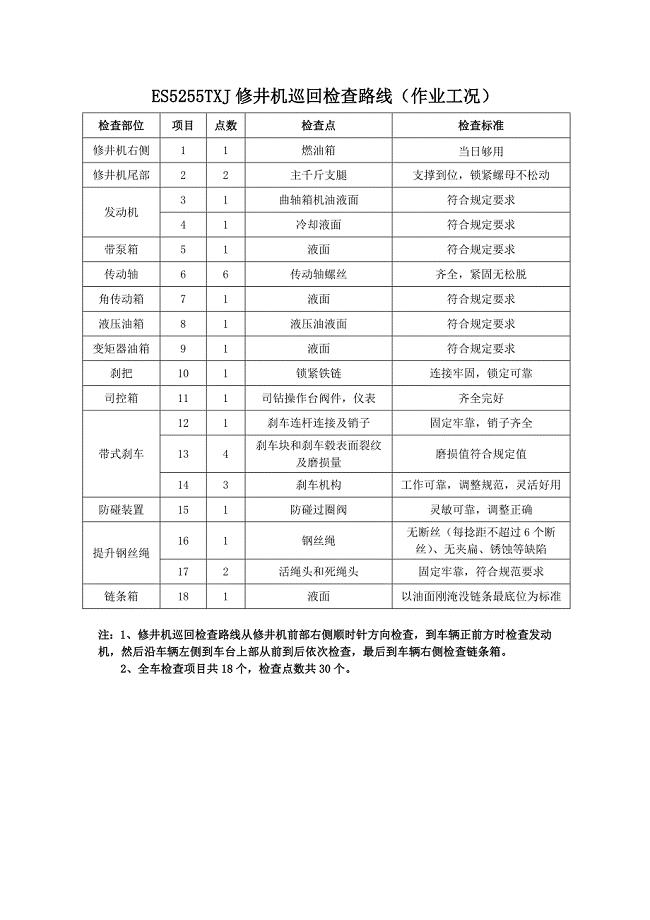
ES5255TXJ修井机巡回检查路线(作业工况)

2023年贵州茅台股票分析报告

市司法局的工作总结

剪力墙结构外文翻译

全套公司绩效考核办法附表格

治病救急术法摘集打印版

优秀教师事迹材料走在学生的花丛中

《去年的树》教学设计

建设工程安全监督档案指南(doc 67页)dnag

最新整理场费用管理条例x

监理工作的指导思想和监理目标

关于安全阀、压力表实行定期检验的规定

宿舍空调管理规定(三篇)

幼儿园秋季保育工作计划范文(三篇).doc
 006休闲中心员工奖罚制度
006休闲中心员工奖罚制度
2023-04-21 16页
 推荐100种常见家常菜的做法
推荐100种常见家常菜的做法
2022-10-25 17页
 福建师范大学21秋《中国画》平时作业一参考答案65
福建师范大学21秋《中国画》平时作业一参考答案65
2024-01-08 13页
 分部分项安全技术交底(同名13016)
分部分项安全技术交底(同名13016)
2022-11-30 45页
 印染废水处理工程设计设计
印染废水处理工程设计设计
2022-10-14 84页
 古诗(带拼音)(同名21980)
古诗(带拼音)(同名21980)
2023-04-26 18页
 川农21春《室内装饰材料专科》在线作业二满分答案6
川农21春《室内装饰材料专科》在线作业二满分答案6
2023-09-21 14页
 2010年与2009年考研数学大纲变化对比——数一
2010年与2009年考研数学大纲变化对比——数一
2023-02-25 14页
 精英论坛-曹纪平经典话术
精英论坛-曹纪平经典话术
2023-02-28 7页
 企业如何进行纳税筹划
企业如何进行纳税筹划
2022-12-28 15页

