
高考化学总复习《化学计量及其应用》专项检测卷-附带答案
10页1、高考化学总复习化学计量及其应用专项检测卷-附带答案学校:_班级:_姓名:_考号:_一、选择题(共12题)1.设NA为阿伏加德罗常数的值。下列说法正确的是( )A. 0.1 mol 27Al3+中含有的电子数为1.3NAB. 100 mL 1 molL1Na2S溶液中含有的阴离子数小于0.1NAC. 标准状况下,22.4 L乙炔中含有的 键数为5NAD. 23 g Na与足量的氧气反应转移的电子数为NA2.室温下,甲同学配制100 g 5%的NaCl溶液,乙同学配制100 mL 0.5 mol/L的NaCl溶液(NaCl的溶解度为36 g/100 g水)。下列说法正确的是( )A. 所需溶质的质量相同B. 所需仪器均包括100 mL容量瓶C. 所配溶液均为不饱和溶液D. 所配溶液质量相同3. 设NA为阿伏加德罗常数的值。下列叙述正确的是( )A. 1 mol FeCO5中含有的 键的数目为5NAB. 标准状况下,22.4 LCH4和22.4 LCl2在光照条件下充分反应后的分子数目为2NAC. 1 molCaH2固体含有的离子数目为2NAD. 一定条件下,5.6 g Fe与0.1 mol
2、Cl2充分反应,转移的电子数为0.3NA4. 在2.8 g Fe中加入100 mL 3 molL1 HCl溶液,Fe完全溶解。NA代表阿伏加德罗常数的值,下列说法正确的是( )A. 反应转移电子的物质的量为0.1 molB. HCl溶液中Cl数为3NAC. 2.8 g 56Fe含有的中子数为1.3NAD. 反应生成标准状况下3.36 L气体5. 科学家通过分析探测器从小行星“龙宫”带回地球的样品,分析出有多种有机化合物分子,其中有两种的结构简式如下图所示。设阿伏加德罗常数的值为NA,下列说法正确的是( ) 乙酸 丙氨酸A. 0.1 mol/L乙酸溶液中含有H+的数目为0.1NAB. 1 mol丙氨酸中NH数目为2NAC. 1 molNH2中电子数为10NAD. 1 mol乙酸可与足量钠反应生成11.2 L H26.设NA为阿伏加德罗常数的值。下列叙述正确的是( )A. 1 molCu(H2O)42+中配位键的数目为12NAB. 标准状况下,22.4 L H2O2中含非极性键的数目为NAC. 常温下,1 L pH=5的NH4Cl溶液中,由水电离出的H+的数目为1105NAD. 2 mol
3、 NO和1 mol O2在密闭容器中充分反应后可得分子的总数目为2NA7. 配制100 mL 1.00 molL1NaOH溶液的操作如下图所示。下列说法不正确的是( )A. 操作1前用托盘天平称取NaOH的质量为4.0 gB. 操作2前NaOH溶液需恢复至室温C. 操作4为定容D. 操作5后液面下降,需补充少量水至刻度线8. 臭氧法处理含氰废水的主要反应原理为5O3+2CN+H2O 5O2+2HCO3+N2。设NA为阿伏加德罗常数的值,下列说法错误的是( )A. 生成1 mol HCO3转移的电子数目为3NAB. 16 g O3和O2的混合物中含有的原子数目为NAC. 标准状况下,22.4 L N2中所含的电子数为14NAD. 2.6 g CN中含有的 键的数目为0.1NA9.设NA为阿伏加德罗常数的值,下列关于反应:S8+NaOHNa2S+Na2SO3+H2O(未配平)的说法不正确的是( )A. 1 mol S8参与反应,断裂8NA个SS共价键B. 生成1 molNa2S,转移2NA个电子C. 1 L pH=12的NaOH溶液中有0.01NA个Na+D. 6.3 gNa2SO3中含有
4、0.15NA个 键10.用硫酸铜晶体CuSO45H2O配制480 mL浓度为0.5 molL1的CuSO4溶液。下列说法正确的是( )A. 用托盘天平称量60.0 g硫酸铜晶体B. 若称量时试剂和砝码放反了,则对配制结果无影响C. 若定容时俯视容量瓶刻度线,则会使所配溶液浓度偏高D. 在转移溶液后,可以不用洗涤烧杯和玻璃棒11. 氨对水体的污染情况越来越受人们的重视。用次氯酸钠可以脱除水中的NH3,原理为2NH3+3NaClO N2+3NaCl+3H2O。设NA为阿伏加德罗常数的值,下列说法正确的是( )A. 33.6 LNH3中所含的 键数目为4.5NAB. 2 L 0.5 mol/L NaClO溶液中含有的ClO数目为NAC. 若该反应生成27 g H2O,则转移的电子数为3NAD. 2 mol N2与3 mol H2在密闭容器中反应生成的NH3分子数为2NA12. 铁和铝都是用途广泛的金属,同温、同压下,将m g铁与足量稀硫酸反应,生成H2的体积为V1 L;将n g铝与足量浓氢氧化钠溶液反应,生成H2的体积为V2 L。下列说法正确的是( )A. 两反应生成H2的物质的量之比为mn
《高考化学总复习《化学计量及其应用》专项检测卷-附带答案》由会员夏***分享,可在线阅读,更多相关《高考化学总复习《化学计量及其应用》专项检测卷-附带答案》请在金锄头文库上搜索。
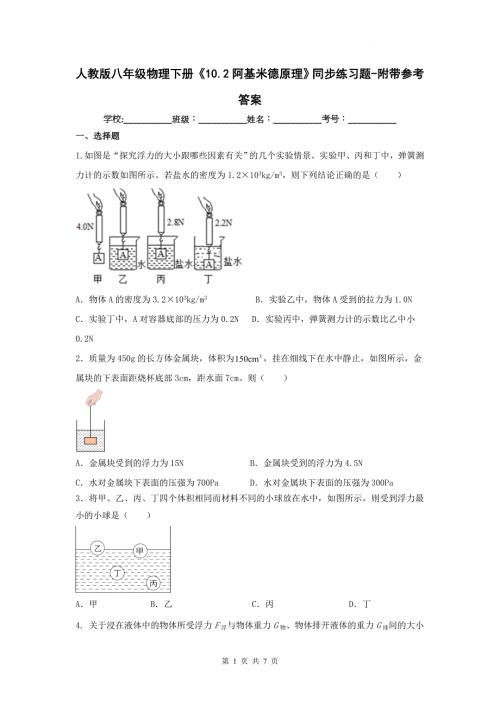
人教版八年级物理下册《10.2阿基米德原理》同步练习题-附带参考答案

人教版八年级物理下册《第十章浮力》同步测试卷-带有答案
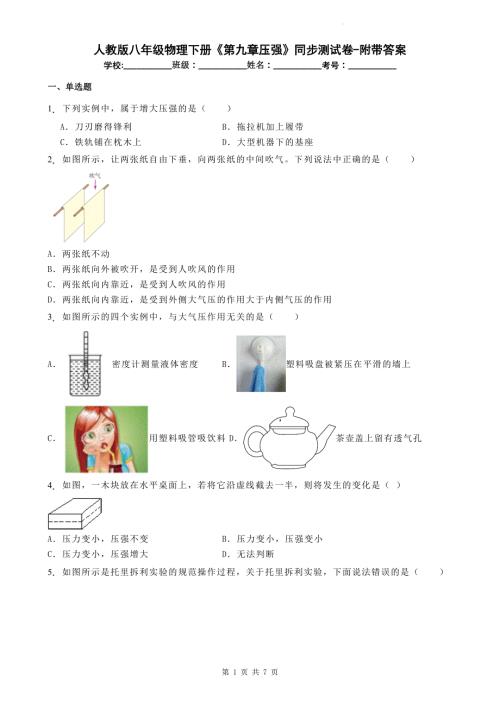
人教版八年级物理下册《第九章压强》同步测试卷-附带答案

人教版八年级物理下册《第十章浮力》同步测试卷-含参考答案

教科版八年级物理上册期末测试卷(带参考答案)

教科版八年级物理上册期末测试卷(带答案与解析)

人教版八年级物理下册《第十章浮力》同步测试卷-附含答案

人教版八年级物理下册《9.3大气压强》同步练习题-附带答案

教科版八年级物理上册期末测试卷(附有答案)

教科版八年级物理上册期末测试卷(带答案)

人教版八年级物理下册《10.1浮力》同步练习题-附带答案

人教版八年级物理下册《第十—章功和机械能》同步测试卷-附带答案
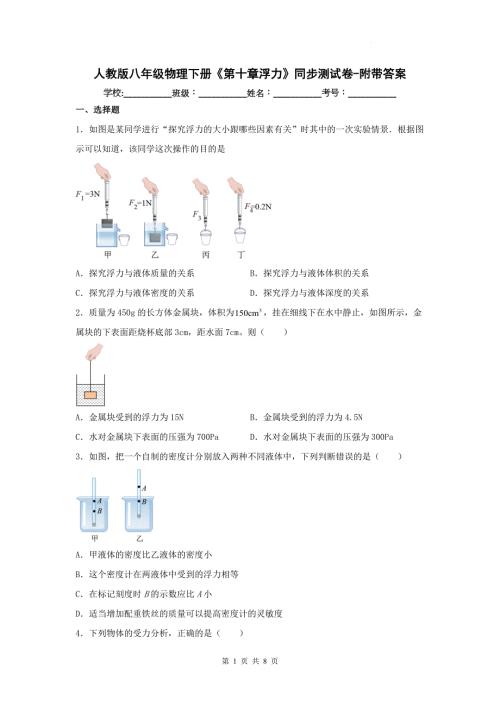
人教版八年级物理下册《第十章浮力》同步测试卷-附带答案

教科版八年级物理上册期末测试卷(含有答案)

人教版八年级物理下册期末测试卷(带参考答案)

人教版八年级物理下册《第十二章简单机械》同步测试卷-附带答案

人教版八年级物理下册《10.3物体的浮沉条件及应用》同步练习题-附含答案

教科版八年级物理上册期末测试卷(带有答案)

人教版八年级物理下册《10.3物体的浮沉条件及应用》同步练习题-含答案

人教版八年级物理下册《第十二章简单机械》同步测试卷-附含答案
 2023年北京市中考数学真题和答案
2023年北京市中考数学真题和答案
2024-05-14 36页
 2023年福建省中考数学真题和答案
2023年福建省中考数学真题和答案
2024-05-14 32页
 2023年甘肃省兰州市中考数学真题和答案
2023年甘肃省兰州市中考数学真题和答案
2024-05-14 38页
 2023年湖南省衡阳市中考数学真题和答案
2023年湖南省衡阳市中考数学真题和答案
2024-05-14 33页
 2023年广东省深圳市中考数学真题和答案
2023年广东省深圳市中考数学真题和答案
2024-05-14 32页
 安徽省合肥市2024届高三第三次教学质量检测化学试题Word版无答案
安徽省合肥市2024届高三第三次教学质量检测化学试题Word版无答案
2024-05-14 10页
 湖南名校联盟2024届高三全真模拟(5月)适应性考试政治试题Word版
湖南名校联盟2024届高三全真模拟(5月)适应性考试政治试题Word版
2024-05-14 6页
 2024届江苏省南通市高三下学期三模英语试题
2024届江苏省南通市高三下学期三模英语试题
2024-05-14 8页
 山西省临汾市2024届高三下学期三模试题英语Word版含答案
山西省临汾市2024届高三下学期三模试题英语Word版含答案
2024-05-14 14页
 2024届湖南省高三下学期5月适应性考试语文试题
2024届湖南省高三下学期5月适应性考试语文试题
2024-05-14 8页

