
2011年高考理综化学7+4模拟强化试题及答案(下篇)
52页1、2011年高考理综化学7+4模拟卷(11)第I卷(选择题共42分)一、选择题(每小题只有一个选项符合题意)7.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物之一。下列关于MMF的说法正确的是A.MMF能溶于水 B.MMF能发生取代反应和消去反应C.1molMMF能与6mol氢气发生加成反应 D.1molMMF能与含3molNaOH溶液完全反应8.元素A的单质及A与B形成的化合物能按如下图所示的关系发生转化。则下列说法正确的是AABnABn+1置换化合化合化合A.图中物质间的转化可能有非氧化还原反应B.当n=1时,A可能是N2C.A一定是金属元素 D.当n=2时,A可能是Fe 9.酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2C7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是乙醇沸点低 乙醇密度比水小 乙醇有还原性 乙醇是烃的含氧化合物A B C D 高#考#资#源#网10.将pH=1的稀硫酸慢慢加入定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100 mL(混合时溶液体积的变化忽略不计
2、),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度为A.0.011 mol/L B.0.22 mol/L C.0.022 mol/L D.0.11 mol/L11.甲、乙、丙、丁4中物质分别含2种或3种元素,它们的分子中各含18个电子。甲是气态氢化物,在水中分步电离出两种阴离子。下列推断合理的是A.某酸溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键C.丙中含有二周期IVA族的元素,则丙一定是甲烷的同系物D.丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 12.25时,将pH=a的CH3COOH溶液VamL与pH=12的NaOH溶液VbmL混合。下列说法正确的是A.若Va=Vb,且NaOH与CH3COOH恰好完全反应,则a2B.若a=2,混合后溶液pH=7,则混合后V总2VbC.若a=2,混合后溶液pHc(CH3COO-)c(OH-)c(H+)13.某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质
3、的量随NaOH溶液的体积变化的图象如下图所示,下列说法正确的是A.原溶液中一定含有SO42-和Na+B.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 高#考#资#源#网D.反应最后形成的溶液中含有的溶质为Na2SO4第II卷25.(14分)A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出)。(1)若A是常见金属单质,与B的水溶液反应生成C和D。D、F是气体单质,D在F中燃烧时发出苍白色火焰。则反应(在水溶液中进行)的离子方程式为 。(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属。且两个反应都有红棕色气体生成,则反应的化学方程式为 。(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色。则D的电子式是 ;工业上生产B的第一个生产阶段是煅烧与A含相同元素的矿石,其化学方程式是 ,使用的设备是 。(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应的化学方程式是 ,B与烧碱溶液反应的化学方程式是 。
《2011年高考理综化学7+4模拟强化试题及答案(下篇)》由会员suns****4568分享,可在线阅读,更多相关《2011年高考理综化学7+4模拟强化试题及答案(下篇)》请在金锄头文库上搜索。

土地管理与地籍测量---第八章界址点测量
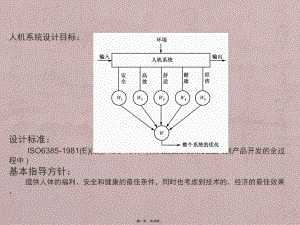
人机工程学案例分析(2)

工程安全培训_201303

第9章房地产投资决策分析

第2章房地产经纪制度

ACM程序设计-东北林业大学acm05

《亲爱的汉修先生》读书交流会

中原_深圳新世界尖岗山项目市场汇报_40P_2012年_别墅_项目分析_量价走势

五年级数学质量分析演示文稿

人工智能小镇-智慧小镇建设20180525

景观基本知识及发展历程

建设工程信息管理(2)

机电驱动技术第二章步进驱动技术
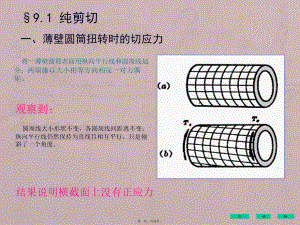
工程力学-第9章圆轴扭转时的应力变形分析与强度刚度设计

第一章第二节幼儿园文化环境建设的原则

第一章检测技术的基础知识

第一章__现代表面工程技术

第六章钢结构工程

第9节项目试运行管理

班主任工作经验交流课件(4)
 钱学森读书心得700字范文
钱学森读书心得700字范文
2023-04-22 8页
 机器人总动员经典电影观后感
机器人总动员经典电影观后感
2023-04-05 13页
 关于提高民办学校教学质量的提高
关于提高民办学校教学质量的提高
2023-07-02 4页
 教师师徒结对心得体会
教师师徒结对心得体会
2023-11-18 19页
 不一样的梦想作文800字大全
不一样的梦想作文800字大全
2023-09-30 5页
 高速桥绿化工程投标文件技术标
高速桥绿化工程投标文件技术标
2024-02-04 49页
 一年级语文的教学反思
一年级语文的教学反思
2023-12-26 34页
 单位工作失误检讨书【多篇】
单位工作失误检讨书【多篇】
2023-08-18 26页
 2022出纳年终工作总结范文6篇【实用模板】
2022出纳年终工作总结范文6篇【实用模板】
2022-09-21 13页
 英语老师求职自荐信
英语老师求职自荐信
2023-06-16 15页

