
综合实验1___同周期、同主族元素性质的递变
11页1、综合实验1 同周期、同主族元素性质的递变实验目的:1 结合所学知识了解实验方案的意义,巩固对同周期、同主族元素性质递变规律的认识。2 掌握常见药品的取用、液体的加热以及萃取等基本操作。3 能准确描述实验现象,并根据现象得出相应结论。实验原理:同周期元素从左到右,金属性渐弱,非金属性渐强。同主族元素从上到下,非金属性渐弱,金属性渐强。元素金属性的强弱可以从元素的单质跟水或酸溶液反应置换出氢气的难易,或由元素最高氧化物对应水化物氢氧化物的碱性强弱来判断;元素非金属性的强弱可以从元素最高氧化物水化物的酸性强弱,或跟氢化合生成气态氢化物的难易以及氢化物的稳定程度来判断,另外也可以由非金属单质是否能把其它元素从它们的化合物里置换出来加以判断。实验器材:仪器:试管、小烧杯、酒精灯、胶头滴管、试卷夹。试剂:钠块、镁条、铝片、氯水(新制)、溴水、氯化钠溶液、溴化钠溶液、碘化钠溶液、稀盐酸(1mol/L)、酚酞试液其它材料:镊子、滤纸、砂纸、玻璃片、火柴(或打火机)。实验步骤1同周期元素性质的递变(1)取100mL小烧杯,向烧杯中注入约50mL水,然后用镊子取绿豆大小的一块钠,用滤纸将其表面的煤油擦去,
2、放入烧杯中,盖上玻璃片,观察现象。反应完毕后,向烧杯中滴入23滴酚酞试液,观察现象。(2)取两支试管各注入约5mL的水,取一小片铝和一小段镁带,用砂纸擦去氧化膜,分别投入两支试管中。若前面两支试管反应缓慢,可在酒精灯上加热,反应一段时间再加入23滴酚酞试液,观察现象。(3)另取两支试管各加入2mL 1mol/L盐酸,取一小片铝和一小段镁带,用砂纸擦去氧化膜,分别投入两支试管中,观察现象。2. 同主族元素性质的递变(1)在三支试管里分别加入约3 mL氯化钠、溴化钠、碘化钠溶液,然后在每一支试管里分别加入新制备的氯水2mL,观察溶液颜色的变化。再各加入少量四氯化碳,振荡试管,观察四氯化碳层的颜色。 (2)在三支试管里分别加入约3 mL氯化钠、溴化钠、碘化钠溶液,然后在每一支试管里分别加入溴水2mL,观察溶液颜色的变化。再各加入少量四氯化碳,振荡试管,观察四氯化碳层的颜色。现象记录和结论实验操作实验现象实验结论同周期元素性质的递变钠块放入盛水的烧杯中铝、镁与水的反应铝、镁与盐酸的反应同主族元素性质的递变氯化钠、溴化钠、碘化钠溶液分别加入新制备的氯水,加入少量四氯化碳氯化钠、溴化钠、碘化钠溶液
3、分别加入溴水,加入少量四氯化碳实验评价与改进: 1实验2中使用的氯水为何要新制备的?加四氯化碳试剂的目的是什么?2如何设计实验证明同周期的硫、氯元素的非金属性强弱?3如何设计实验证明同主族的钠、钾元素的金属性强弱?实验改进意见及实验感悟:综合实验2 乙酸与乙醇的性质 乙酸乙酯的制备实验目的:1掌握观察液态有机物颜色、状态、气味的基本方法。2掌握向试管中添加液体试剂、实验仪器的装配、给试管中的液体加热等基本操作。3了解制备乙酸乙酯的基本原理,能确定产物的生成。实验原理:1CH3COOH CH3COO + H + ,2CH3COOH + Na2CO3 2CH3COONa + H2O + CO2 ;22CH3CH2OH + O2 2CH3CHO + 2H2O ;3CH3CH2OH + CH3COOH CH3COOCH2CH3 + H2O 。实验器材:仪器:试管、大烧杯、酒精灯、胶头滴管、铁架台(带铁夹)、单孔塞、导管若干。试剂:无水乙醇、冰醋酸、粗铜丝、热水、稀醋酸溶液、饱和Na2CO3溶液、石蕊试液、浓硫酸。其它材料:火柴(或打火机)。实验步骤1乙酸的性质向两支试管中各加入3mL稀醋酸溶液
4、,分别滴加石蕊试液、饱和Na2CO3溶液。2. 乙醇的性质 向试管中加入3 4mL无水乙醇,浸入50左右的热水中。将铜丝下端弯成螺旋状,用酒精灯外焰烧热至表面变黑后,迅速插入无水乙醇中。反复多次,观察并感受铜丝颜色和乙醇气味的变化。3乙酸乙酯的制备(1)在一支试管中加入3mL无水乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸。在另一支试管中加入饱和Na2CO3溶液。按右图所示连接好装置。(2)用酒精灯小心均匀地加热试管3 5 min ,使混合液保持微沸,产生的蒸气经导管冷凝后通到饱和Na2CO3溶液的液面上,注意观察液面上的变化。(3)取下盛有Na2CO3溶液的试管(小心不要被烫着),并停止加热。(4)振荡盛有Na2CO3溶液的试管,静置,待溶液分层后,观察上层的油状液体,并注意闻气味。现象记录和结论实验操作实验现象实验结论乙酸的性质稀醋酸溶液中滴加石蕊试液稀醋酸溶液中滴加饱和Na2CO3溶液。乙醇的性质烧热至表面变黑后的铜丝迅速插入无水乙醇中,反复多次。乙酸乙酯的制备用酒精灯小心均匀地加热已加好无水乙醇、浓硫酸和冰醋酸的试管3 5 min ,使混合液保持微沸,产生的蒸气经导
《综合实验1___同周期、同主族元素性质的递变》由会员jiups****uk12分享,可在线阅读,更多相关《综合实验1___同周期、同主族元素性质的递变》请在金锄头文库上搜索。

建立安全生产长效机制-共创和谐平安输气管道

土石方爆破工程设计方案

康师傅百货商场制度汇编之退换货管理办法

庙头中学2012年中考百日誓师大会学生代表发言稿

围堰拆除爆破工程

华能洱源马鞍山风电场工程土石方爆破管理制度

国资委:全面开展管理提升活动-为培育世界一流企业奠定坚实基础

《专业技术人员职业发展与规划》电子书

应收票据审计方案
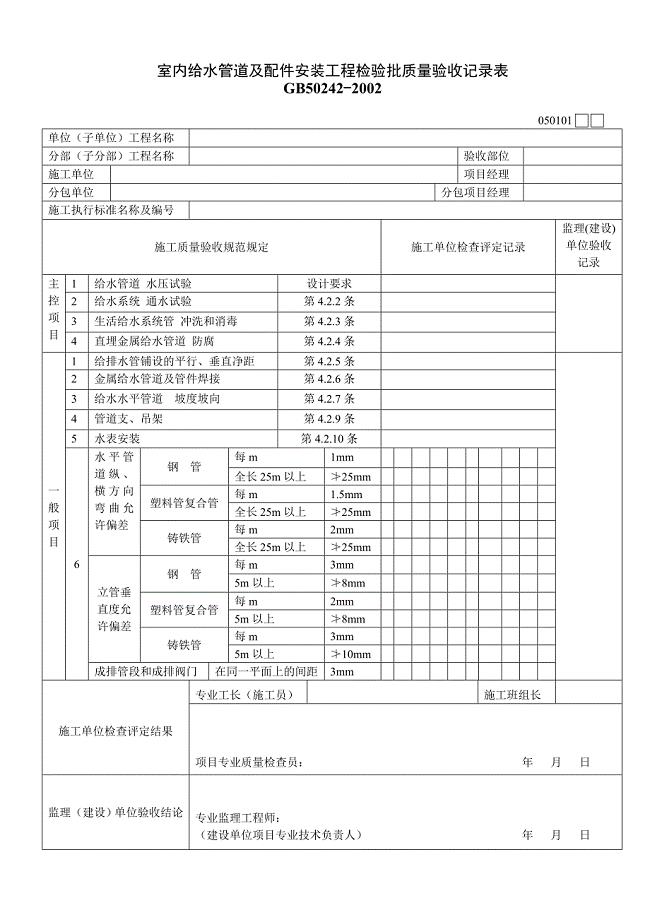
建筑给水排水与采暖工程质量验收用表

广播电视管理条例行政处罚裁量标准

广东电力系统调度运行操作管理规定

建筑给排水工程名词解释

幼儿园小班安全健康活动教案:宝宝误食后的急救

建业集团房屋建筑工程交房标准内容技术交底

建筑心理学论文(1)

康师傅百货商场制度汇编之工服管理程序009

建筑工程专业一级建造师继续教育培训结业报告20

廉洁风险防控回头看工作汇报材料

平台工作人员服务规范
 2024年安徽省芜湖市中考二模语文试卷【含答案】
2024年安徽省芜湖市中考二模语文试卷【含答案】
2024-04-24 10页
 2024届河北省邯郸市中考一模语文试题【含答案】
2024届河北省邯郸市中考一模语文试题【含答案】
2024-04-24 10页
 2024年(6月份)中考数学押题试卷【含答案】
2024年(6月份)中考数学押题试卷【含答案】
2024-04-24 25页
 2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024-04-24 10页
 辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
2024-04-23 4页
 第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
2024-04-23 10页
 江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
2024-04-23 19页
 江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
2024-04-23 10页
 江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
2024-04-23 16页
 小学六年级体育与健康测试题【含答案】
小学六年级体育与健康测试题【含答案】
2024-04-23 5页

