
化学平衡练习题
4页1、化学平衡练习题1、体积完全相同的两个容器A和B,已知A装有SO2和O2各1g,B装有SO2和O2各2g,在相同温度下反应达到平衡时A中SO2的转化率为a%,B中SO2的转化率为b%,则A、B两容器中SO2转化率的关系正确的是( )A、a%b% B、a%b% C、a%b% D、2a%b%2、在密闭容器中进行H2(g)+Br2(g)2HBr(g)(正反应放热),反应达到平衡后,欲使颜色加深,应采取的措施是( )A、升温 B、增压 C、减压 D、降温 3、对反应2NO2(g)N2O4(g),在一定条件下达到平衡,在温度不变时,欲使c(NO2)/ c(N2O4)的比值增大,应采取的措施是( )A、体积不变,增加NO2的物质的量 B、使体积增大到原来的2倍C、充入N2,保持压强不变 D、体积不变,增加N2O4的物质的量4、在容积相同且固定不变的四个密闭容器中,进行同样的可逆反应:2A(g)+B(g)3C(g)+2D(g)起始时四个容器所盛A、B的量分别为:甲:2mol A,1mol B;乙:1mol A,1mol B;丙:2mol A,2mol B;丁:1mol A,2mol B。在相同温度下建
2、立平衡时,A、B的转化率大小关系正确的是( )A、A的转化率:甲丙乙丁 B、A的转化率:甲乙丙丁C、B的转化率:甲丙乙丁 D、B的转化率:甲乙丙丁5、对达到平衡的可逆反应X+YW+Z,增大压强则正、逆反应速率(v)的变化如下图,分析可知X,Y,Z,W的聚集状态可能是( )A、Z,W为气体,X,Y中之一为气体B、Z,W中之一为气体,X,Y为非气体C、X,Y,Z皆为气体,W为非气体D、X,Y为气体,Z,W中之一为气体6、某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B2C。若维持温度和压强不变,当达到平衡时容器的体积为VL,其中C气体的体积占10%。下列推断正确的是( )原混合气体的体积为1.2VL 原混合气体的体积为1.1VL 反应达到平衡时气体A消耗掉0.05 VL 反应达到平衡时气体B消耗掉0.05 VLA、 B、 C、 D、7、在容积固定为2L的密闭容器中,充入X、Y气体各4mol,发生可逆反应:X(g)+2Y(g)2Z(g),并达平衡,以Y的浓度改变表示的反应速度与时间t的关系如图所示,则Y的平衡浓度表达式正确的是(式中S是对应区域的面积)( )8
3、、()()()(正反应为吸热反应)的可逆反应中,在恒温条件下,B的体积分数()与压强(p)的关系如图6所示,有关叙述正确的是()。 点,正逆;点,正逆 点比点反应速率快9、某温度下,在固定容积的容器中,可逆反应A(g)+3B(g)2C(g)达到平衡。测得平衡时物质的量之比为A:B:C=2:2:1。保持温度不变,以2:2:1的体积比再充入A、B、C,则( )A、平衡向正反应方向移动 B、平衡不移动C、C的百分含量增大 D、C的百分含量有可能减小10、将固体NH4I置于密闭容器中,在一定温度下发生下列反应:NH4I(s)NH3(g)+HI(g);2HI(g)H2(g)+I2(g)。达到平衡时,c(H2)=0.5mol/L, c(HI)=4mol/L,则此温度下反应的平衡常数为( )A、9 B、16 C、20 D、2511、在密闭容器中充入4mol X,在一定温度下4X(g)3Y(g)+Z(g),达到平衡时有30%的X发生分解,则平衡时混合气体总的物质的量是( )A、3.4mol B、4mol C、2.8mol D、1.2mol12、在恒温、恒容下,有反应2A(g)+2B(g)C(g)+3D
《化学平衡练习题》由会员汽***分享,可在线阅读,更多相关《化学平衡练习题》请在金锄头文库上搜索。

高三数学一模试卷

煤矿应急救援指挥机构管理机构组织机构及管理职责

智力障碍儿童感知觉发展

污水处理施工方案

谜语小游戏谜语谜底

巴西铁矿石购销合同英语

公司销售员工工作计划标准范本(四篇).doc
![以面层底面弯拉应力为控制指标的沥青路面可靠性分析[资料]](https://union.152files.goldhoe.com/2023-11/17/bdcba1b7-fb7b-4cb2-abf0-75e6abca3d74/pic1.jpg)
以面层底面弯拉应力为控制指标的沥青路面可靠性分析[资料]

小学五年级语文教案少年闰土

二语复习教案
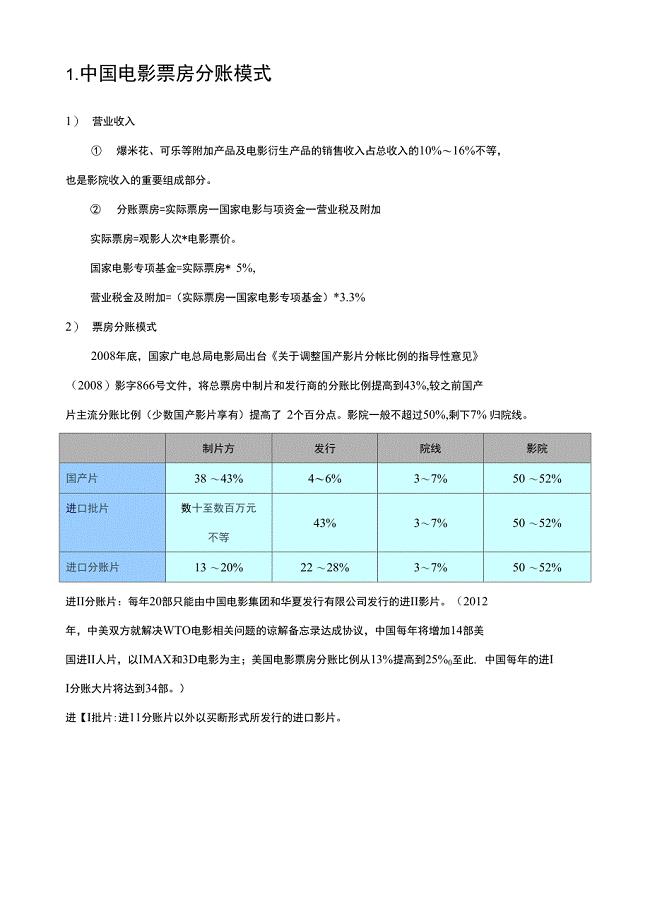
票房及分成常识

发客户邮件的格式范文6篇

舟山关于成立精密轴公司可行性报告(参考范文)

探索语文多媒体教学课件的评价标准

2023年教师转正述职报告_2

镇江消费电子功能性产品项目申请报告(参考模板)

工程造价实习鉴定

扬州市房地产抵押按揭合同书

恐艾症产生的原因及脱恐方法
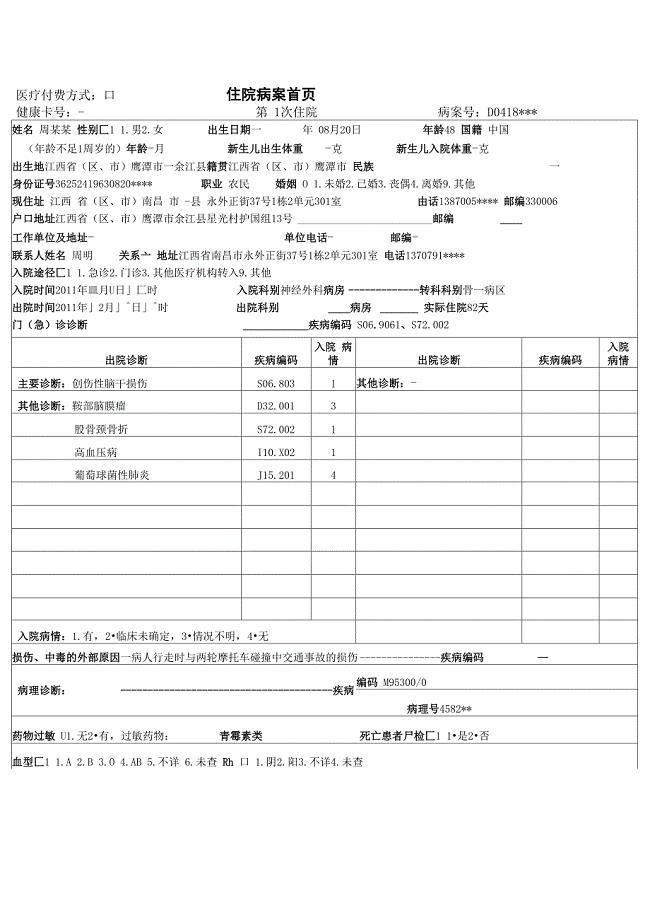
新病案首页填写范例及填写说明
 《女娲补天》预习卡
《女娲补天》预习卡
2024-03-08 1页
 临床路径病历质控表
临床路径病历质控表
2023-02-01 2页
 高三专业基础课十月月考试试题机械基础
高三专业基础课十月月考试试题机械基础
2024-01-01 3页
 如何安全使用电器?
如何安全使用电器?
2023-03-18 1页
 8年级英语阶段测试(月考)
8年级英语阶段测试(月考)
2023-04-28 4页
 2014年北京高考物理试题和答案
2014年北京高考物理试题和答案
2023-03-23 9页
 上交的李希贵思想交流
上交的李希贵思想交流
2023-11-20 3页
 分数四则混合运算经典题型
分数四则混合运算经典题型
2023-03-19 2页
 五上1-4单元重点句的理解
五上1-4单元重点句的理解
2024-02-09 1页
 云南省禁毒防艾知识竞赛试题及参考答案
云南省禁毒防艾知识竞赛试题及参考答案
2023-05-04 23页

