
分析方法的选择
5页1、分析方法的选择 一般而言 ,体内样品中待测物的预期浓度范围是决定体内样品检测方法的首要因素。无论从 动物或人体内获得的体内样品,其中所含药物或其特定代谢产物的浓度大多较低 (1O-io-1O-6g/ml).且难以通过增加体内样品量提高方法员敏度。因而在建立体内样品分析方法 时选择适宜的检测方法是必须首先考虑的。1. 色谱分析法 气相色谱、高效液相色谱等2. 免疫分析法放射免疫分析法(RIA)酶免疫分析法(EIA)荧光免疫分析法(FIA),多用于蛋白质多肽等生物大分子的检测3. 生物学方法 常能反映药效学的本质,用于抗生素类亚欧我的体内分析4.由于色谱分析法具有较高的灵敏度、选择性、准确度和精密度被广泛使用分析方法建立的一般程序1)色谱条件的筛选2)色谱条件的优化3)试验样品的测试分析方法的验证(一)选择性1. 内源性物质的干扰2. 未知代谢产物的干扰3. 同服药物的干扰4. 与参比方法的相关性二)标准曲线与定量范围标准曲线反应了体内样品中所测定药物的浓度与仪器响应值的关系(三)定量下限定量下限(LLOQ)是标准曲线上的最低浓度点,表示方法的灵敏度即测定样品中符 合准确度和精密度要求的最
2、低药物浓度。(四)精密度与准确度精密度(precisio n)是指在确定的分析条件下相同生物基质中相同浓度样品的一系 列测量值的分散程度。通常用QC样品的相对标准差(RSD)表示。MM-SAKUftxy= M 1QQ% 阳;= 3009!;准确度(acecuraey)是指在确定的分析条件下测得的试验样品浓度与真实浓度的 接近程度,通常用QC样品的实测浓度与标示浓度的百分比(accuracy)或相对偏差 (relative rror,RE)表示。准确度可通过重复测定已知浓度的待测物样品获得。x|(W=工工g-讦-工淀-订t=) J=1E-|J A-l 批为r嗣=工-五)样品稳定性在体内药物分析中。含药体内样品由临床实验室(或动物实验室)采集后转移 至分析实验室进行分析测试 ,通常不能及时完成分析;另-方面,体内样品的数量- 般较大,在1个工作日内难以完成全部体内样品的分析,通常需在多个工作日内完 成;其次,随着自动进样器的应用,多个处理过的样品同时置于自动进样器中等待 分析;再者,每个未知体内样品一般测定 1次,但有时亦需进行复测。此外分析物 和内标物储备液和工作溶液在整个分析过程中的稳
3、定性也很重要。为确保分析结 果的可靠性与可重复性,必须在分析方法的每一步骤确保样品的稳定性。对分析物和内标的储备液和工作溶液以及QC样品的稳定性考察应在不同储 存条件下进行,时间尺度应考虑试验样品储存的时间1. 短期稳定性 通常应考察分析物和内标的储备液和工作溶液及 QC 样品 从冰箱储存条件到室温或样品处理温度下短期放置的稳定性、QC样品的冷冻和 融化稳定性,以及处理过的样品在自动进样器温度下的稳定性,以保证检测结果 的准确性和重现性。2. 长期稳定性 在整个样品分析期间,QC样品的长期储存.以及分析物和 内标的储备液和工作溶液的长期储存稳定性也将影响着分析结果的准确性和重 现性。所以,需对QC样品在冰冻(-20C或-80C)条件下、分析物和内标的储备液和 工作溶液在特定温度(如4C或-20C)下以及不同存放时间进行稳定性评价,以确定 QC样品和分析物和内标的储备液和工作溶液稳定的存放条件和时间,应在确保样 品稳定的条件下进行测定。3 .测定方法(1)测定法与要求:采用低和高浓度 QC 样品,进行室温或样品处理温度下的短期 放置稳定性.冷冻和融化稳定性、冰箱长期储存的长期稳定性以及处
《分析方法的选择》由会员大米分享,可在线阅读,更多相关《分析方法的选择》请在金锄头文库上搜索。

2023年服务员年终工作总结模板(2篇).doc

大班安全教案多篇汇总版详
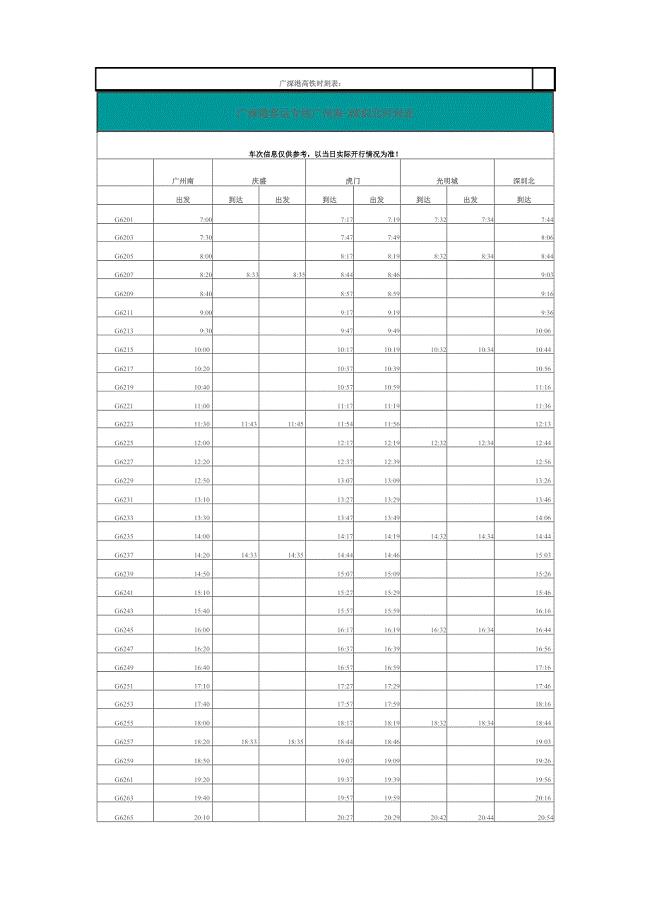
广深港高铁时刻表

心理培训心得体会15篇

学校应急演练计划书

竞聘演讲稿开头和结尾

三明仪器仪表销售项目商业计划书范文

郑州市国际国内物流大通道项目评估报告(参考模板)

2022年高中物理选修(3-4)第5章《新时空观的确立》word章末总结学案

2012年物业管理师《物业管理综合能力》 实战模拟试卷

吹响林东五小美术艺术号角

好用的劳动合同集锦9篇

幼儿园大班学期教学工作总结四篇

2022年人事科长竞聘演讲稿范本

固体垃圾废弃物填埋场课程设计

幼儿教师学习心得体会集锦三篇

小学英语骨干教师培训计划参考范文(二篇).doc

氧化氯的使用范围和使用方法

2023年大班上学期个人计划例文(二篇)

教室、公共场所消毒记录表
 心理培训心得体会15篇
心理培训心得体会15篇
2023-11-13 33页
 土木工程概论复习总结
土木工程概论复习总结
2022-09-17 8页
 WPCS风电控制系统概述
WPCS风电控制系统概述
2022-07-29 8页
 10 各向异性屈服条件和流动理论
10 各向异性屈服条件和流动理论
2023-02-17 13页
 比较器电路
比较器电路
2022-12-05 6页
 矿井通风常见事故案例
矿井通风常见事故案例
2023-05-06 13页
 混凝土技术资料
混凝土技术资料
2022-12-14 9页
 江南大学科技成果
江南大学科技成果
2023-07-24 2页
 安全保护装置
安全保护装置
2022-10-06 9页
 码头竣工验收报告
码头竣工验收报告
2023-03-03 9页

