
盐类的水解知识点总结
14页1、盐类的水解1. 复习重点1. 盐类的水解原理及其应用2. 溶液中微粒间的相互关系及守恒原理2. 难点聚焦(一)盐的水解实质压。 H*+OHIl IIHB A(OH)b当盐AB能电离出弱酸阴离子(B)或弱阳离子即可与水电离出的H或OH结合成电 解质分子,从而促进水进一步电离.与中和反响的关系:水解、盐+水丁二一一酸+碱(两者至少有一为弱)中和由此可知,盐的水解为中和反响的逆反响,但一般认为中和反响程度大,大多认为 是 完全以应,但盐类的水解程度小得多,故为万逆反响,真正发生水解的离子仅占极小比例。(二)水解规律简述为:有弱才水解,无弱不水解越弱越水解,弱弱都水解谁强显谁性,等强显中性具体为:1. 正盐溶液 强酸弱碱盐呈酸性 强碱弱酸盐呈碱性 强酸强碱盐呈中性 弱酸碱盐不一泄如 NHtCNCHACOcNH,NHF碱性中性酸性取决于弱酸弱碱相对强弱 假设只有电离而无水解,那么呈酸性(如NaHSOj 假设既有电离又有水解,取决于两者相对大小电离程度水解程度,呈酸性电离程度V水解程度,呈碱性强碱弱酸式盐的电离和水解:如H,PO :及其三种阴离子随溶液pH变化可相互转化:pH值增大A焉 0, Hf
2、Oi HPOf POfpH减小 常见酸式盐溶液的酸碱性碱性:NaHCOx NaHS、NaGPO,、立 HS酸性(很特姝,电离大于水解):NaHSO3. NaHzPO : . NaHSO ;三)影响水解的因素内因:盐的本性.外因:浓度、湿度、溶液碱性的变化(1)温度不变,浓度越小,水解程度越大.(2)浓度不变,湿度越高,水解程度越大.(3)改变溶液的pH值,可抑制或促进水解。(四)比拟外因对弱电解质电离和盐水解的影响.HA H+A Q 宁令 +比 0Q温度(T) Tt-*a tTt-*h t加水平衡正移,t促进水解,ht增大Hj抑制电离,a f促进水解,hf增大OH 促进电离,a t抑制水解,hf增大A 抑制电离,(】f 水解程度,ht注:a一电离程度h一水解程度思考:弱酸的电离和弱酸根离子的水解互为可逆吗?在CHcCOOH和CHACOONO :的溶液中分别参加少呈:冰醋酸,对CHjCOOH电离程度 和CHeCOO水解程度各有何影响?(五)盐类水解原理的应用考点1.判断或解释盐溶液的酸碱性例如:正盐KX、KY、KZ的溶液物质的量浓度一样,其pH值分别为7、8、9,那么HX、HY、HZ的酸
3、性强弱的顺序是一样条件下,测得NaHC03C&COOWNaAlO :三种溶液的pH值一样。那实验么它 们 的物质的量浓度由大到小的顺序是因为电离程度CH3COOHHA1O :所以水解程度NaA10= NaHC03CIJCOONS一样条件下,要 使三种溶液pH值一样,只有浓度32. 分析盐溶液中微粒种类.例如Na: S和NaHS溶液溶液含有的微粒种类一样,它们是Na S :、HS、H : S、OH、H H: 0,但微粒浓度大小关系不同.考点2-比拟盐溶液中离子浓度间的大小关系.(1)一种盐溶液中各种离子浓度相对大小 当盐中阴、阳离子等价时不水解离子 水解的离子 水解后呈某性的离子(如IT或0H 显性对应 离子 如0H或打实例:aCH3C00Na. bNHCla. Na* CH5C00 OH H*b. Cl NH OH 当盐中阴、阳离子不等价时。要考虑是否水解,水解分几步,如多元弱酸根的水解,那么是几价分几步,为主第一步, 实例Na : S水解分二步S : +H=0+0H (主要)HS +H : 0 LA : S+0H (次要)各种离子浓度大小顺序为:NaSs EOH HS if(2)两种
4、电解质溶液混合后各种离子浓度的相对大小. 假设酸与碱恰好完全以应,那么相当于一种盐溶液. 假设酸与碱反响后尚有弱酸或弱碱剩余,那么一般弱电解质的电离程度盐的水解程度.考点3溶液中各种微粒浓度之间的关系以Na:S水溶液为例来研究(1) 写出溶液中的各种微粒阳离子:Na H*阴离子:S、HS、OH(2) 利用守恒原理列出相关方程.1电荷守恒:Na+H*=2S= + HS + 0H 2物料守恒:Na.S=2Na+S:假设SE发生局部水解,S原子以三种微粒存在于溶液中。S 、HS ,根据S原 子守恒及 N/的关系可得.Na+=2Ss +2HS +2H=S3质子守恒H : 040H由比0电离出的H=OH ,水电离出的IT局部被S:结合成为HS、H : S,根据H(质 子守 恒,可得方程:OH = H*+HS +2H-S想一想:假设将Na : S改为NaHS溶液,三大守恒的关系式与Na : S对应的是否一样?为什 么?提示:由于两种溶液中微粒种类一样,所以阴、阳离子间的电荷守恒方程及质子守恒 是一 致的。但物料守恒方程不同,这与其盐的组成有关,假设NaHS只考虑盐本身的电离而不考虑 HS的进一步电
《盐类的水解知识点总结》由会员ni****g分享,可在线阅读,更多相关《盐类的水解知识点总结》请在金锄头文库上搜索。

2023年调度员个人工作总结范文(5篇).doc

开学第一课观后感范文

吉林省中考化学试题

走进珐琅厂体验景泰蓝喇中社会实践方案

三年级上册美术教案

【管理精品】离职分析的理论和实现上

单项式系数和次数

信访和群众工作目标考核的自查报告范文

小学学校工作总结-(-上)

《农村环境综合整治调查问卷》

KingSCADA初级教程第五章动画连接与脚本程序

实习报告审计实习报告

2022年内蒙古成品保护施工方案

医院感染管理培训制度

电气工程及其自动化毕业设计论文(最终版本)资料

元旦文艺联欢晚会主持词范文
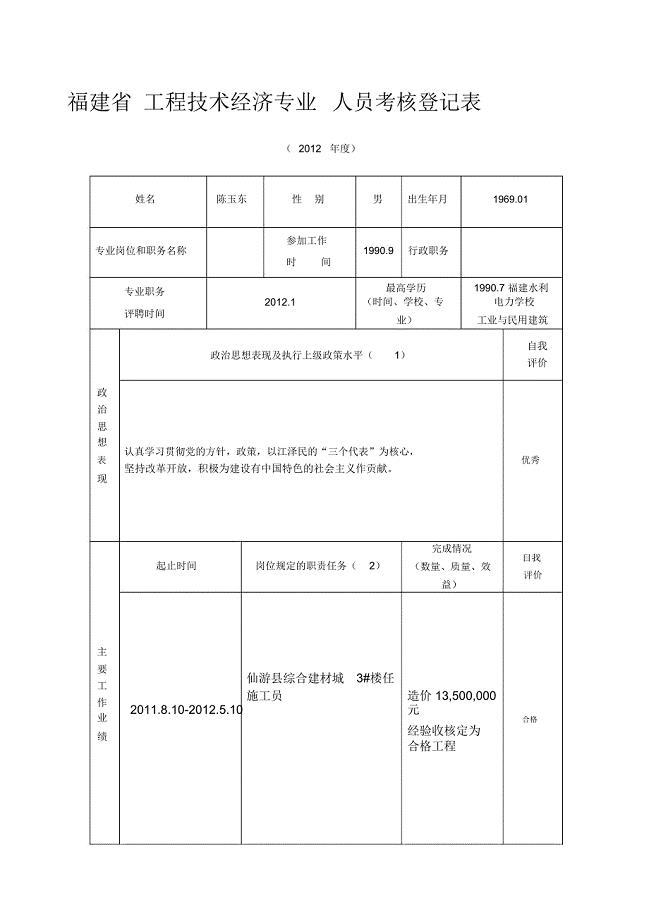
福建省工程技术经济专业人员考核登记表

新老师培训心得体会_2

收银员心得体会

有关小学教学计划二年级3篇
 基因突变及其他变异 (1)
基因突变及其他变异 (1)
2023-12-07 8页
 管理学原理学习总结
管理学原理学习总结
2023-11-09 8页
 企业税务基本知识
企业税务基本知识
2023-05-10 14页
 浙江农产品出口贸易的现状以及对策论文
浙江农产品出口贸易的现状以及对策论文
2022-07-12 25页
 某市自来水厂DN600市政管道安装工程施工组织设计(word版本)
某市自来水厂DN600市政管道安装工程施工组织设计(word版本)
2023-04-23 31页
 模型技巧完全手册-喷漆的方法
模型技巧完全手册-喷漆的方法
2023-03-04 8页
 am和dsb振幅调制器的设计
am和dsb振幅调制器的设计
2024-02-05 11页
 毕业设计(论文)双容水箱液位调节阀远程控制系统的设计
毕业设计(论文)双容水箱液位调节阀远程控制系统的设计
2023-05-20 53页
 抗滑桩专项施工方案(word)可编辑
抗滑桩专项施工方案(word)可编辑
2024-02-10 46页
 谐波对于电网的危害非常大
谐波对于电网的危害非常大
2022-12-06 4页

