
考点19、硫酸及其盐
22页1、考点 19、硫酸及其盐1 复习重点1硫酸的性质及重要用途;浓硫酸的特性:强氧化性、吸水性、脱水性1重要硫酸盐的性质及SO 24 的检验;2难点聚焦1.利用硫酸的强酸性制备多种物质:( 1 )制气体:制氢气Zn+H 2SO 4ZnSO 4+H 2;制 H2S :FeS+H 2SO 4H2 S+FeSO 4(2) 制较弱的酸:制 H3 PO 4 ;Ca 3(PO 4)2+3H 2 SO 4 (浓 )2H 3PO 4+2CaSO 4制 CH 3COOH :2CH 3 COONa+H 2 SO 42CH 3COOH+Na 2SO 4(3) 制化肥:Ca 3 (PO 4)2+2H 2 SO 4 (浓 )Ca(H 2PO 4) 2+2CaSO 42NH 3+H 2 SO 4 =(NH 4 )2 SO4(4) 制硫酸盐:制胆矾: CuO+H 2SO 4+4H 2 OCaSO 45H 2O( 晶体 )制绿矾: Fe+H 2SO 4FeSO 4+H 22.利用 H2 SO 4 高沸点性制取易挥发性酸。( 1)制 HF : CaF 2+H 2 SO4 (浓 )2HF +CaSO 4 (铅皿中 )微热( 2
2、)制 HCl : NaCl (固) +H 2SO 4(浓)NaHSO 4 +HCl 强热NaHSO 4 +NaClNa 2 SO 4+HCl 微热( 3)制 HNO 3: NaNO 3+H 2SO 4(浓)HNO 3+NaHSO 43.利用硫酸的稳定性制不稳定性酸。Na 2SO 3+H 2SO 4Na 2 SO 4 +H2 O+SO 24.利用浓 H2 SO 4 的强氧化性制取SO 2Cu+2H 2SO 4(浓 )CuSO 4+SO 2 +2H 2O5.利用浓 H2 SO 4 的脱水性:1浓 H 2SO4( 1)制 C2H4: CH 3CH 2OHCH 2CH 2+H 2O170 C浓H SO24( 2)制 CO :HCOOHCO +H 2O稀H SO246.利用浓 H2 SO 4 的吸水性做干燥剂。干燥: O2 、H 2、 Cl 2 、N 2、CO 、 CO 2、 SO 2不干燥:碱性:NH 3还原性: H 2S、 HI 、HBr7.用 H2SO 4 作催化剂:浓H SO24( 1)乙烯水化: CH 2 CH 2 +H 2 OCH 3CH 2OH2. 浓硫酸( 1 )物理性质:无色油
3、状液体,常见的浓硫酸质量分数为98.3% ,沸点为338 ,高沸点难挥发性。思考:浓硫酸的稀释方法。( 2 )化学性质: 吸水性(干燥剂)三种形式:与水任意比例混溶,溶于水剧烈放热。吸收气体中水蒸气(作为干燥剂,不能干燥硫化氢、溴化氢、碘化氢、氨气)与结晶水合物反应。实验:浓硫酸与胆矾反应,由胆矾蓝色变为白色说明浓硫酸有吸水性。 脱水性(炭化)实验 6 3 :潮湿的纸屑、棉花、木屑中分别滴入几滴浓硫酸。现象:三种物质都发生了变化,生成了黑色的炭。实验 6 4 :在 200mL 烧杯中放入20g 蔗糖,加入几滴水,搅拌均匀。然后再加入15mL 溶质的质量分数为 98% 的浓硫酸,迅速搅拌。观察实验现象。2现象:蔗糖逐渐变黑,体积膨胀,形成疏松多孔的海绵状的炭。说明:脱水性是浓硫酸的性质,而非稀硫酸的性质,即浓硫酸有脱水性。脱水性是浓硫酸的化学特性,物质被浓硫酸脱水的过程是化学变化的过程。反应时, 浓硫酸按水分子中氢、氧原子数的比为2 : 1夺取有机物中的氢原子和氧原子。可被浓硫酸脱水的物质一般为含氢、氧元素的有机物,其中蔗糖、木屑、纸屑和棉花等物质被子脱水后生成了黑色的炭(炭化)。 强氧
《考点19、硫酸及其盐》由会员M****1分享,可在线阅读,更多相关《考点19、硫酸及其盐》请在金锄头文库上搜索。

德运之争与辽金王朝的正统性问题 附辽朝对正统含义的选择和利用

岁月依一抹浅香于心间

五年级上信息技术教案-多彩的信息世界_天津版

全国土地利用总体规划纲要

职场礼仪_酒桌上与领导喝酒的学问
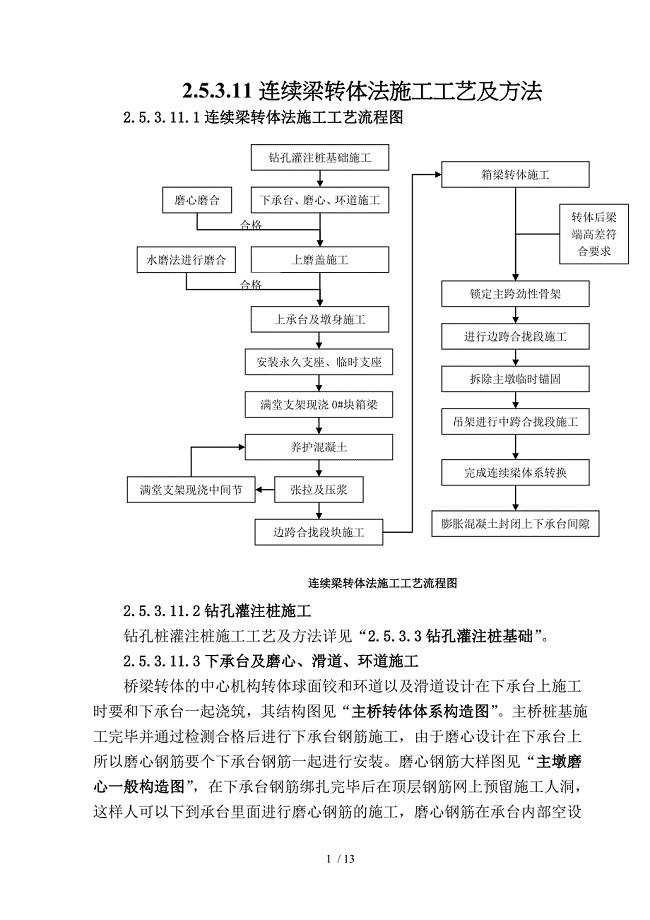
连续梁转体法施工工艺及方法

八年级物理上册-声现象-三声音的特性教案-人教新课标版
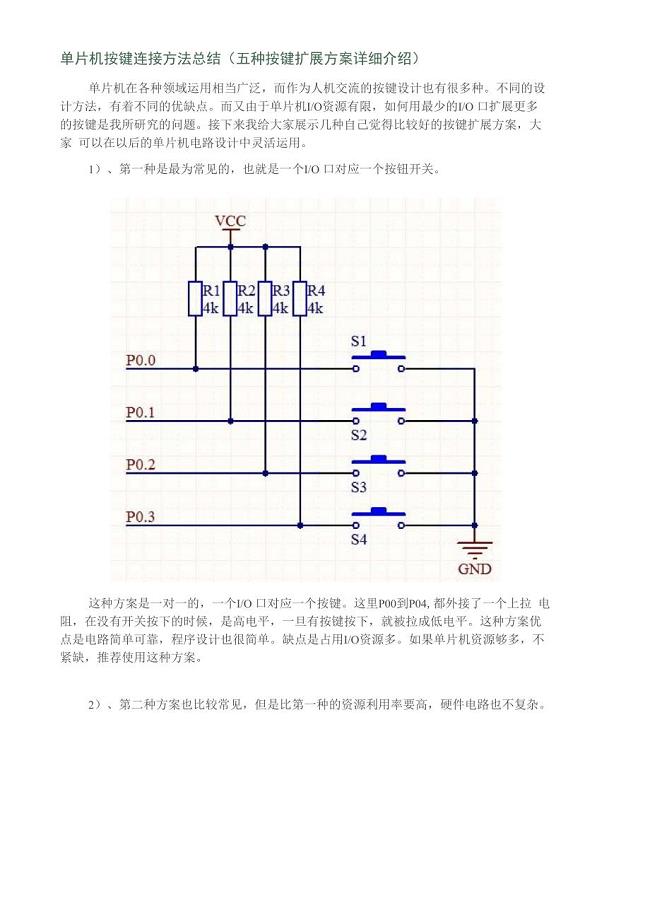
单片机按键连接方法

上半年工作总结及下半年工作计划2023年(3篇).doc

2022年年度工作总结通用10篇

校园国庆活动策划案.doc

Android_ics_stagefright框架数据流向分析

培训机构生源转让协议书格式版(五篇).doc

某地区渔业存在问题及发展思路

2013年高考数学总复习 第八章 第3课时 平面的基本性质及两直线位置关系随堂检测(含解析) 新人教版

六年级上册语文《回顾·拓展三》教案

一个很特别的人

教师年度考核个人总结报告范本(四篇).doc

数学教研组工作计划(10篇)

福建省2019年中考语文模拟试卷
 2023年个人工作总结范文个人工作总结_个人工作总结范文
2023年个人工作总结范文个人工作总结_个人工作总结范文
2022-11-08 9页
 项目采购管理的实践与探讨
项目采购管理的实践与探讨
2022-12-28 19页
 老师节表彰大会发言稿汇总五篇
老师节表彰大会发言稿汇总五篇
2023-06-25 4页
 人力资源部门个人工作计划格式范本(三篇).doc
人力资源部门个人工作计划格式范本(三篇).doc
2022-10-02 12页
 《卖火柴的小女孩》词语解释
《卖火柴的小女孩》词语解释
2023-03-29 3页
 小区物业工作计划安排(四篇)
小区物业工作计划安排(四篇)
2023-02-05 7页
 岁月依一抹浅香于心间
岁月依一抹浅香于心间
2023-07-25 5页
 创业孵化服务中心运营实施方案
创业孵化服务中心运营实施方案
2023-04-12 46页
 乡村规划师上半年工作个人工作总结
乡村规划师上半年工作个人工作总结
2023-08-13 4页
 2022部队士兵半年总结
2022部队士兵半年总结
2023-06-17 14页

