
从理想气体看真实气体的相变
7页1、从理佩扎体看夷變九体的相麦一、理想气体液体密度的数屋级为lg / cm3 = lOOOkg/m?,气体密度的数量级为lkg/m3,前者是后考的1000倍,或者说,同样数最的气体分子占用的体枳是液体体枳的1000倍,因 此物质在气态时分子间的平均距离是液态时的贩6 = 10倍。在液体中分子之间的距离不可能小于英直径,从而气体分子之间的距离比其直径大得多。 由于分子间的相互作用随距离递减很明显,所以在这样人的距离上分子间作用人町忽略。 只有在两个分子偶尔相遇的短暂时间里,强大的斥力才起作用,改变了它们各自的运动 状态之后,使它们再度分开。我们把分子之间的这种邂逅过程形容为“碰撞”(包括气 体内分子之间和气体分子与容器壁分子之间的碰撞)。在两次碰撞之间,由于惯性,分 子将做直线运动。我们还假定分子间的碰撞是完全弹性的,即平动动能不向内部自由度 (如转动、振动、激发等)转移。有了以上假设,我们就为气体设置了一个微观模型,归纳起來,此模型有以下几个要点:(1分子本身的大小比起它们之间的平均距离可忽略不计;(2)除了短暂的碰撞过程外,分子间的柑互作用可以忽略:(3)分子间的碰撞是完全弹性的。我们将
2、这样的气体叫做理想气体二、理想气体状态方程根据以上假设,并结合力学知识,我们可以得到以下方程:pV =厢,这就是理想气 体状态方程,其中p为气体压强,V为体积,V为气体物质的量,T为气体的热力学温 度,R为一普适常量,称为普适气体常量。(具体推导过程可参见有关热学教材) 对理想气体状态方程的修正一van der Waals物态方程在推导理想气体状态方程的时候,我们儿乎把分子力完全忽略了,但是在实际情况中分 子力的作用还是有一定影响的。不过,由于气体中分子力的效应毕竟比较小,我们町以 将它作为理想气体模型的修正來处理。分子力的作用表现在体积和压强两个方面。先看它对体积的影响。分子力由短程斥力和较长程的引力组成,分子力対气体体枳的影 响主要在前者。形象的说,由于排斥力的存在,分子相当于一个个貝仃 疋V径的小球, 在小球占有的体枳内,其它分子是无法侵入的,所以应该从理想气体状态方程中的体积 项V中扣除这部分体积,由于这部分体枳正比于气体分子数冃,亦即正比于气体物质的 量V o于是将理想气体状态方程中的V换成V7 b,其中b是每个气体分子在一定范闱 (指其余气体分子无法进入的范圉)内的体枳,这
3、样修正后的体枳VT b就是每个分子 在考察范围内能够自有活动的体积。我们再看压强的修正。一般来说,压强有来自分子运动和分子力两部分的贡献,前者叫 做动理压强,记作R后者代衷(体的内聚力,称为内压强,记作Pu。分子力对压强的 影响主要在于较为长程的吸引力部分。对于处在气体内部的一个分子,周闱分子给它的 吸引力平均说来抵消了,从而刘它的自由E行不产生影晌,只要将体枳修正项考虑进去,则pV =跖式对描述戸斤依然是付效的,即现在来看,它来自假想截面AS两侧附近分子之间的吸引力。从最纲上看斥强和能最密度(单位体枳内的能量)是一样的,用位力法町以证明,p口正比于分子间相互作用 势能密度U而U又正比于施力者的数密度和受力者的数密度.故正比于分子数密度1/*的平方。分子数密度正比于摩尔数V,反比于体积V,故 OC才,作为吸引势Pu足 负的,它可以写成_ i/2aP尸一時把以上两部分加起来,就得到气体中的压强或(p +(V 优)=vRT.(*)(*)式称为范德瓦尔斯(van der Waals)物态方程三、气液相变在描述实际(体的状态方面,van der Waals方程虽在数值上不尽准确,但它是一个非
《从理想气体看真实气体的相变》由会员枫**分享,可在线阅读,更多相关《从理想气体看真实气体的相变》请在金锄头文库上搜索。

建筑安全生产标准化示范工地评价标准

西安交通大学22春《电算化会计》离线作业二及答案参考62

ENVI采集地类波谱对比

福建师范大学21秋《通信原理》在线作业三满分答案90

班主任工作总结安全教育(三篇).doc

文明礼仪中期报告

【好习惯】好习惯让同学成就最好的自己

算法工程师岗位的职责表述(4篇)

燃气和电气设备的检查管理制度(三篇).doc
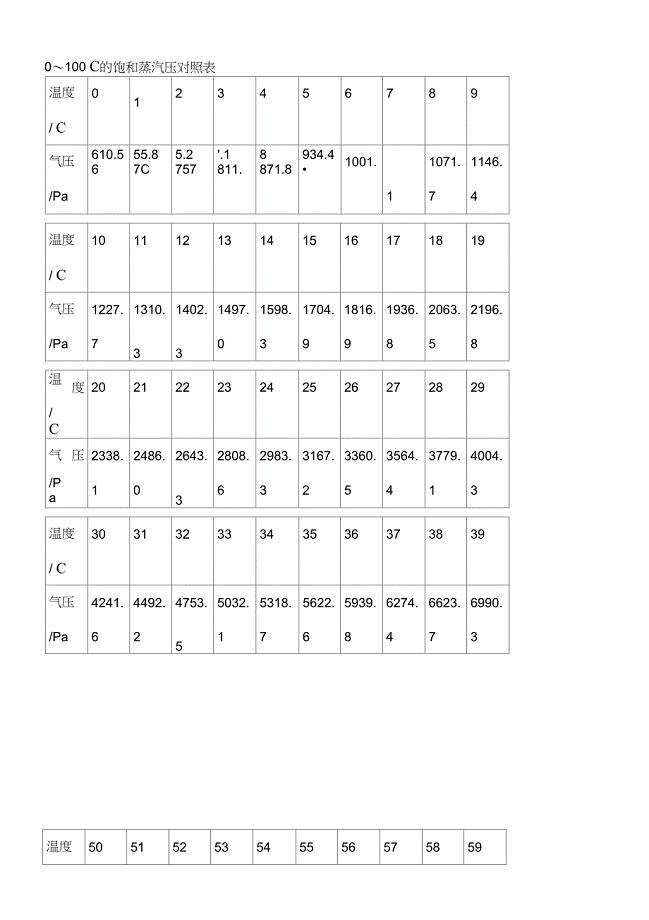
温度和水蒸汽分压对照表

asp制作用户登陆界面

行政管理专业自我鉴定

低碳生活调查报告

幼儿园中班班级安全计划范文(四篇).doc

精选公司前台下半年工作计划B

建筑装饰作业安全施工作业票

2022公司文秘工作总结范文3篇(文秘工作总结年)

ERP中的财务管理集成

学期体育教研工作计划样本(二篇).doc

学生成长档案 (2)
 运用联想丰富写作范文
运用联想丰富写作范文
2023-10-28 4页
 重庆关于成立高性能纤维及复合材料公司可行性研究报告_模板范文
重庆关于成立高性能纤维及复合材料公司可行性研究报告_模板范文
2024-02-04 109页
 湖南中级职称考试给排水实务
湖南中级职称考试给排水实务
2023-01-30 31页
 志愿者社会实践论文大学生实践3000字
志愿者社会实践论文大学生实践3000字
2023-03-28 11页
 短小品搞笑大全剧本
短小品搞笑大全剧本
2022-12-26 7页
 2022年关于实践报告的格式报告
2022年关于实践报告的格式报告
2023-05-01 12页
 有关单位犯罪不应成为对直接责任人减轻处罚的借口
有关单位犯罪不应成为对直接责任人减轻处罚的借口
2023-01-15 7页
 “青春有约 走进军营”主题活动策划书
“青春有约 走进军营”主题活动策划书
2022-12-05 3页
 蔬菜基地建设规划方案模板(二篇)
蔬菜基地建设规划方案模板(二篇)
2023-09-01 9页
 建筑安全生产标准化示范工地评价标准
建筑安全生产标准化示范工地评价标准
2023-05-03 69页

