
高三下学期第三次质量检测化学试卷(含答案)
20页1、高三下学期第三次质量检测化学试卷(含答案)(考试时间:75分钟 试卷满分:100分)学校:_班级:_姓名:_考号:_注意事项考生在答题前请认真阅读本注意事项及各题答题要求:1.本试卷共8页,满分为100分,考试时间为75分钟。考试结束后,请将本试卷和答题卡一并交回。2.答题前,请务必将自己的姓名、准考证号用0.5毫米黑色墨水的签字笔填写在试卷及答题卡的规定位置。3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮擦干净后,再选涂其他答案。作答非选择题,必须用0.5毫米黑色墨水的签字笔在答题卡上的指定位置作答,在其他位置作答一律无效。5.如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。可能用到的相对原子质量:一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。1. 材料科学是一门与工程技术密不可分的应用科学。下列有关相关物质的材料的说法,正确的一项是A. 石墨烯和石墨炔都是新型的有机高分子材料B. 太阳能电池板的核心材料是晶体硅,属于无机非金属
2、材料C. “特氟龙”的主要成分聚四氟乙烯的单体属于烃类D. 高压电线的制造主要使用金属铝而不使用铜的原因是铝的导电性更好且密度更低【答案】B【解析】【详解】A石墨烯和石墨炔都是碳的单质,故属于新型的无机非金属材料,A错误;B硅是一种良好半导体材料,太阳能电池板的核心材料是晶体硅,属于无机非金属材料,B正确;C“特氟龙”的主要成分聚四氟乙烯的单体为:CF2=CF2,其不属于烃类而是烃的衍生物,卤代烃,C错误;D高压电线的制造主要使用金属铝而不使用铜的原因,是铝表面能够形成一层致密的氧化物保护膜而耐腐蚀,并不是利用其导电性更好且密度更低,D错误;故答案为:B。2. 利用反应可制备水煤气,下列有关说法正确的是A. 是极性分子,因此在水中的溶解度较大B. 一个分子中只含有一个配位键C. 的电子式为D. 比较稳定的原因是可以形成分子间氢键【答案】B【解析】【详解】AH2为非极性分子,H2O为极性分子,根据“相似相溶”的原理,H2难溶于水,A项错误;BCO分子中含1个键和2个键,其中1个键是由O原子提供孤电子对,C原子提供空轨道,通过配位键形成的,B项正确;CH2O的电子式为,C项错误;DH2O比
3、较稳定是因为H-O键键能较大,键比较牢固不易断裂,而分子间氢键主要影响的是水的熔沸点,D项错误;故选B。3. 2022年9月9日,国家航天局、国家原子能机构联合发布:我国科学家在嫦娥五号月壤样品中发现一种新矿物,命名为“嫦娥石”,英文名称为。嫦娥石是一种磷酸盐矿,属于陨磷钠镁钙石族。理想组成为,下列说法正确的是A. 电负性大小:B. 第一电离能大小:C. 碱性强弱:D. 半径大小:【答案】A【解析】【详解】A同周期元素从左到右电负性增大,同主族元素从上到下电负性减小,电负性大小:,故A正确;B同周期元素随着核电荷数增大第一电离能整体呈现增大趋势,第一电离能大小:,故B错误;C同主族元素随着核电荷数增大金属性增强,对应最高价氧化物水化物碱性增强,碱性强弱:,故C错误;D氧负离子和镁离子的核外电子排布相同,O的核电荷数小,半径更大,故D错误;故选A。4. 实验室用如下图所示装置探究与溶液的反应(实验前先通入排除装置中的空气)。下列说法不正确的是A. 用装置甲产生B. 装置乙中无明显现象,则与未发生反应C. 装置丙中注入,产生红棕色气体,说明装置乙中发生了氧化反应D. 装置丁吸收尾气并防止空
4、气进入装置丙【答案】B【解析】【分析】甲为二氧化硫发生装置,乙为二氧化硫与硝酸钠的反应装置,反应生成NO进入丙,但是整个过程没有明显现象,因此只能通过向丙中通入氧气,看是否有红棕色气体生成,来确定乙中是否发生反应。【详解】A 甲为二氧化硫的发生装置,方程式为H2SO4+Na2SO3=Na2SO4+SO2+H2O,A正确;B由于生成NO为无色无味气体,故该其反应没有明显现象,B错误;C注入氧气,产生红棕色气体,说明装置丙中有NO,进一步证明乙中发生了反应,C正确;D 丁做尾气处理,并且防止空气进入丙,D正确;故选B。5. 一种重要有机中间体的合成路线如下,下列说法中正确的是A. 物质丙分子式为B. 物质甲可以发生氧化、取代、水解和消去反应C. 图示反应类型为加成反应D. 物质乙中的原子不可能处于同一平面【答案】D【解析】【详解】A由物质丙的结构简式可知,其分子式为C14H12Br2,A项错误;B甲分子苯环上含碳溴键,但与溴原子相连的碳原子的邻位碳原子上没有H原子,不能发生消去反应,B项错误;C由合成路线可知,甲和乙反应除生成丙之外,还其他产物生成,该反应不是加成反应,C项错误;D乙分子结
《高三下学期第三次质量检测化学试卷(含答案)》由会员夏***分享,可在线阅读,更多相关《高三下学期第三次质量检测化学试卷(含答案)》请在金锄头文库上搜索。
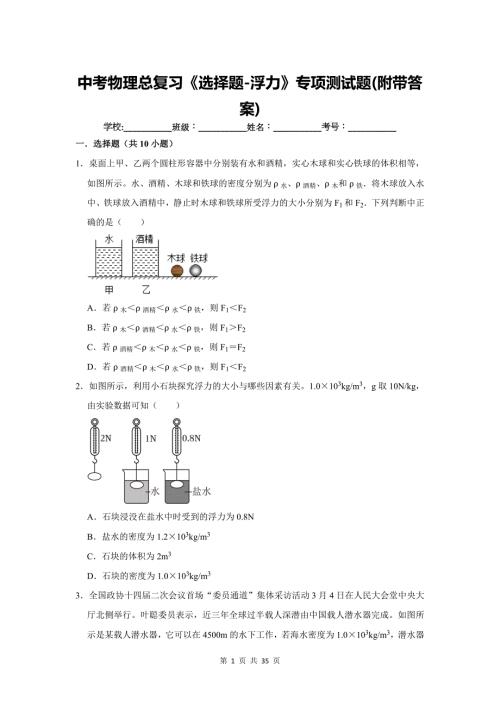
中考物理总复习《选择题-浮力》专项测试题(附带答案)
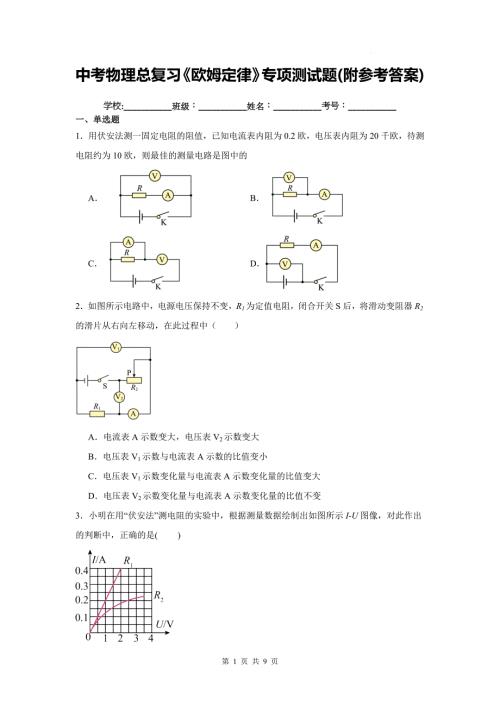
中考物理总复习《欧姆定律》专项测试题(附参考答案)

中考物理总复习《透镜及其应用》专项测试题(含参考答案)

中考物理总复习《物态变化》专项测试题(含有参考答案)

高考物理《模型方法-动态平衡》专题解析-带答案

中考物理总复习《电流和电路》专项测试题(附带答案)

中考物理总复习《电磁学多选》专项测试题(附带答案)

中考物理总复习《电功率》专项测试题(附带答案)

中考物理总复习《压强》专项测试题(含参考答案)

中考物理总复习《物态变化》专项测试题(有参考答案)

中考物理总复习《动态电路分析》专项测试题(附带答案)

中考物理总复习《电功率》专项测试题(附带答案)

中考物理总复习《声现象》专项测试题(附带答案)

中考物理总复习《选择题-电能和电功率》专项测试题(附带答案)

山东省高三下学期第三次高考模拟考试语文试卷及答案解析

中考物理总复习《电流和电路》专项测试题(带答案)
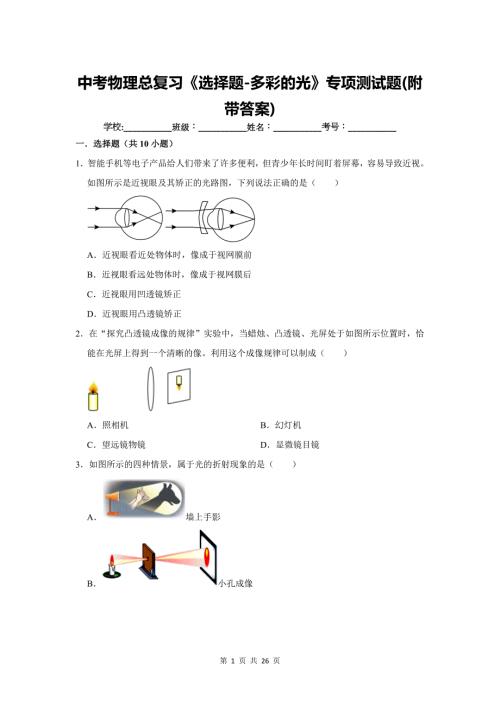
中考物理总复习《选择题-多彩的光》专项测试题(附带答案)

中考物理总复习《机械运动》专项测试题(附带答案)

中考物理总复习《运动和力》专项测试题(附带答案)

中考物理总复习《内能-内能的利用》专项测试题(附带答案)
 高考地理二轮优选习题专题五人口与城市专题整合名师优质学案
高考地理二轮优选习题专题五人口与城市专题整合名师优质学案
2023-01-27 4页
 2022年高考英语一轮复习 Unit 9 Wheels课时练 北师大版必修3
2022年高考英语一轮复习 Unit 9 Wheels课时练 北师大版必修3
2022-12-15 12页
 2022年高中地理课后知能检测第1章环境与环境问题第2节环境问题概述湘教版
2022年高中地理课后知能检测第1章环境与环境问题第2节环境问题概述湘教版
2023-04-09 5页
 高考地理一轮复习 12.2 世界地理分区(含解析)湘教版
高考地理一轮复习 12.2 世界地理分区(含解析)湘教版
2022-10-08 5页
 唐山学大教育高考考点解析课程
唐山学大教育高考考点解析课程
2023-07-18 3页
 安徽省滁州市定远县育才学校2019-2020学年高一化学上学期期末考试试题实验班
安徽省滁州市定远县育才学校2019-2020学年高一化学上学期期末考试试题实验班
2022-08-28 9页
 2021版高考物理一轮复习第一章质点的直线运动2匀变速直线运动规律创新练1含解析
2021版高考物理一轮复习第一章质点的直线运动2匀变速直线运动规律创新练1含解析
2023-01-24 3页
 高三上学期第三次调研考试生物试题 含答案
高三上学期第三次调研考试生物试题 含答案
2023-11-01 13页
 河南省鹤壁市淇滨高级中学2017-2018学年高一数学3月月考试题
河南省鹤壁市淇滨高级中学2017-2018学年高一数学3月月考试题
2022-09-02 5页
 WIFI模块UART协议
WIFI模块UART协议
2022-11-01 8页

