
研究生入学考试物理化学复习资料
59页1、研究生入学考试物理化学复习资料 第一章 热力学第一定律一、 选择题1凡是在孤立体系中进行的变化,其U和H的值一定是 (a) U 0 , H 0 (b) U = 0 , H = 0 (c) U 0 , H 0 (d) U = 0 , H大于、小于或等于零不确定 (答案) d (H=U+D(pV) =U+ V D p )2. 指出下列过程中的可逆过程(a) 摩擦生热(b) 室温、标准压力下一杯水蒸发为同温同压下的汽(c) 373K,标准压力下一杯水蒸发为汽(d) 手电筒中干电池放电使灯泡发亮 (答案) c (可逆过程有如下特点:状态变化时推动力与阻力相差无限小,系统与环境始终无限接近于平衡态;过程中的任何一个中间态都可以从正、逆两个方向到达;系统经过一个循环后,系统和环境均恢复原态,变化过程中无任何耗散效应;在相同的始、终态间,恒温可逆过程系统对环境作最大功,环境对系统作最小功;由于状态变化时推动力与阻力相差无限小,所以完成过程所需时间为无限长。具体说来:在某一温度及与该温度对应的平衡压力下发生的相变化;内、外温差相差dT的传热过程;内、外压差相差dp的膨胀或压缩过程;通过的电流为dI的充
2、电或放电过程等都可看作是可逆过程)3. 将某理想气体从温度T1加热到T2。若此变化为非恒压过程,则其焓变H应为何值? (a) H=0 (b) H=Cp(T2-T1) (c) H不存在 (d) H等于其它值 (答案) b(对理想气体,反之亦然。 对理想气体,在计算时,只要是简单的pVT变化,即使不是恒容过程,仍可用式或计算热力学能的变化, 因为理想气体,仅是温度的函数,恒容与否对并无影响。 同理,对理想气体,反之亦然。 对理想气体,在计算时,只要是简单的pVT变化,即使不恒压过程,仍可用式或计算焓的变化, 因为理想气体,仅是温度的函数,恒容与否对并无影响。)同理,对理想气体,反之亦然。例如:. 当理想气体冲入一真空绝热容器后,其温度将 (a) 升高 (b) 降低(c) 不变 (d) 难以确定 (答案)c (U=Q+W, p外=0 , W=0 ,又绝热 ,所以U)因为是真空故不做功,又因为是绝热故无热交换,故U0。温度不变。此外,理想气体的自由膨胀过程,同样有 绝热 ,p外=0 , W=0 所以U温度不变 温度不变. 理想气体自由膨胀过程中(a). W = 0,Q0,DU0,DH=0 (b
《研究生入学考试物理化学复习资料》由会员cn****1分享,可在线阅读,更多相关《研究生入学考试物理化学复习资料》请在金锄头文库上搜索。

2023年行政人员的辞职报告集锦八篇.docx

鸡群常见拉稀性疾病的鉴别要点.doc

歌曲《蜗牛与黄鹂鸟》教案.docx

2023年农村三资代理服务工作汇报.docx

儿童心理问题个案分析及干预.doc

(XX电站)增效扩容改造工程建设管理工作报告.doc

洁丰干洗店加盟流程和优势.doc

2016年造价工程师考试《案例分析》:工程索赔分类考试题.docx

红楼梦的读书心得集锦15篇

山东潍坊诸城0809九年级上期末考试试卷

中国知名企业形象广告语.doc

2022年教育学心理学(小学)专业教师资格证考试考试试题+答案卷8

最新行政能力倾向测试常识300题及答案(2).doc

新闻要素在故事化过程中的变形.docx

二级Java练习及解析.doc

保洁合同范文六篇

消防官兵体能训练内容与方法

紫外线诱变育种
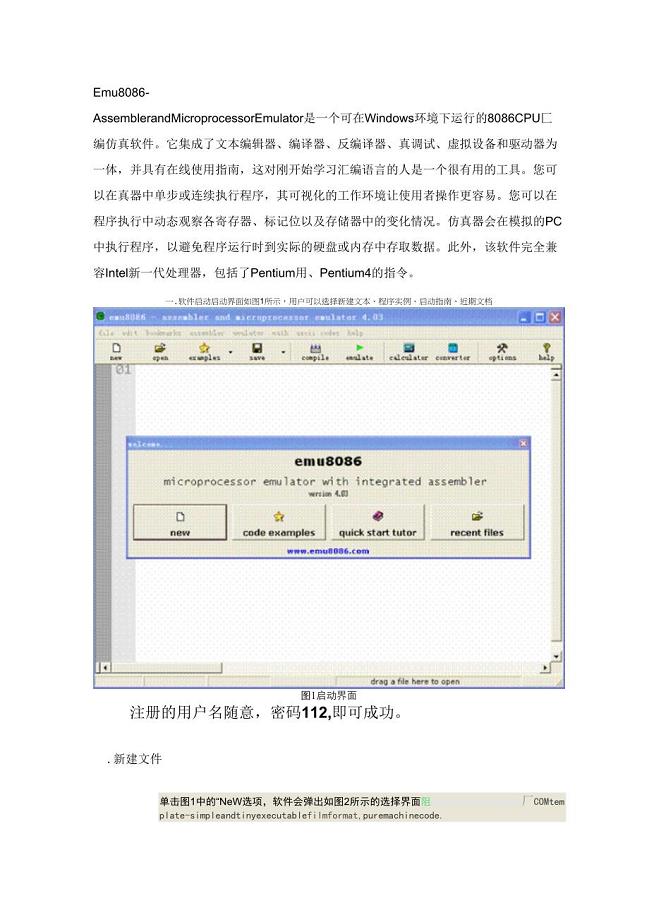
Emu8086仿真软件使用方法

信用管理体系认证提交资料清单.doc
 基于岩石地质本质性的碳酸盐岩单轴抗压强度预测.docx
基于岩石地质本质性的碳酸盐岩单轴抗压强度预测.docx
2023-01-28 5页
 概预算应用于工程造价中的必要性分析
概预算应用于工程造价中的必要性分析
2023-06-06 3页
 北师大版小学一年级上册数学期中考试试卷共6套
北师大版小学一年级上册数学期中考试试卷共6套
2023-03-05 25页
 现代测绘技术的应用与发展
现代测绘技术的应用与发展
2023-02-04 4页
 浅析林业企业财务风险预警系统管理问题及对策
浅析林业企业财务风险预警系统管理问题及对策
2024-02-14 5页
 刊水泥稳定碎石基层要求
刊水泥稳定碎石基层要求
2024-03-01 4页
 数字经济下创新要素综合配置与产业结构调整
数字经济下创新要素综合配置与产业结构调整
2022-10-25 3页
 电子商务专业毕业论文大纲.doc
电子商务专业毕业论文大纲.doc
2024-01-10 8页
 餐饮企业安全生产事故隐患排查和治理制度
餐饮企业安全生产事故隐患排查和治理制度
2024-01-10 3页
 公路工程造价与设计变更的控制
公路工程造价与设计变更的控制
2024-02-04 5页

