
九年级化学酸碱盐
11页1、初 三 化 学 自 学 案课题常见的酸学习目标1.知道盐酸、硫酸的主要性质和用途;2.认识浓硫酸的腐蚀性和稀释方法;3.掌握酸的化学性质,知道酸具有相似化学性质的原因。重点掌握酸的化学性质,知道酸具有相似化学性质的原因。难点掌握酸的化学性质,知道酸具有相似化学性质的原因。学 习 内 容补充:什么是酸碱盐总结:1:溶液导电的内因是因为溶液中存在: 2:溶液呈电中性的原因:能导电的溶液中, 一:酸碱盐的定义:1、酸: 2、碱: 3、盐: 铵根离子与金属离子相似,看作为金属离子,所以NH4Cl 练习:1、判断下列物质哪些是酸?哪些是碱?哪些是盐?H2O O2 HCl K2MnO4 MnO2 H2SO4 Ca(OH)2 Fe(OH)3 KNO3 SO3 KCl ZnCl2 NaOH NH3H2O NH4Cl NaHCO3 Cu2(OH)2CO3酸: 碱: 盐: 2、下列物质中,含有可以自由移动的氯离子的是( )A.HCl气体 B.NaCl晶体 C.KCl溶液 D.KNO3溶液3、下列化合物中不属于碱类的是( )A.氢氧化钡 Ba(OH)2 B.纯碱 Na2CO3 C.酒精 C2H5OH D.氢
2、氧化钾 KOH4、写出下列反应的化学方程式,并判断物质的所属类别(金属单质、非金属单质、氧化物、酸、碱、盐)(1)锌与稀硫酸(2)碳酸钙与稀盐酸(3)分解高锰酸钾(4)二氧化碳通入澄清石灰水中(5)一氧化碳还原氧化铁6、含有下列离子的溶液中,溶质全部为酸的是 ( ) AH、Na、SO42 BH、Cl、NO3 COH、K、Ba2 DAg、K、NO3知识点一:常见的酸浓盐酸、浓硫酸的物理性质、特性及用途:浓盐酸 浓硫酸颜色、状态打开瓶盖现象原因气味敞口久置质量及c%原因用途浓硫酸的特性:脱水性:能够将纸张、木材、布料、皮肤里氢、氧元素按水的组成比夺去,使它们脱水生成黑色的炭,发生炭化。(思考:脱水性是什么性质?) :浓硫酸跟空气接触,能够 空气里的水分,可用作某些气体的 。强烈的 。强氧化性:与金属反应时一般不生成氢气,而生成水。浓硫酸的稀释:稀释浓硫酸时,应将 其沿杯壁慢慢倒入 中,且边倒边搅拌。而不能把 往 里倒,以免水沸腾将硫酸带出,造成危险。(因为硫酸溶于水时放出大量的热)万一浓硫酸洒在皮肤上,请立即 ,然后涂3%-5%的 溶液。巧学妙记:浓硫酸的稀释:“酸入水,沿内壁,慢慢倒,不
《九年级化学酸碱盐》由会员大米分享,可在线阅读,更多相关《九年级化学酸碱盐》请在金锄头文库上搜索。

煤层气排采制度分析

混合肥料项目申请报告写作参考模板

精品人教版七年级上册128课“读一读写一写”汇编

花生种植技术0001

职业经理人聘任协议书.docx

2023年《影》的水墨光影.docx

初三下学期班级工作计划样本(六篇)

2021年广东省普通高中学业水平选择性考试(广东卷)及答案

2019-2020学年高中政治第一单元文化与生活第二课文化对人的影响第2框文化塑造人生随堂达标验收含.doc

工厂个人年终工作总结.doc

中央广播电视大学开放专科市场营销学课程期末考试历年试题及答案精编汇总推荐

我和李钧老师的故事

鞍山半导体材料设计项目实施方案

发展改革系统民主评议政风行风工作实施方案_1.docx
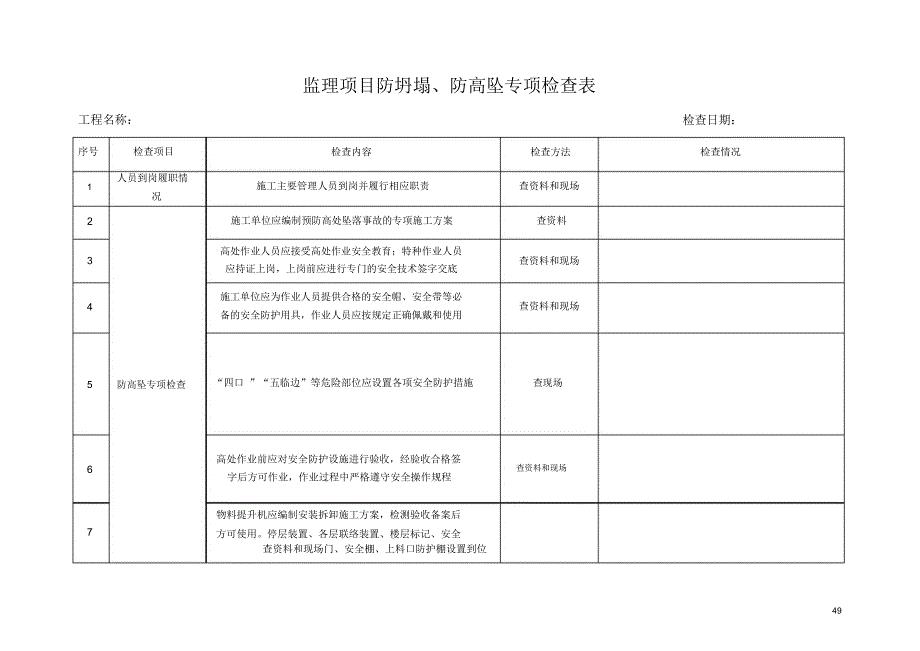
监理项目防坍塌防高坠专项检查表

中国地质大学21春《信息资源管理》在线作业二满分答案_67

怎样提升低段学生计算的正确率 怎样提升低段学生处理问题的能力
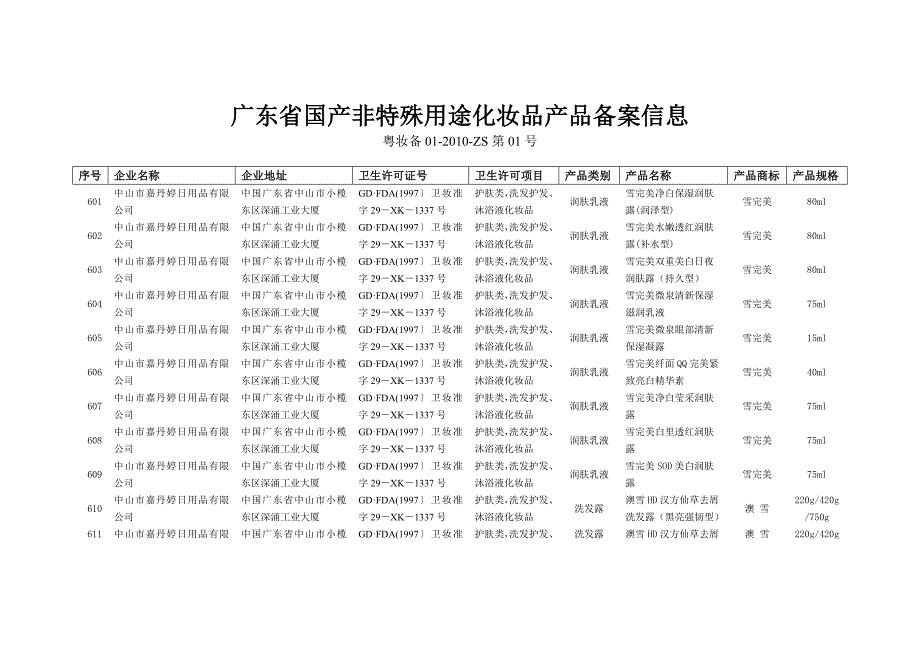
广东省国产非特殊用途化妆品产品备案信息29880.doc

五年级英语日常交际用语80句

2023年大数据时代企业管理会计的应用探析.docx
 2021安全月活动上的领导讲话稿
2021安全月活动上的领导讲话稿
2023-10-04 6页
 电大中级财务形考任务一
电大中级财务形考任务一
2023-01-27 2页
 浙江省绍兴市九年级上学期科学期末学业成绩调测试卷及答案.docx
浙江省绍兴市九年级上学期科学期末学业成绩调测试卷及答案.docx
2022-09-11 21页
 冲床车间预防事故预案
冲床车间预防事故预案
2023-08-15 4页
 初中后进学生评语
初中后进学生评语
2022-12-26 12页
 初中思想品德评语
初中思想品德评语
2024-02-13 12页
 第二十五章概率初步章末测评
第二十五章概率初步章末测评
2023-12-16 4页
 插齿机安全技术操作规程
插齿机安全技术操作规程
2023-03-18 1页
 教学模式的几点思考
教学模式的几点思考
2022-07-27 3页
 高中物理课堂教学中的创新教育
高中物理课堂教学中的创新教育
2023-11-20 4页

