
全国高考化学氧化还原反应的综合高考真题汇总
27页1、全国高考化学氧化还原反应的综合高考真题汇总一、高中化学氧化还原反应1阳极泥处理后的沉渣中含AgCl,工业上可用Na2SO3溶液作浸取剂浸出回收。某小组在实验室模拟该过程。已知:i25oC时,部分物质的溶解度:AgCl 1.9104 g;Ag2SO3 4.6104 g;Ag2SO40.84 g。ii25oC时,亚硫酸钠溶液酸化过中含微粒的物质的量分数随pH变化如图所示。.浸出氯化银取AgCl固体,加入1 mol/L Na2SO3溶液作浸取剂,充分反应后过滤得到浸出液(pH=8),该过程中发生的反应为AgCl + Ag(SO3)23 + Cl。(1)用平衡移动原理解释AgCl溶解的原因是_。. 酸化沉银(2)经检测,沉淀m为AgCl,则溶液m中含微粒的主要存在形式是_。(3)探究沉淀n的成分。甲同学认为沉淀n一定不含Ag2SO4,其依据是_。乙同学认为沉淀n可能含Ag2SO3,进行实验验证。i. 本实验设计的依据是:Ag2SO3具有_性。ii. 乙同学观察到_,得出结论“沉淀n不含Ag2SO3”。丙同学从溶液n的成分角度再次设计实验证明沉淀n不含Ag2SO3。i. 本实验设计的依据是:若沉
2、淀n含Ag2SO3,则溶液n中含微粒的总物质的量_(填“”、“”或“”)Cl物质的量。ii. 结合实验现象简述丙同学的推理过程:_。浸取剂再生(4)溶液m经处理后可再用于浸出AgCl,请简述该处理方法_。【答案】AgCl(s)Ag+(aq)+ Cl-(aq) ,Ag+与SO32- 结合生成Ag(SO3)23 ,促进AgCl的溶解平衡正向移动 HSO3- Ag2SO4的溶解度远大于AgCl或Ag2SO3,溶液中Ag+ 的浓度很小 还原 b中清液的颜色与c相同,均为浅紫色溶液 e中无沉淀生成,说明清液中没有Cl-,则溶液n中加入稀硝酸使Ag(SO3)23全部转化为Ag+,Ag+将Cl全部沉淀,由此可知溶液n中含Ag元素的微粒总物质的量不小于n(Cl) 加NaOH溶液调节pH至910 【解析】【分析】I、(1)利用平衡移动的知识答题即可;II、(2)生成沉淀m时,溶液m的pH为5,观察图像,可以得知HSO3-的物质的量分数占100%;(3)溶液中Ag+的浓度很小,而Ag2SO4的溶解度较大,故不会形成Ag2SO4沉淀;依据Ag2SO3的还原性答题;e中无沉淀生成,说明清液中没有Cl-,则溶液
3、n中加入稀硝酸使Ag(SO3)23全部转化为Ag+,Ag+将Cl全部沉淀,由此可分析出溶液n中含Ag元素的微粒总物质的量不小于n(Cl);III、(4)m溶液中的溶质为NaHSO3,浸取剂为Na2SO3溶液,需要加入NaOH溶液将NaHSO3转化为Na2SO3。【详解】I、(1)AgCl(s)Ag+(aq)+ Cl-(aq),Ag+与SO32- 结合生成Ag(SO3)23-,促进AgCl的溶解平衡正向移动;II、(2)生成沉淀m时,溶液m的pH为5,观察图像,可以得知HSO3-的物质的量分数占100%,则溶液m中含微粒的主要存在形式是HSO3-;(3)Ag2SO4的溶解度远大于AgCl或Ag2SO3,溶液中Ag+ 的浓度很小;i、酸性KMnO4溶液具有强氧化性,SO32-具有还原性,则该实验涉及的依据是Ag2SO3具有还原性;ii、沉淀中无Ag2SO3,则该沉淀不会使酸性KMnO4溶液褪色,故可以观察到a试管中酸性KMnO4溶液褪色,b、c试管中酸性KMnO4溶液依然呈紫色;e中无沉淀生成,说明清液中没有Cl-,则溶液n中加入稀硝酸使Ag(SO3)23全部转化为Ag+,Ag+将Cl全部
4、沉淀,由此可分析出溶液n中含Ag元素的微粒总物质的量不小于n(Cl);III、(4)m溶液中的溶质为NaHSO3,浸取剂为Na2SO3溶液,根据曲线图可知,加入NaOH溶液调整pH到9-10即可。2过硫酸钠(Na2S2O8)具有极强的氧化性,且不稳定,某化学兴趣小组探究过硫酸钠的相关性质,实验如下。已知SO3是无色易挥发的固体,熔点16.8,沸点44.8。(1)稳定性探究(装置如图):分解原理:2Na2S2O82Na2SO42SO3O2。此装置有明显错误之处,请改正:_,水槽冰水浴的目的是_;带火星的木条的现象_。(2)过硫酸钠在酸性环境下,在Ag的催化作用下可以把Mn2氧化为紫红色的离子,所得溶液加入BaCl2可以产生白色沉淀,该反应的离子方程式为_,该反应的氧化剂是_,氧化产物是_。(3)向上述溶液中加入足量的BaCl2,过滤后对沉淀进行洗涤的操作是_。(4)可用H2C2O4溶液滴定产生的紫红色离子,取20mL待测液,消耗0.1molL1的H2C2O4溶液30mL,则上述溶液中紫红色离子的浓度为_molL1,若Na2S2O8有剩余,则测得的紫红色离子浓度将_(填“偏高”“偏低”或“
《全国高考化学氧化还原反应的综合高考真题汇总》由会员hs****ma分享,可在线阅读,更多相关《全国高考化学氧化还原反应的综合高考真题汇总》请在金锄头文库上搜索。

2023年信息门户建设方案.docx

利通二小合唱队训练计划及实施方案.doc

春季学期英语组教研工作总结

2023年银行青年节演讲稿.docx

2007年10月自考国际贸易理论与实务试题17352.doc

2023大学生实习参考心得.docx

2023国旗下的讲话把握机会从现在开始参考讲话.docx

2023年档案局落实争先创优情况总结新编.docx

中国少儿足球注册各种表格

2023年学校科学发展观党性分析材料范文.doc

客房服务员中级操作技能考核.doc

自查自纠专题报告

新资源食品列表(2012更新).doc

一年级语文工作计划格式范文(二篇)
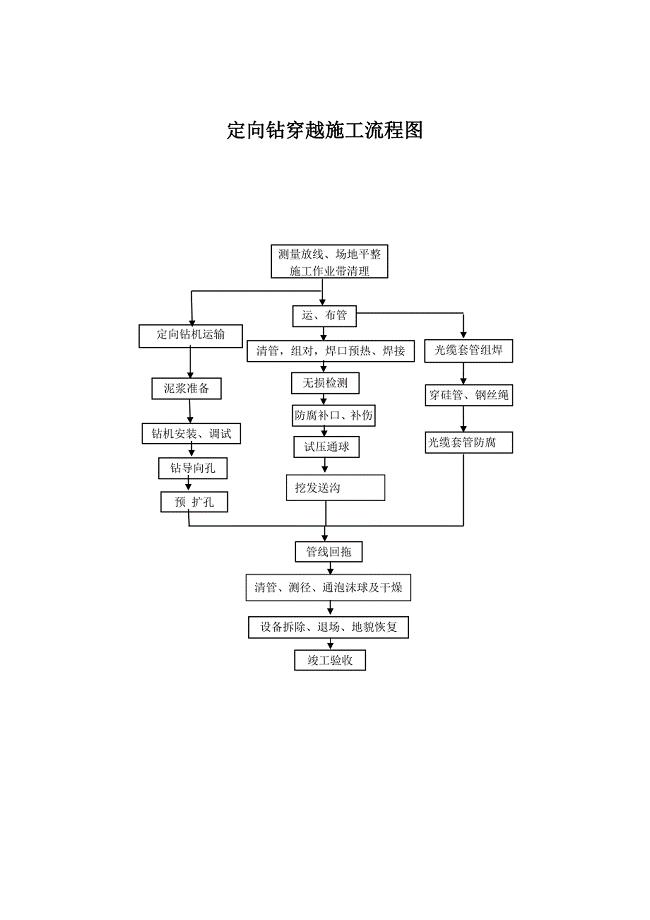
定向钻穿越施工流程图.docx

质量分数计算题

世说新语两则练习

中国 河南 郑州日照长度和太阳高度角表.doc

话术的定义与含义.doc

形式各样的障碍跑课的教学设计
 校园二手交易系统-需求规格说明书(共11页)
校园二手交易系统-需求规格说明书(共11页)
2022-10-07 11页
 乡镇安全生产工作计划
乡镇安全生产工作计划
2023-04-17 11页
 陡沟中心学校教师聘任制实施方案
陡沟中心学校教师聘任制实施方案
2023-05-22 4页
 毕业生-外文翻译之光催化方向资料
毕业生-外文翻译之光催化方向资料
2022-09-05 10页
 (物理一轮复习教案合集)示范高中高中物理一轮复习教案word文档
(物理一轮复习教案合集)示范高中高中物理一轮复习教案word文档
2023-02-18 646页
 医疗器械行业调查报告
医疗器械行业调查报告
2023-05-23 7页
 七年级疫情期间网上教学心得
七年级疫情期间网上教学心得
2023-09-02 2页
 群体性上访事件应急预案(共8页)
群体性上访事件应急预案(共8页)
2023-04-08 8页
 模板安装及支撑技术交底
模板安装及支撑技术交底
2023-02-05 14页
 上厦门市九年级质量检测化学试题及答案
上厦门市九年级质量检测化学试题及答案
2023-01-16 11页

