
高中化学竞赛试题
6页1、成都实外高2012级化学竞赛训练题(八)H1.008相对原子质量He4.003Li6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc98Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs132.9Ba137.3LaLuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po210At210
2、Rn222Fr223Ra226AcLaRfDbSgBhHsMtDs第第题(12分)14Ag8NaCN2H2OO24NaAg(CN)24NaOH Ag2S4NaCN2NaAg(CN)2Na2S Zn2NaAg(CN)2Na2Zn(CN)42Ag(各2分)2Al3Ag2S6H2O6Ag2Al(OH)33H2S(2分)34Au8CNO22H2O4Au(CN)24OHZn2Au(CN)2Zn(CN)422Au(各2分)题(12分)银以游离态单质银或以硫化矿的形式存在于自然界。无论以何种形式存在的银矿,都可用氰化钠溶液浸取,而获得银氰配合物的溶液,再在溶液中用锌还原即可得粗银。1试写出上述有关的三个配平的化学方程式。2银器使用日久逐渐变黑而失去美丽的外观。对变黑的银器多用抛光的方法使之恢复光泽,但这样黑绣中的银也随之损失掉。一种化学除银黑锈的简便方法是:含食盐的稀溶液于铝容器内,将变黑银器浸入溶液中,并使银器与铝容器接触,放置一段时间后,黑锈就会褪去,而银却极少损失。写出除锈的化学反应方程式。3金属金常常可以在铝硅酸盐岩石中发现,它很细地分散在其他矿物之中。从金矿中提取金,传统的且效率极高的方法
3、也是氰化法。试写出配平的化学方程式。第第题(6分)1Hg2Cl2(2分) (1分)212Hg12NaCl4KAl(SO4)23O26Hg2Cl26Na2SO42K2SO42Al2O3(2分)3升华(1分)题(6分)汞有一种化合物X,室温下是无气味、白色结晶粉末,不溶解于水,400500时升华,光照能分解,常用做电极材料。X俗名轻粉,可由水银、明矾、食盐等混合炼制,有攻毒杀虫消水肿之功效。1写出X的化学式和电子式;2写出制备X的化学方程式;3从反应体系中分离出X的方法。第第题(25分)1(1)2CuFeS2O2Cu2S2FeSSO2 FeSO2FeOSO22Cu2S3O22Cu2O2SO2 FeOSiO2FeSiO3 Cu2S2Cu2O6CuSO2 2CuFeS22SiO25O22Cu2FeSiO34SO2(各1分)(2)以粗铜作阳极,薄精铜片作阴极,用直流电电解纯硫酸铜溶液(2分)2(1)A是CuCl;B是NaCuCl2(各1分)(2)CuFeS23FeCl3CuCl4FeCl22SCuFeS23CuCl24CuClFeCl22SNaClCuClNaCuCl22NaCuCl22NaCl
4、CuCuCl2(各1分)(3)母液可以在处理铜矿砂时循环使用(1分)3(1)4CuFeS22H2SO417O24CuSO42Fe2(SO4)32H2O(2分)(2)即使含量较少的矿也可以被利用,这种方法适意于被废弃的损坏矿堆;与治炼法不同,没有SO2排放到大气中,减少了对环境的污染;能量成本费用远远低于冶炼法。(各1分)4(1)4CuFeS217O24CuSO42Fe2O38SO2(2分)(2)控制加入CuFeS2的速度,因CuFeS2与O2反应放热(1分)(3)CuSO4CuOSO3(2分)题(25分)铜是一种重要的导电金属,含铜最丰富的自然资源是黄铜矿(CuFeS2)。一般铜的冶炼以黄铜矿为原料。1常规冶炼方法是通入适量氧气,将金属转化为低价硫化物;通入适量氧气,将金属转化为低价氧化物;加入SiO2将铁以矿渣形式除去;将铜的硫化物和氧化物按适当比例混合反应得到单质粗铜。(1)写出各步反应方程式和总反应方程式。(2)上述方法得到的是粗铜,如何得到精铜?2除上述干法外,另一种用湿法冶炼的技术是:用FeCl3、CuCl2的混合液处理富铜矿砂,使其中的Cu元素转变为难溶物A,S元素转变为硫
《高中化学竞赛试题》由会员枫**分享,可在线阅读,更多相关《高中化学竞赛试题》请在金锄头文库上搜索。

信托借款合同标准范文(六篇)

公司股东合伙协议书简单版(四篇).doc

职业经理人培训心得体会

改善办公环境 提高企业形象

2023年写企业文化心得体会总结汇总

大学生创新创业计划范文(3篇).doc

房建主体施工方案

酒店餐饮领班工作总结(二篇).doc
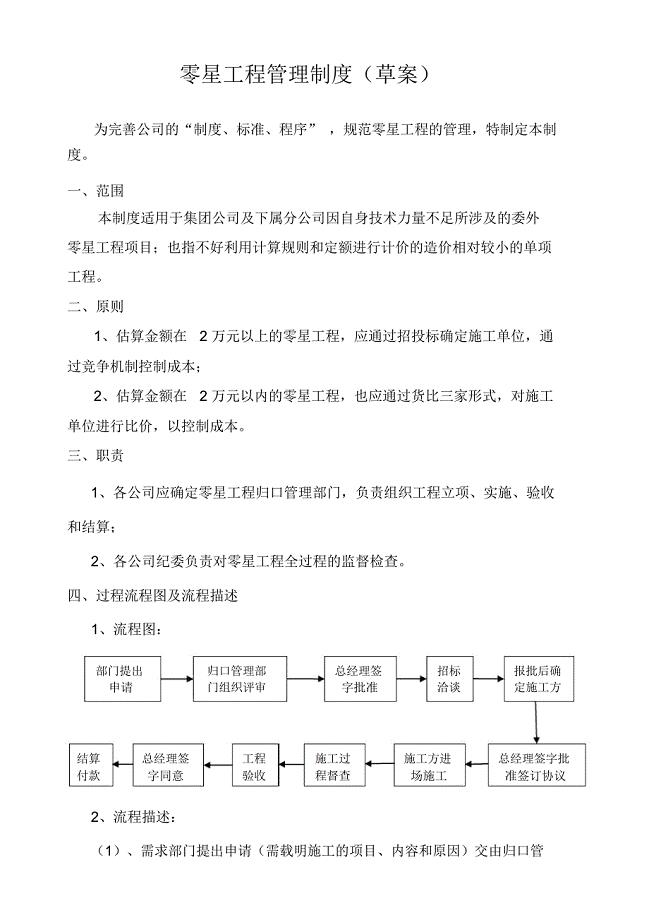
零星工程管理制度(草案)

机关演讲稿4篇

文明施工选择及多选题答案

2活动量管理办法

九年级历史上册复习提纲2

施工组织设计污水管道改造工程

北大万柳周转楼悬挑架施工方案(正式)

中外合资电力建设股东协议书范文(二篇)

福建师范大学21秋《心理测量学》在线作业三答案参考8

收养协议书模板集合九篇

销售员考核工作总结样本(3篇).doc

华电辉腾锡勒2^
 2021年福建高院案例:未办理收养手续养子女有继承权吗?
2021年福建高院案例:未办理收养手续养子女有继承权吗?
2022-11-01 5页
 2022年高考化学大一轮复习第33讲盐类的水解考点3盐类水解的应用考题集萃实战演练
2022年高考化学大一轮复习第33讲盐类的水解考点3盐类水解的应用考题集萃实战演练
2023-06-01 2页
 高考语文判断和修改语病的基本原理与简洁方法
高考语文判断和修改语病的基本原理与简洁方法
2024-02-17 6页
 高二语文期中复习题四
高二语文期中复习题四
2022-10-11 6页
 2012年高中生物第3章单元过关测试新人教版必修
2012年高中生物第3章单元过关测试新人教版必修
2023-07-12 5页
 排列组合中的分堆问题高二数学课
排列组合中的分堆问题高二数学课
2022-10-06 2页
 2022年鲁教版化学九年《化学元素与人体健康》word同步教案一
2022年鲁教版化学九年《化学元素与人体健康》word同步教案一
2024-01-16 3页
 高中化学金属与非金属的反应单元小结与测试新人教版必修
高中化学金属与非金属的反应单元小结与测试新人教版必修
2023-07-05 4页
 高三英语一轮复习辅导与测试 第1部分 Unit 5 First aid课时训练 新人教版必修5
高三英语一轮复习辅导与测试 第1部分 Unit 5 First aid课时训练 新人教版必修5
2023-06-12 6页
 高中语文:《中国古代诗歌散文欣赏》第3单元第2课 《阁夜》(教案)新人教版选修系列
高中语文:《中国古代诗歌散文欣赏》第3单元第2课 《阁夜》(教案)新人教版选修系列
2022-08-01 3页

