
第一页物化B卷答案
9页1、Q = -W = nRT ln 件=P2W =4441JAS (体)=2-4441J - K-1 = -14.90J - K-1 T 298.151 x 8.314 x 298.15ln600I100 丿AA = AG = nRT ln 厶=P_ 1AS(隔)=AS(体)+ AS(环)Q 4441乂 =J - K-1 = 14.90J - K-1T 298.15S(环)=J=4441J郑州大学2010年攻读硕士学位研究生入学试题B卷答案学科、专业:化学研究方向:工业催化,应用化学共 8 页)考试科目:物理化学(五),科目代码925 答案一律写在考点统一发的答题纸上,否则无效1. 1molO2由298.15K, 100 kPa的压力下经等温可逆压缩增至600 kPa的终态。试求Q, W, AU , AH , AG , AA , AS(体)以及 AS(隔)?(20分)解:J是理想气体的等温可逆过程AU = 0AH 二 0J = -4441J1 x 8.314 x 298.151n 型( 600 丿_环AS(隔)=02分2.在一5C时,过冷液体苯的蒸气压为2632Pa,而固体苯的蒸气压为22
2、80Pa。已知1 mol过冷液体苯在一5C凝固时的AS=-35.65J - K-1 - mol-1,气体为理想气体,求该凝固过程的AG及AH。m(20 分)解:在相同的始终态间可设计可逆过程如下:(1日 lcc IL5二GAs e .A;:, Hh c c d 5 m - -恒温 可逆- -J-温逆 恒可rl- AGn51 -嚴ALlol0 tl5二3 1-a gJp J.Ls1 H22 ch- mo- - -根据状态函数法:AG = AG +AG +AG +AG +AG12345AG = 0,过程和为可5因为过程和(5)为凝聚相的等温变压过程,所以AG = 0 ,1逆相变过程,所以AG AG = 0。24AG = AG3 = nRT 燈=J = 319.9J(2280)1x 8.314 x 268 x ln(2632丿AH AG + T AS 319.9 + 268 x 1x (35.65) J 9874Jmin。(1)求反应在65 C、3.某一级反应测得其半衰期在65C时为2.50 min,在80C时为0.50 mi80C时的速率常数匕、k2 (2)求反应的活化能。(3)在什么温度
3、下方使该一级反应1 min完成 90% ?(20分)解:该反应是一级反应=皿k = ln2/ t =0.277min-111/2k = ln2/ t =1.386min-121/2(2) 由公式In (k2/ k1)=Ea/R (1/T1-1/T2)代入数据,得:Ea=106.58KJ/mol(3) -ln(1-x)=kt代入数据,得k3=2.303min-1由 ln (k3/ k1)=Ea/R (1/人-1任3)代入数据,得 T3=356.8K 4.气相反应H2(g)+Br 2(g)=2HB r(g)的历程为:(1) BJ 一 2Br(kJ Br + H 2 -HBr + H(k 2)(3) H + Br 2 一HBr + Br(k 3)(4) H + HBr - H + Br2(k 4)(5) 2Br Br2(k 5)试证明反应的动力学方程式为:dHBr kH Br i/2 cc厶Zdt1+k艷Br 2(10 分)dHBr k证:二kdt= 2k Br -k BrH + k HBr + k HHBr -2k Br2 =01222324BrH + k HBr - k HHBr324(
4、1)dt= k BrH - k HBr - k HHBr =0dt22324(1)-得:=2k HBr dt 32(2) + (3) 2k Br -2k Br2 =01 2 -Br二(kAk Br 2丿1/2以(5)代入(2)式移项得:以(6)代入(4)式得:(k )1.k丿H二丿k Br + k HBr324(k)Jk Br + k HBr324(k )k5丿k H221/2Br 1/22(6)2k k H dHBr _ _3 22dt式分子、分母各除以k3Br2,并令k = 2k21/2Br 3/22(7)1/2dHBr kH Br 1/2 cc2 21+k艷 Br dt5.有二元凝聚系统相图如图所示。已知A、B可生成化合物。解答下列问题:(18分)(1) 写出A与B生成稳定化合物和不稳定化合物的组成;(2) 指出相图上条件自由度为0的线;(3) 根据此二元凝聚系统相图列表分析所标区域的相数、相态及自由度数;(4) 画出从系统点O-O,的步冷曲线,并说明冷却过程的相变化。图二元凝聚系统相图解:(1)稳定化合物AB;不稳定化合物A2B;2分(2) 自由度为0的线:HEI、LMN、DJ
《第一页物化B卷答案》由会员ni****g分享,可在线阅读,更多相关《第一页物化B卷答案》请在金锄头文库上搜索。

京东物流园实训报告范文三篇

【最新资料】陕西省中考数学试题及答案(Word版)

合伙型联营合同范文(5篇).doc

包工包料装修合同常用版(4篇).doc

新人教版小学数学五年级上册教学计划范文.doc

临时租赁协议实标准版(9篇)

KET词汇表(完整默写表)

全面认真做好高中各年级开学衔接工作计划幼小衔接工作计划

华师一附中光谷分校七年级下数学测试题(二)
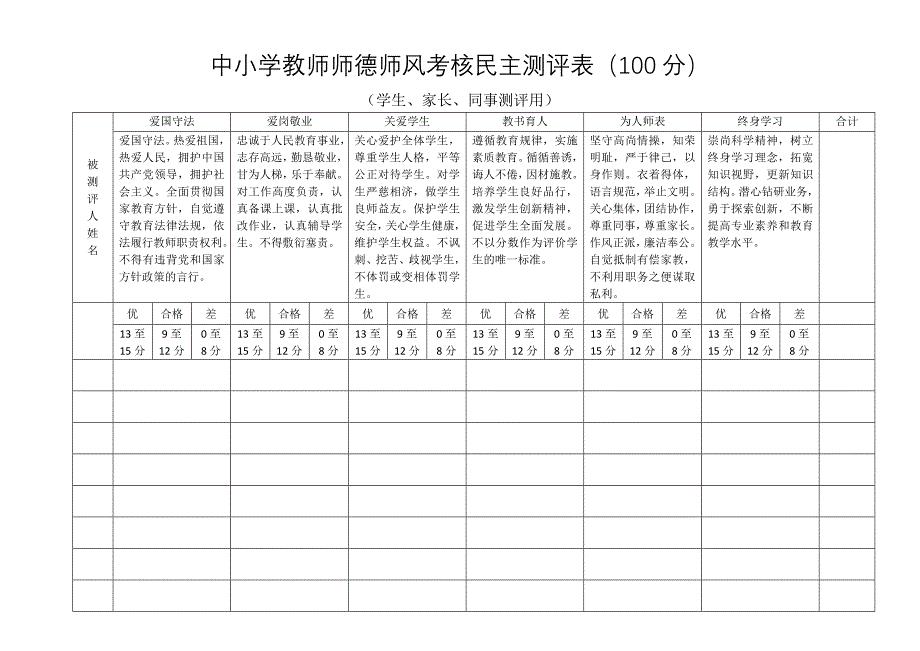
中小学教师师德师风考核民主测评表.docx

美世点因素法岗位评估体系

消防卫士优秀个人事迹(6篇)

2023年王市长讲话

公司借款合同4篇

神经生物学复习题答案

发明专利请求书47967

劳务协议简易样本(九篇)

幼儿交通安全活动方案(三篇)

廉洁工作总结4篇

转速、电流反馈控制直流调速系统仿真
 住宅单张文案
住宅单张文案
2023-07-09 2页
 海洋工程环境影响评价技术导则
海洋工程环境影响评价技术导则
2023-03-06 15页
 独一味胶囊治疗腰椎间盘突出症的临床观察
独一味胶囊治疗腰椎间盘突出症的临床观察
2022-09-24 2页
 电力安全生产的主要措施
电力安全生产的主要措施
2023-05-25 11页
 H型钢柱拼接节点技术手册
H型钢柱拼接节点技术手册
2024-02-25 17页
 高光谱数据处理的相关方法
高光谱数据处理的相关方法
2023-03-23 9页
 人体必需脂肪N3与N6(讲稿)
人体必需脂肪N3与N6(讲稿)
2023-03-09 6页
 电气工程及其自动化
电气工程及其自动化
2023-04-02 14页
 工会各岗位职责
工会各岗位职责
2023-11-26 15页
 网络摄像机设置说明书
网络摄像机设置说明书
2022-09-24 14页

