
福建省泉港一中2015届高三高考围题卷理综
5页1、泉港一中2015届高三高考围题卷理科综合试题(满分:300分 考试时间:2小时30分钟)第卷 本卷18小题,每小题6分。共108分。在每小题给出的四个选项中,只有一个选项符合题目要求。6. 下列对物质的用途的描述中,错误的是 A. 铝可用于冶炼某些熔点较高的金属 B. Na2O2课用于漂白某些物质 C. 碱石灰可用于干燥CO2、NH3等气体 D. NaClO可用作消毒剂7. 下列关于乙酸的说法不正确的是( ) A食醋中含有3%5%的乙酸 B黄酒变酸是因为部分乙醇氧化为乙酸C与甲酸甲酯互为同分异构体 D通过乙酸乙酯的碱性水解直接获取8. 短周期元素R、T、X、Y、Z在元素周期表的相对位置如下表所示,它们的最外层电子数之和为24。则下列判断正确的是( )AR位于元素周期表中第二周期第VA族 BR能分别与X、Z形成共价化合物C气态氢化物稳定性:YT DZ元素的最高价氧化物对应的水化物的化学式为HZO49. 在常温下,对于pH=3的醋酸溶液。下列说法正确的是( )。A在醋酸溶液中,NH4+、Na+、SiO32-、CO23-能大量共存B与Na2S2O3溶液反应的离子方程式:S2O32-2H+SS
2、O2H2OC常温下,加水稀释醋酸,增大D该醋酸溶液中c(CH3COO-)0.001 molL-110下列实验方案中,不能达到实验目的的是( )选项实验目的实验方案A检验淀粉是否水解生成葡萄糖向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后水解液用NaOH溶液中和,然后再加入新制Cu(OH)2浊液,加热,观察是否有红色沉淀生成B检验Fe(NO3)2晶体是否已氧化变质将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变红C验证Br2的氧化性强于I2将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色D验证Fe(OH)3的溶解度小于Mg(OH)2将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色11. 右图为一种微生物燃料电池结构示意图,关于该电池叙述正确的是( ) A分子组成为Cm(H2O)n的物质一定是糖类 B微生物所在电极区放电时发生还原反应 C放电过程中,H从正极区移向负极区 D正极反应式为:MnO24H+2eMn22H2O12. 在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g) +Y(g)3
3、Z(g) H0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( ) A升高温度,平衡常数增大 BW点X的正反应速率等于M点X的正反应速率 CQ点时,Y的转化率最大 D平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大第卷必考部分23. (15分)元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是 。a原子半径和离子半径均减小 b金属性减弱,非金属性增强c氧化物对应的水化物碱性减弱,酸性增强 d单质的熔点降低(2)还原性最弱的简单阴离子的结构示意图是 。(3)晶体硅(熔点1410 )是良好的半导体材料。由粗硅制纯硅过程如下: Si(粗)SiCl4SiCl4(纯)Si(纯)在上述由SiCl4制纯硅的反应中,测得每生成1.12 kg纯硅需吸收a kJ热量,写出该反应的热化学方程式 。(4)Na2S溶液长期放置有硫析出,原因为 (用离子方程式表示)。(5)已知:2SO2(g)O2(g)2SO3(g) 平衡常数为K12NO(g)O2(g)2NO2(g) 平衡常数为K2
《福建省泉港一中2015届高三高考围题卷理综》由会员夏**分享,可在线阅读,更多相关《福建省泉港一中2015届高三高考围题卷理综》请在金锄头文库上搜索。

2023年小学端午节主题活动总结.docx

2023年五年级上册数学教案45梯形的面积︳北师大版秋五年级上册梯形的面积.doc

江苏省苏州市吴中学区2023学年化学九年级第一学期期中教学质量检测试题含解析.doc
![第11课时 通分[1].docx](https://union.152files.goldhoe.com/2022-8/3/7f0129e0-1c7a-4a49-a8fa-08423bb008b9/pic1.jpg)
第11课时 通分[1].docx

2023农村建设发展年度计划范文(2篇).doc

2023年办公室工作总结深入开展创先争优活动的工作总结.docx

集团高校毕业生成才先进个人问卷.doc

2023年最美家庭事迹材料优秀例文精选.docx

2023年七年级语文第课 《小巷深处》导学案.doc

公司员工结婚领导精彩的讲话稿范文8篇

巧用蒙太奇手法优化语文PPT课件制作优秀获奖科研论文.docx

2023年交通安全主题演讲稿22.docx

市场监管局优化营商环境工作开展情况的报告
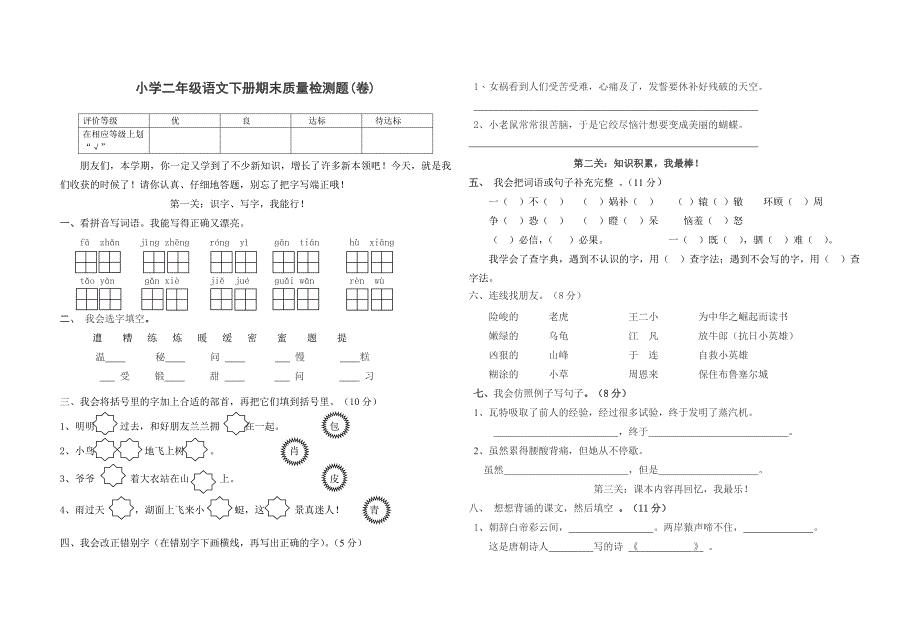
小学二年级语文下册期末质量检测题(卷)

2023年观后感春节作文61范文.docx

2023年初中政治教学中德育教育渗透新探.doc

2023年各单位执行公司“四大任务六大措施”纪委综合运营室跟踪检查情况简要汇报2.docx

家长如何检查孩子的作业.doc

巡回检验纪录设备

安全管理之煤矿安全与心理
 2022年高中化学 第4章第1节 开发利用金属矿物和海水资源教学设计 新人教版必修2
2022年高中化学 第4章第1节 开发利用金属矿物和海水资源教学设计 新人教版必修2
2023-12-28 6页
 广东省潮州市2013届高三第二次模拟考试英语试题版含答案
广东省潮州市2013届高三第二次模拟考试英语试题版含答案
2023-03-21 11页
 2017版《188套重组优化卷》高考生物一轮训练:课时考点13细胞的分化、衰老、凋亡和癌变.doc
2017版《188套重组优化卷》高考生物一轮训练:课时考点13细胞的分化、衰老、凋亡和癌变.doc
2023-05-23 17页
 2018-2019学年高考英语一轮复习Unit16Stories高考试卷分块专练北师大版选修6
2018-2019学年高考英语一轮复习Unit16Stories高考试卷分块专练北师大版选修6
2023-11-24 16页
 2022年高考数学一轮复习 第六章 不等式课时训练
2022年高考数学一轮复习 第六章 不等式课时训练
2023-06-01 13页
 中学生学习态度与学习方法综合测评量表99题系统详实,非常好用
中学生学习态度与学习方法综合测评量表99题系统详实,非常好用
2022-12-14 14页
 高一16班主题班会安全教育教案
高一16班主题班会安全教育教案
2022-09-07 4页
 高三文理科生十大理想职业
高三文理科生十大理想职业
2022-09-17 3页
 江西省吉安市吉水县第二中学2022-2023学年物理高一上期末联考模拟试题含解析
江西省吉安市吉水县第二中学2022-2023学年物理高一上期末联考模拟试题含解析
2023-09-01 11页
 浙江省杭州市2012-2013学年高二数学下学期期中试题 理 新人教A版
浙江省杭州市2012-2013学年高二数学下学期期中试题 理 新人教A版
2024-02-02 9页

