
2013届高三化学一轮复习 45分钟滚动基础训练卷(7)(含解析) 新人教版
6页1、45分钟单元基础训练卷(七) 考查范围:第七单元分值:100分一、选择题(本题包括7小题,每小题6分,共42分,每小题只有一个正确答案)1下列叙述正确的是()A电镀时,通常把待镀的金属制品作阳极B氯碱工业是电解熔融的NaCl,在阳极能得到Cl2C氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为O24H4e=2H2OD图D71中电子由Zn极流向Cu,盐桥中的Cl移向CuSO4溶液图D712镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高而平稳,因而越来越成为人们研制绿色电池所关注的焦点。某种镁二次电池的反应为xMgMo3S4MgxMo3S4,下列叙述不正确的是()A放电时正极的电极反应为:Mo3S42xe=Mo3SB充电时阴极的电极反应为:xMg22xe=xMgC放电时Mg2向正极移动D放电时Mo3S4发生氧化反应3大功率镍氢动力电池及其管理模块,是国家“十五”“863”计划电动汽车重大专项中一项重要课题。我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池。常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为La
2、Ni56Ni(OH)2LaNi5H66NiO(OH)下列说法正确的是()A放电时储氢合金作正极B充电时储氢合金作阳极C充电时阳极周围c(OH)增大D放电时负极反应:LaNi5H66OH6e=LaNi56H2O4串联电路中四个电解池分别装有0.5 molL1的下列溶液,用惰性电极电解,连接直流电源一段时间后,pH最小的是()AKNO3溶液BNaCl溶液CAgNO3溶液 DCuCl2溶液图D725如图D72所示,X为铁,Y为石墨电极,a是电解质溶液,实验开始前,在U形管的两边同时滴入几滴酚酞,下列叙述错误的是()A合上K1、断开K2,若a是稀硫酸,则Y上有气泡冒出B合上K1、断开K2,若a是饱和食盐水,则Y电极附近溶液慢慢变为红色C合上K2、断开K1,若a是硫酸铜溶液,则Y电极上有红色物质析出D合上K2、断开K1,若a是氢氧化铁胶体,则X电极附近红褐色加深6用铅蓄电池电解AgNO3溶液、Na2SO4溶液,a、b、c、d电极材料均为石墨。已知铅蓄电池的总反应式为:Pb(s)PbO2(s)2H2SO4(aq)2PbSO4(s)2H2O(l),通电时a电极质量增加,下列说法正确的是()图D73A
3、电路中转移1 mol电子时,Y电极质量增加48 gB放电时铅蓄电池负极的电极反应式为:PbO2(s)4H(aq)SO(aq)2e=PbSO4(s)2H2O(l)Cc、d电极产生气体的物质的量之比为12DX是负极7用石墨作电极电解1 000 mL 0.1 molL1 CuSO4溶液,通电一段时间后关闭电源,测得溶液的质量减少了9.8 g。下列有关叙述正确的是(NA代表阿伏加德罗常数)()A电解过程中流经外电路的电子个数为0.2NAB在标准状况下,两极共产生4.48 L气体C电解后溶液的pH为1(溶液体积不变)D加入11.1 g Cu2(OH)2 CO3可将溶液彻底复原二、非选择题(本题包括4个小题,共58分)8(14分)钢铁工业是国家工业的基础,请回答钢铁腐蚀与防护过程中的有关问题。(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式为_。(2)下列哪些装置可防止铁被腐蚀_(填字母)。图D74(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置如图D75:图D75A电极对应的金属是_(写元素名称),B电极的电极反应式是_。若电镀前
《2013届高三化学一轮复习 45分钟滚动基础训练卷(7)(含解析) 新人教版》由会员夏**分享,可在线阅读,更多相关《2013届高三化学一轮复习 45分钟滚动基础训练卷(7)(含解析) 新人教版》请在金锄头文库上搜索。

2021音体美工作总结.doc
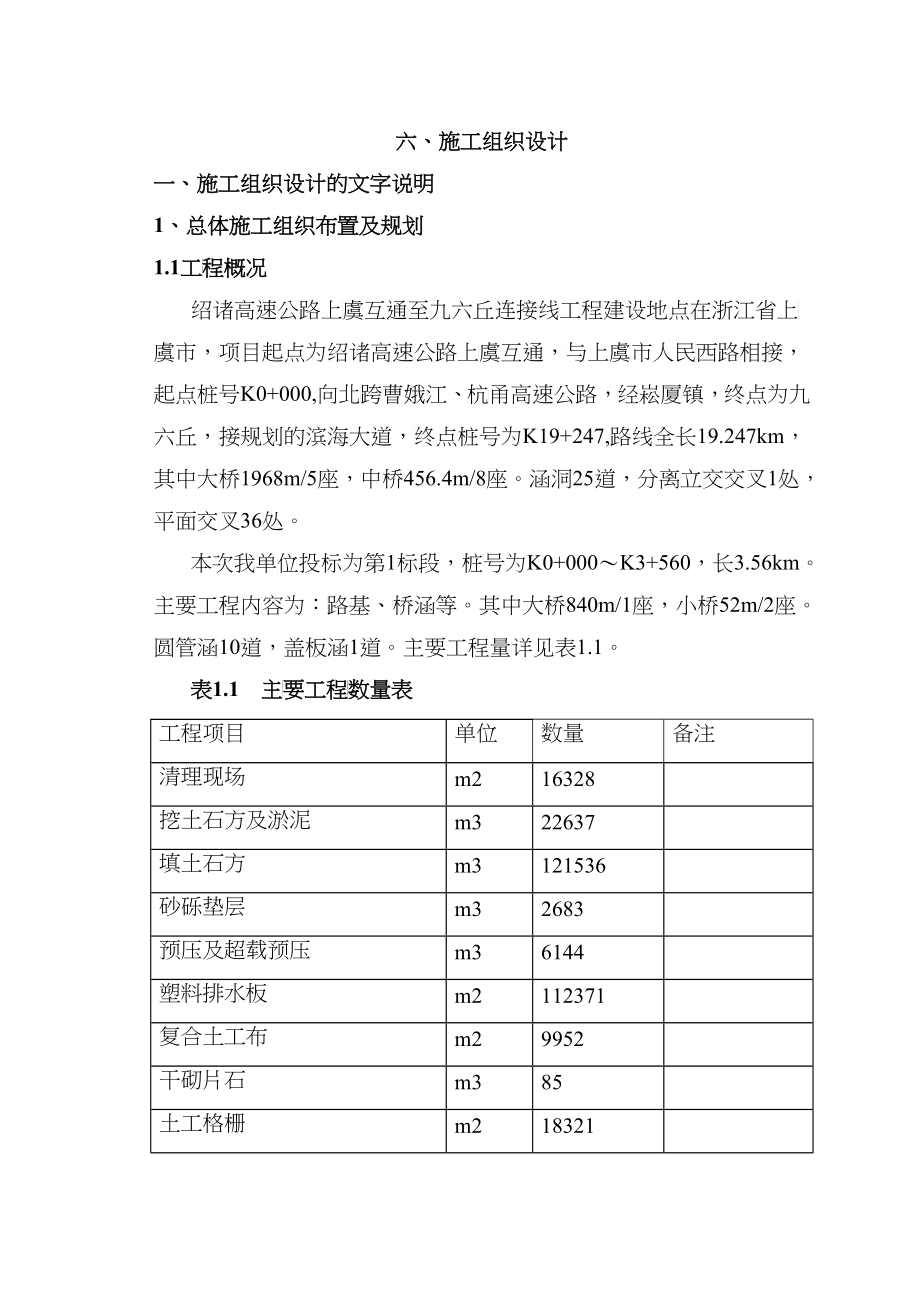
上虞互通至九六丘连接线工程1标施组

采用任务驱动模式教好信息技术课

2023年四川省眉山市彭山区谢家街道李山村社区工作人员考试模拟题及答案

自我介绍演讲稿【推荐】.doc

课前三分钟励志演讲稿合集15篇.doc

小学联盟防控新型冠状病毒传染病应急预案

幼儿园事业单位年度考核个人总结模板.doc

热门读书活动总结模板五篇

2019教育初三化学第五单元化学方程式测试题.doc

安全工作排查整改方案.docx

邮储银行生日演讲稿精选WORD.docx

银行个人年度工作总结(4篇).doc

我是一台电脑作文

道路安全法扣分细则

2022年小学五年级数学期中考试总结.doc

新能源环卫车项目可行性研究报告-可参考案例-备案立项.doc

煤矿中专自我总结范文3篇.docx

2021高校老师工作述职报告写作范本 .docx

鸡年吉祥成语.docx
 五金配件简明分类列表
五金配件简明分类列表
2024-01-14 7页
 只用圆规作已知圆圆心的作法及证明
只用圆规作已知圆圆心的作法及证明
2023-01-18 3页
 天津市2013届高三数学总复习 综合专题 导数在研究函数单调性中的应用 课堂验收(学生版)
天津市2013届高三数学总复习 综合专题 导数在研究函数单调性中的应用 课堂验收(学生版)
2023-08-22 1页
 分数变化问题
分数变化问题
2023-08-20 7页
 临时水电施工组织设计(DOC)(DOC 14页)
临时水电施工组织设计(DOC)(DOC 14页)
2023-06-05 14页
 实施GSP内审表.doc
实施GSP内审表.doc
2023-05-22 59页
 中国建筑分包管理手册
中国建筑分包管理手册
2023-09-25 72页
 花园住宅楼工程施工组织设计方案
花园住宅楼工程施工组织设计方案
2022-11-26 80页
 红宝太和胶囊使用手册
红宝太和胶囊使用手册
2022-09-11 12页
 《从生物圈到细胞》教案
《从生物圈到细胞》教案
2024-01-03 2页

