
【最新资料】鲁科版化学选修四1.2.2 电解原理的应用每课一练含答案
6页1、最新教学资料鲁教版化学一、选择题(本题包括7小题,每小题3分,共21分)1下列描述中,不符合生产实际的是 ()A电解熔融的氧化铝制取金属铝,用铁作阳极B电解法精炼粗铜,用纯铜作阴极C电解饱和食盐水制烧碱,用涂镍碳钢网作阴极D在镀件上电镀锌,用锌作阳极解析:电解池的阳极发生氧化反应、阴极发生还原反应。电解熔融的Al2O3制Al时,若用Fe作阳极,会发生Fe2e=Fe2,Fe2移动到阴极上发生Fe22e=Fe,使得到的Al不纯。答案:A2某同学在做电解食盐水的实验时,误用铜棒做两极材料,请判断下列说法正确的是()A完全电解后,得到CuCl2溶液B电解完全并放置一段时间后,得到蓝色沉淀和NaCl溶液C电解一段时间后,NaCl溶液浓度可能变小D电解后溶液中的NaCl质量一定不变解析:阳极反应Cu2e=Cu2,阴极反应2H2e=H2,余下OH,一段时间之后Cu2会与OH在两极之间部分反应生成Cu(OH)2,电解过程中不消耗NaCl,只消耗水,所以剩余的NaCl溶液浓度可能变大或不变(饱和溶液),溶液中NaCl质量可能变小(饱和溶液,析出晶体)或不变。答案:B3许多金属都可以通过电解的方法达到精炼
2、的目的。下列有关该方法的叙述中,正确的是 ()A含杂质的粗金属做阳极,与直流电源的正极相连B阴极只要是一种导体即可,与精炼过程无关C电解质溶液中除了含有精炼的金属的阳离子之外,绝对不能含有其他金属阳离子D在精炼过程中,电解质溶液的成分不发生任何变化解析:阳极要失电子,含杂质的粗金属做阳极,纯金属做阴极,若阴极用其他导体就会使需要精炼的金属覆盖在该导体上;粗金属中可能含有一些比较活泼的金属,失电子之后也会进入溶液,电解质溶液的成分可能会增加。答案:A4在水中加入等物质的量的Ag、Pb2、Na、SO、NO、Cl,该溶液放在用惰性材料做电极的电解槽中,通电片刻,则氧化产物与还原产物的质量之比为 ()A35.5108 B16207C81 D10835.5解析:由于Ag与Cl、Pb2与SO形成沉淀,电解的是NaNO3溶液,实质是电解水。答案:C5在25时,将两个铂电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,在阳极逸出a mol气体,同时有W g Na2SO410H2O析出,若温度不变,此时剩余溶液中溶质的质量分数为 ()A.100%B.100%C.100%D.100%解析:此题要注
3、意题目条件。“铂电极”与“铜电极”不同,在阳极析出a mol气体与在阴极析出a mol气体不同。消耗水的计算:2n(H2O)n(O2),即消耗2a mol水,析出晶体中所含溶质为W g。原溶液减少的质量为(W2a18) g,因剩余溶液仍为饱和溶液,故剩余溶液中溶质的质量分数为/(W2a18)100%100%。答案:D6Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下图所示,电解总反应为:2CuH2OCu2OH2。下列说法正确的是 ()A石墨电极上产生氢气B铜电极发生还原反应C铜电极接直流电源的负极D当有0.1 mol电子转移时,有0.1 mol Cu2O生成解析:从反应中得知Cu在通电时失电子在阳极放电,发生氧化反应,另一电极(石墨)作阴极,发生还原反应,2H2O2e=H22OH,相应的2Cu2OH2e=Cu2OH2O,转移0.1 mol电子生成0.05 mol Cu2O,故B、C、D项错。答案:A7KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解质溶液。在一定条件下电解,反应式为KI3H2O=KIO33H2。下列有关说法中,正确的是()
《【最新资料】鲁科版化学选修四1.2.2 电解原理的应用每课一练含答案》由会员hs****ma分享,可在线阅读,更多相关《【最新资料】鲁科版化学选修四1.2.2 电解原理的应用每课一练含答案》请在金锄头文库上搜索。

民法经典案例口决超强记忆

关于月是故乡明的记叙文800字

有关文员实习日记三篇

财务审核人员岗位职责(4篇)

2023年助理工作计划标准模板(5篇)

导轨插销铰链项目资金申请报告写作模板-定制代写

大面积停电事件应急处置预案

各级人员安全生产岗位责任制常用版(6篇)

2023年毕业实习总结范文(5篇).doc

公司后勤个人工作计划例文(2篇).doc

山西省朔州市怀仁某校高一数学下学期期末考试试题理

售楼处客服工作总结2023(售楼处销售经验总结)
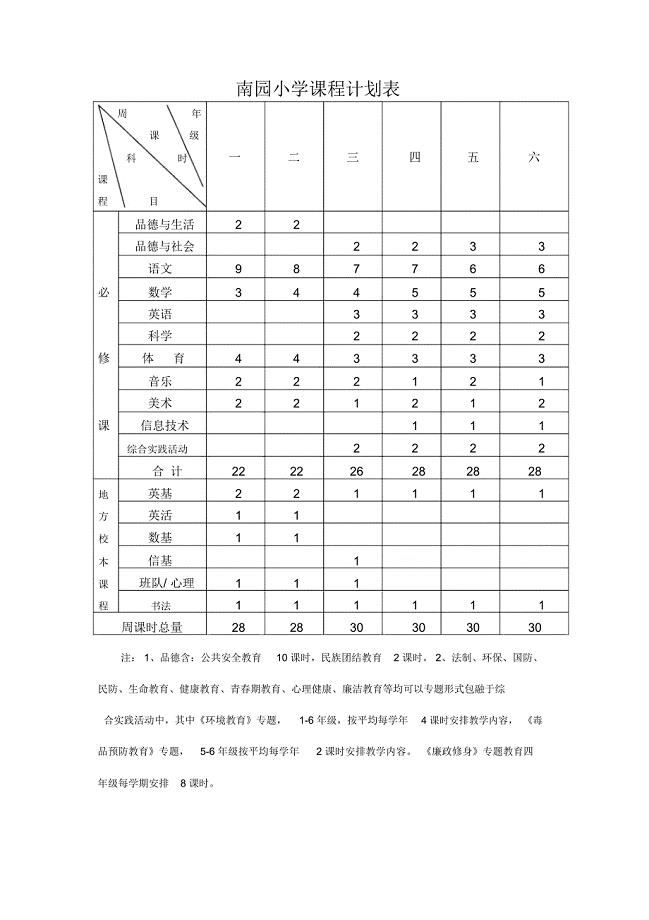
南园小学课程计划表

上海市劳动合同官方版(4篇).doc

部编人教版六年级下册语文《语文园地一》教案

三年级下册语文试题-25慢性子裁缝和急性子顾客一课一练

立柱式自动焊接机安全技术操作规程

幼儿园家长学校工作总结

2022年12月教师学期教学工作总结

高中数学第一章集合阶段性测试题(DOC 6页)
 2022年证券一般从业考试模拟卷含答案第171期
2022年证券一般从业考试模拟卷含答案第171期
2024-02-23 81页
 大庆石化公司制氢装置用转化催化剂
大庆石化公司制氢装置用转化催化剂
2023-02-19 6页
 初中语文教师专业发展培训方案
初中语文教师专业发展培训方案
2024-02-12 8页
 仓库管理工作总结范文
仓库管理工作总结范文
2022-09-24 12页
 新教材高中数学 1.3全称量词与存在量词练习 北师大版选修11
新教材高中数学 1.3全称量词与存在量词练习 北师大版选修11
2022-12-18 5页
 造价工程师《建设工程计价》考试历年真题汇总含答案参考2
造价工程师《建设工程计价》考试历年真题汇总含答案参考2
2023-11-23 25页
 西咪替丁胶囊生产工艺规程
西咪替丁胶囊生产工艺规程
2023-11-13 12页
 Dreamweaver网页设计课程复习资料
Dreamweaver网页设计课程复习资料
2023-08-18 9页
 溢洪道消力池施工方案
溢洪道消力池施工方案
2023-11-10 24页
 拖动系统课程设计汇本报告
拖动系统课程设计汇本报告
2023-02-20 20页

