
高中化学1.1原子结构第4课时导学案新人教版选修3
7页1、此资料由网络收集而来,如有侵权请告知上传者立即删除。资料共分享,我们负责传递知识。选修三第一章第一节原子结构导学案(第4课时)学习时间 2020 2020学年上学期 周【课标要求】 复习巩固本章知识【主要知识再现】一、原子的诞生二、宇宙的组成与各元素的含量三、元素的分类 非金属元素:22种(包括稀有气体)元素金属元素:绝大多数四、能级与能层1能级表示方法及各能级所能容纳的最多电子数2各能层包含的原子轨道数目和可容纳的电子数电子层原子轨道类型原子轨道数目可容纳电子数11s1222s,2p4833s,3p,3d91844s,4p,4d,4f1632nn22n2五、核外电子进入轨道的顺序按照构造原理,电子进入轨道的顺序为:1s、2s、2p、3s、3p、4s、3d、4p、5s、4d、5p因此,特别要注意的是,核外电子排布并非全是按照能层的顺序逐层排布的,排满K层后再排到L层,排满了L层再排到M层,但并非排满M层后再排到N层,根据构造原理中电子进入轨道的顺序,电子是排满4s后再进入3d。例如:21号元素钪核外的21个电子依次填充轨道的顺序为1s22s22p63s23p64s23d1,但钪元素原子
2、的电子排布式应写作:1s22s22p63s23p63d14s2或Ar3d14s2。六、能量最低原理的简述在多电子原子中,核外电子总是尽先占据能量最低的轨道,然后再依次进入能量较高的原子轨道,以使整个原子的能量最低,这就是能量最低原理能量最低原理是自然界中一切物质共同遵守的普遍法则。绝大多数元素原子的核外电子排布,都是按照构造原理中的能级顺序依次进入原子轨道,而使整个原子处于能量最低状态,称之为基态。七、少数元素的基态原子的电子排布它们对于构造原理有1个电子的偏差。因为能量相同的原子轨道在全充满(如p6和d10)、半充满(如p3和d5)和全空(如p0和d0)状态时,体系的能量较低,原子较稳定。八、原子最外层、次外层及倒数第三层最多容纳电子数的解释1依据: 构造原理中的排布顺序,其实质是各能级的能量高低顺序,可由公式得出ns(n2)f(n1)dnp。2解释(1)最外层由ns、np组成,电子数不大于268。(2)次外层由(n1)s(n1)p(n1)d组成,所容纳的电子数不大于261018。(3)倒数第三层由(n2)s(n2)p(n2)d(n2)f组成,电子数不大于26101432。九、多电子原子中,电子填充原子轨道时,原子轨道能量的高低存在如下规律:1相同能层上原子轨道能量的高低: nsnpndnf。2形状相同的原子轨道能量的高低: 1s2s3s”“”或“”表示下列各组多电子原子的原子轨道能量的高低。(1)2s_3p(2)4s_4d(3)4s_3p (4)5p_7d(5)3d_4d7.A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大两个单位,C的质子数比B多4个,1 mol A的单质与酸反应,能置换出1 g H2,这时A转化为具有与氖原子相同的电子层结构的离子。试问:(1)A是_元素、B是_元素,C是_元素。(2)A的原子结构示意图:_,B的核外电子排布式:_,C原子最外层电子的轨道表示式:_
《高中化学1.1原子结构第4课时导学案新人教版选修3》由会员壹****1分享,可在线阅读,更多相关《高中化学1.1原子结构第4课时导学案新人教版选修3》请在金锄头文库上搜索。

浅谈人民币汇率制度的选择

毕业生实习鉴定表个人鉴定

“让校园充满爱”主题班会活动方案

常用污水处理设备及去除率

公司内部股权转让协议经典版(八篇).doc

商业计划书的编制参考
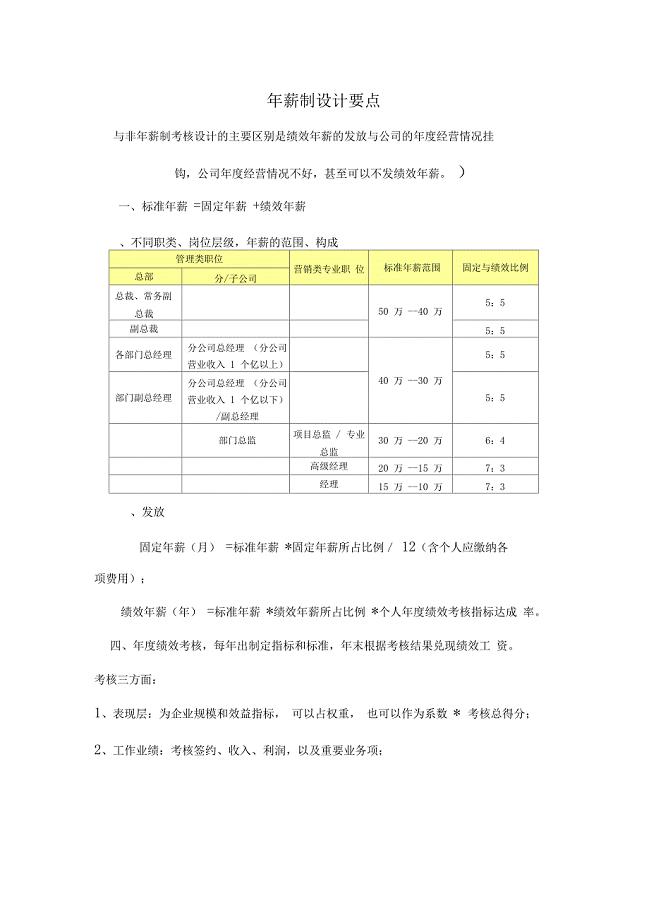
年薪制设计要点及细则参考

假期社会实践心得

茂名PCB研发项目投资计划书_模板范文

【施工方案】鄂州互通立交墩台施工方案(DOC 22页)

小学一年级班主任工作总结范文4篇2

乙二醇丁醚(ETHYLENEGLYCOLMONOBUTYLETHER)化学物质安全资料表

教育教学工作总结二

保证书500字

混凝土结构施工安全防护措施正式版

稀土发光材料的开题报告

幼儿教育评价课程心得体会

(保证书)国庆遵纪守法保证书

车辆工程专业毕业设计汽车整车论文

电销业务员工作计划标准模板(七篇).doc
 铁路系统列检员安全生产的的心得体会
铁路系统列检员安全生产的的心得体会
2023-09-03 3页
 大学教学年度个人工作总结1000字
大学教学年度个人工作总结1000字
2024-02-01 5页
 职业生涯规划的方法与步骤
职业生涯规划的方法与步骤
2023-10-16 20页
 北理工汽车构造与原理在线作业
北理工汽车构造与原理在线作业
2023-11-03 34页
 酒店餐厅经理工作计划样本(2篇).doc
酒店餐厅经理工作计划样本(2篇).doc
2023-09-11 7页
 特种设备安全监察2022年工作总结
特种设备安全监察2022年工作总结
2023-07-19 12页
 备课组工作计划(7篇)
备课组工作计划(7篇)
2024-02-09 35页
 关于质量管理专题座谈会汇报材料
关于质量管理专题座谈会汇报材料
2023-08-11 21页
 安全培训教案矿井安全管理人员初训25次1班MicrosoftW
安全培训教案矿井安全管理人员初训25次1班MicrosoftW
2024-02-23 26页
 职业学校商业计划书
职业学校商业计划书
2023-09-24 8页

