
高中化学必修一氧化还原反应第一课时
8页1、第二章 第三节 氧化还原反应(第一课时)学习目标:1.理解氧化剂、还原剂、氧化产物、还原产物概念,提高判断氧化还原反应的能力。2.探究从化合价升降的角度分析氧化还原反应的方法,揭示氧化还原反应的本质。3.学会用“单线桥” 和“双线桥”分析氧化还原反应,能初步感受化学反应守恒思想-电子守恒学习重点: 用化合价的观念理解氧化还原反应的相关概念及氧化还原本质的理解。学习难点: 氧化还原反应的实质,氧化还原反应的分析方法自主预习一: 知识链接:标出下列物质中加点元素的化合价:Fe2O3 FeO CuO FeSO4 Na2SO3 Al2S3 Na2S NaOH KMnO4 Na2CO3 NaNO3 KClO3 NH4NO3 二、氧化还原反应1、从得失氧的角度分析氧化还原反应写出碳还原氧化铜的化学反应方程式: _ CuO_氧,发生了_反应;C_氧,发生_反应定义:_氧化还原反应。2.从化合价变化的角度认识氧化还原反应H2+CuO=Cu+H2O 标出元素化合价, 元素化合价降低, 元素化合价升高, 发生氧化反应, 发生还原反应(1)氧化反应:物质所含元素的化合价的反应。(2)还原反应:物质所含元素的
2、化合价的反应。(3)氧化还原反应:物质所含元素化合价有的反应。合作探究【思考】氧化还原反应的特征是什么?运用这一特征可以迅速准确的判断反应是否为氧化还原反应。为什么会有这样的特征?【探究二】 氧化还原反应的本质1. 阅读课本P36(第3段)到P37(第2段),思考下列问题(1)根据阴、阳离子的形成过程和氯化钠的形成过程,回答钠和氯气的氧化还原反应的发生过程是怎样的?(2)氯化钠形成过程中,钠是如何失去电子而氯又是怎样得到电子的?得到1个电子,化合价如何变化?(3) 氯化氢的形成过程是否也和氯化钠的形成过程一样存在电子得失问题?为什么?化合物的形成电子得失(偏移)化合价变化氧化、还原情况2Na+Cl2=2NaCl钠原子失去 个电子转移给氯钠元素的化合价 ,被 钠发生 反应Cl2发生 反应氯原子得到 个电子氯元素的化合价 ,被 H2+Cl2=2HClH与Cl共用电子对,且共用电子对发生偏移,偏向 H化合价 被 Cl化合价 被 氢气发生 反应 氯气发生 反应 【课堂小结】氧化还原反应1.特征:元素的 有升降,2.本质:有 转移。【归纳总结】氧化反应、还原反应与得失电子与化合价变化的关系氧化反
3、应:元素化合价 ,实质是该元素的原子 (或偏离)电子,被 。(升失氧)还原反应:元素化合价 ,实质是该元素的原子 (或偏向)电子,被 。(降得还)【探究三】氧化剂、还原剂、氧化产物和还原产物之间的关系化合价 降低 , 得 电子,被 还原 氧化剂+还原剂=还原产物+氧化产物化合价 升高 , 失 电子,被 氧化 氧化还原反应中各概念之间的关系:1. 氧化剂具有 性,所含元素化合价 , 电子,发生 反应,被 ,对应生成 产物。2还原剂具有 性,所含元素化合价 , 电子,被 ,对应生成 产物。【探究四】氧化还原反应中电子转移的表示方法(1)双线桥法:表示同种元素在反应前后得失电子的情况,以氢气还原氧化铜为例,参考P36页的双线桥法,分析元素得失电子和化合价变化。失去2e-,化合价升高,被氧化失去2e-,化合价升高,被氧化如:高温+1-100H2+CuO=Cu+H2O 2Na+Cl2=NaCl 得到2e-,化合价 得到2e-,化合价 降低, 被还原 降低, 被还原 归纳:双线桥法表示时的注意事项:(1)双线桥的箭头“横跨”等号的左右;箭头箭尾必须对应化合价变化的同种元素;(2)双线桥的一个箭头始
《高中化学必修一氧化还原反应第一课时》由会员一****分享,可在线阅读,更多相关《高中化学必修一氧化还原反应第一课时》请在金锄头文库上搜索。

小学四年级数学上册2022年秋期中测试教学质量分析

中小学教师师德师风建设学习心得体会三千字

2019年云南省特岗教师招考试卷中学地理特岗真题

2020年云南特岗教师招考中学地理特岗真题试卷

2016年云南特岗教师招聘考试小学数学特岗真题

2017年云南特岗教师招考小学数学特岗真题专业知识和两学真题
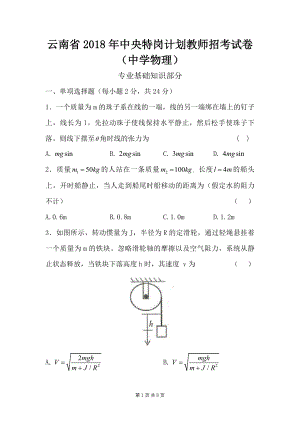
2018年云南特岗教师招考试卷中学物理特岗真题

2018年云南省特岗教师招考小学数学特岗真题专业知识和两学真题

2020年云南特岗教师招考小学数学特岗真题专业知识和两学真题参考答案

2020年云南省特岗教师招考中学物理特岗真题试卷

2020年云南特岗招考中学数学特岗真题含教育学心理学部分

云南省特岗教师招聘考试真题2017年小学美术特岗真题

2017年云南特岗教师招考试卷中学地理特岗真题

2017年云南特岗教师招考试卷中学物理特岗真题

2018年云南特岗教师招考中学地理特岗真题

部编版二年级语文下册春季学期期末教师个人工作教育教学工作总结

2019年云南特岗教师招考试卷中学物理特岗真题卷

南阳小学一二年级无纸化测试工作总结

农村小学“学困生”的成因分析及对策研究实施方案

农村中小学学生暑假安全教育安全记录主题班会齐全
 【公开课学案】Unit+3Reading+and+Thinking+学案选择性必修第四册
【公开课学案】Unit+3Reading+and+Thinking+学案选择性必修第四册
2024-05-29 3页
 【学案】Unit+3+Reading+and+Thinking学案人教版(2019)选择性必修第四册
【学案】Unit+3+Reading+and+Thinking学案人教版(2019)选择性必修第四册
2024-05-29 3页
 【学案】Unit+3Reading+and+Thinking+导学案人教版(2019)选择性必修第四册
【学案】Unit+3Reading+and+Thinking+导学案人教版(2019)选择性必修第四册
2024-05-29 3页
 【学案】Unit+3Reading+and+Thinking+学案人教版(2019)选择性必修第四册+
【学案】Unit+3Reading+and+Thinking+学案人教版(2019)选择性必修第四册+
2024-05-29 2页
 【教案】Unit+3Reading+and+Thinking教案人教版选择性必修第四册
【教案】Unit+3Reading+and+Thinking教案人教版选择性必修第四册
2024-05-29 12页
 【教案】Unit+3+Reading+and+Thinking+教案-人教版(2019)选择性必修第四册
【教案】Unit+3+Reading+and+Thinking+教案-人教版(2019)选择性必修第四册
2024-05-29 4页
 【作文】读后续写结尾升华汇总必备素材
【作文】读后续写结尾升华汇总必备素材
2024-05-29 5页
 【教案】Unit+4+Reading+and+Thinking教学设计人教版(2019)必修第三册
【教案】Unit+4+Reading+and+Thinking教学设计人教版(2019)必修第三册
2024-05-29 3页
 【教案】Unit+4+Reading+and+Thinking+教案人教版(2019)必修第三册
【教案】Unit+4+Reading+and+Thinking+教案人教版(2019)必修第三册
2024-05-29 7页
 【教案】Unit+4+Reading+and+Thinking教案人教版高中必修第三册
【教案】Unit+4+Reading+and+Thinking教案人教版高中必修第三册
2024-05-29 7页

