
高考化学专题~工艺设计流程题(含答案)
11页1、 .wd.高考专题练习工艺流程题铝灰清洗H2OHClaq搅拌加热95B溶液降温熟化调节pH至4.04.5D固体产品C用水喷淋,吸收气体ageaq1(15分)聚合氯化铝晶体的化学式为Al2(OH)nCl6-nxH2Om,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:1搅拌加热操作过程中发生反响的离子方程式;。2生产过程中操作B和D的名称均为B和D为简单操作。3生产过程中可循环使用的物质是用化学式表示。4调节pH至4.04.5的目的是。5实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯洁。生产过程中C物质可选用。ANaOH BAl C氨水 DAl2O3216分将磷肥生产中形成的副产物石膏CaSO42H2O转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。1本工艺中所用的原料除CaSO42H2O、(NH4
2、)2CO3外,还需要_等原料;2石膏悬浊液中参加碳酸铵溶液后反响的化学方程式为:_;3过滤操作所得固体有_填化学式等物质,该固体可用作生产水泥的原料;4过滤操作所得滤液是(NH4)2SO4溶液。检验滤液中含有NH4+的方法是:_;5氯化钙结晶水合物CaCl26H2O是目前常用的无机储热材料,选择的依据除熔点较低和熔化的热效应高外,还因为其_,举出该晶体的无水物在实验室的一种用途_ 。 3、制取纯洁CuCl22H20的生产过程是: (l用粗CuO含少量铁溶解在足量的稀盐酸里加热、过滤,得到Cu Cl2含FeCl2)的溶液,经测定,溶液的PH值为3 。 (2对l的溶液按以下步骤进展提纯:可做氧化剂的物质有A) KMnO4 B) K2Cr2O7 (C) H2O2 (DNaClO Cu2、Fe2十在PH值为4一5时不水解,而Fe3+却几乎全部水解。试答复: l参加的氧化剂x是答编号:; 参加x 的作用是:; 反响的离子方程式是:(2物质 Y 是;沉淀z是。参加Y 能形成沉淀z的原因是(3别离出沉淀z,并将溶液班蒸发欲获得晶体CuCl22H20。采取什么措施才能顺利得到晶体CuCl22H20?4
3、碘酸钙是食品及饲料添加剂中补碘补钙的常用试剂,微溶于水。制备碘酸钙的实验流程如下。中间产物碘酸氢钾的合成原理为:I2+2KClO3+HClKH(IO3)2+KCl+Cl2,答复以下问题:(1)制备碘酸氢钾的实验装置(支撑仪器太加热装置略去)如图,请在方框中补充必要的装置图并注明试剂.(2)假设为上图增加加热装置,所需仪器除铁架台(带铁圈)、石棉网外还有。(3)实验中判断碘反响完全的实验现象是。(4)“调pH至10的目的是。(5)参加CaCl2时反响的化学方程式为。(6)从水溶液中别离出碘酸钙时,可能得到无水盐、一水合物等,本实验得到的产品是Ca(IO3)26H2O,上述流程中与此结果密切相关的步骤是。5二氧化钛(TiO2)广泛用于制造高级白色油漆,也是许多反响的催化剂。工业上用钛铁矿主要成分为FeTiO3(钛酸亚铁,不溶于水)、Fe2O3及少量SiO2杂质作原料,制取二氧化钛及绿矾,其生产流程如下: 答复以下问题:FeTiO3溶于过量硫酸的离子方程式_。流程中生成TiO2xH2O离子方程式为_ 。假设铁粉的用量缺乏,可能导致产品TiO2中混有_杂质。(4)以TiO2为原料制取金属钛的其
《高考化学专题~工艺设计流程题(含答案)》由会员M****1分享,可在线阅读,更多相关《高考化学专题~工艺设计流程题(含答案)》请在金锄头文库上搜索。

保密制度大纲.docx
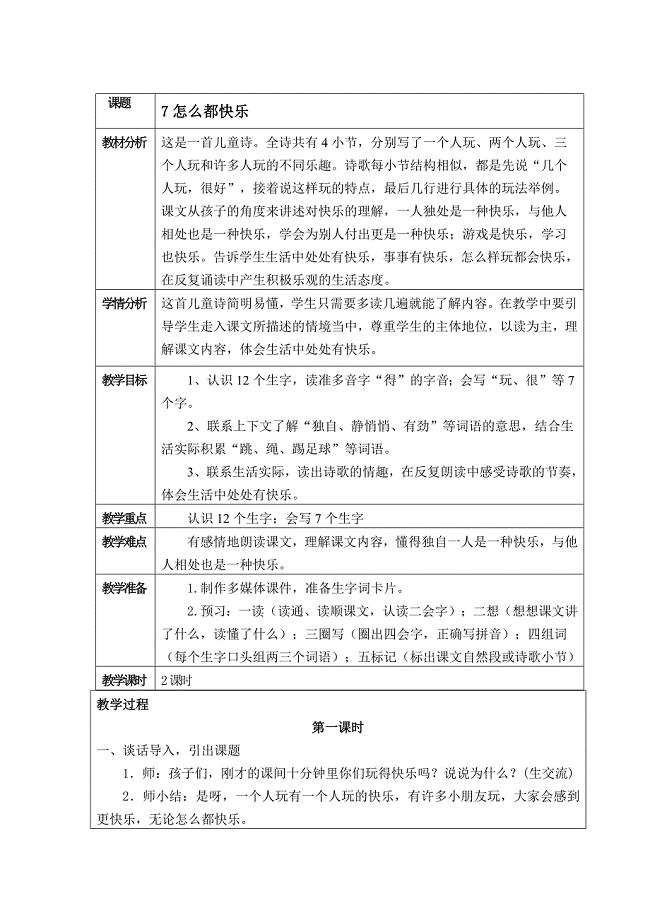
肖强花+教学设计.docx

读毕淑敏散文有感700字文档2022合辑

新年作文新年印象作文.doc

第1课时幂的乘方.doc
![没有秘密长不大读书笔记[五篇范文].docx](https://union.152files.goldhoe.com/2023-10/10/62263d45-998c-4002-8fc5-cf27187936db/pic1.jpg)
没有秘密长不大读书笔记[五篇范文].docx

2023年加强基建渣土管理实施方案.docx

项目物业承接查验移交资料清单

高考英语8级词汇训练.docx

纪委监委落实监督责任和党内问责工作情况专题报告.docx

基层人口计生干部综合业务知识测试.doc

军旅小品《我是排头兵》.doc
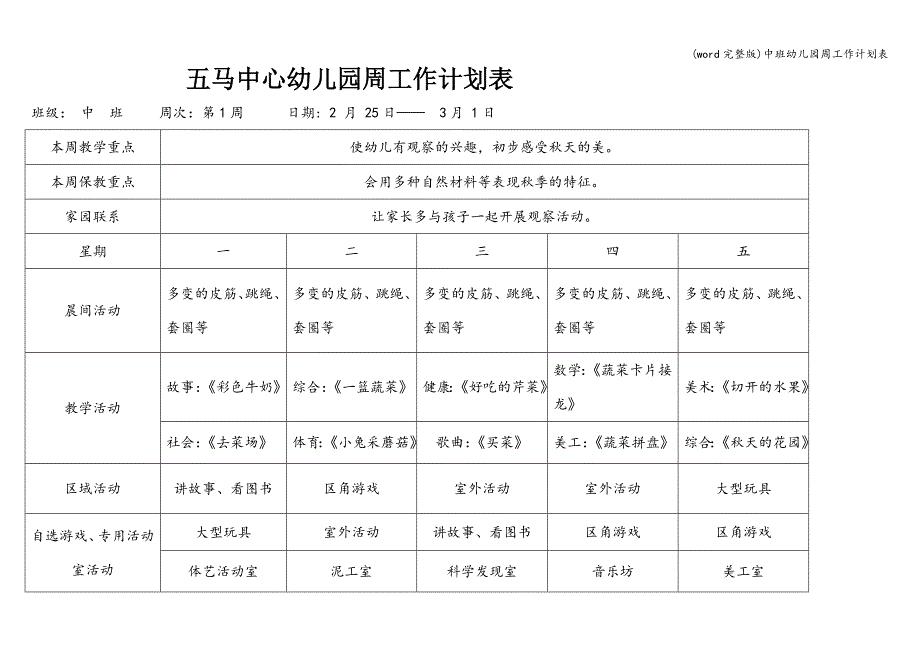
(word完整版)中班幼儿园周工作计划表.doc

hdd水平定向钻机培训讲义

空间曲线的主法线曲面的几何性质

客服实习心得体会

小升初数学应用题50道带答案(能力提升).docx

小学数学教学总结_8.doc

车库租赁协议书常范本(五篇).doc

高中生读目送心得感悟范文5篇.doc
![2BFH-4型玉米灭茬种肥联合播种机灭茬机构结构设计说明书[带图纸].doc](/Images/s.gif) 2BFH-4型玉米灭茬种肥联合播种机灭茬机构结构设计说明书[带图纸].doc
2BFH-4型玉米灭茬种肥联合播种机灭茬机构结构设计说明书[带图纸].doc
2023-08-06 41页
 “六五”普法工作的汇报材料
“六五”普法工作的汇报材料
2022-09-04 6页
 SQL数据库语言的使用
SQL数据库语言的使用
2023-06-13 3页
 dbx处理器中文说明书
dbx处理器中文说明书
2023-07-02 25页
 浙江幼儿园装备规范方案(试行)
浙江幼儿园装备规范方案(试行)
2024-02-03 22页
 2015-2016年人教版小学二年级数学下册期中试卷
2015-2016年人教版小学二年级数学下册期中试卷
2024-01-31 5页
 机房、基站安全管理.doc
机房、基站安全管理.doc
2024-01-17 1页
 测绘师继续教育(2019年必修内容--技术)试卷及参考答案.doc
测绘师继续教育(2019年必修内容--技术)试卷及参考答案.doc
2022-12-09 13页
 创建“五好”党支部工作总结
创建“五好”党支部工作总结
2022-09-07 6页
 浙江大学远程教育2015年刑法分论在线作业答案
浙江大学远程教育2015年刑法分论在线作业答案
2022-08-30 15页

