
高中化学 课时分层作业10 溴、碘的提取 苏教版必修1
7页1、课时分层作业(十) 溴、碘的提取 (建议用时:45分钟)学业达标练1关于氧化还原反应的说法中正确的是()A失去电子的物质是氧化剂B氧化反应的本质是得电子C原子得到电子后,元素的化合价一定升高D有单质参加或生成的反应不一定是氧化还原反应D还原剂失去电子,化合价升高,发生氧化反应,氧化剂得到电子,化合价降低,发生还原反应,故A、B、C错误。3O22O3不是氧化还原反应。2下列对氧化还原反应的分析中,不合理的是 ()AMg变成MgO时化合价升高,失去电子,因此Mg在该反应中作还原剂BKMnO4受热分解时,Mn元素的化合价既升高,又降低,因此Mn元素既被氧化又被还原C反应CuSO42NaOH=Cu(OH)2Na2SO4不属于氧化还原反应D在反应2H2O2H2O2中,H2O既是还原剂,又是氧化剂【答案】B3下列反应中,氯元素被氧化的是()A2KClO32KCl3O2B2P5Cl22PCl5CMnO24HCl(浓),MnCl22H2OCl2DH2Cl22HClC氯元素被氧化时,氯元素的化合价升高。4下列化学反应中电子转移的表示方法正确的是()5下列电子转移的表示方法中正确的是()DA项,被氧化与被
2、还原标错;B项,得失不能用“”和“”代替;C项,失去和得到标错。6下列微粒中,只有氧化性的是()S2Fe2Fe3SHMgABCDC处于最高价,反应时化合价只能降低,作氧化剂,只有氧化性。7下列变化中需加入氧化剂才能实现的是 ()AH2SSO2BAsOAsOCCl2NaClODH2O2O2A加入氧化剂才能实现的变化肯定是物质所含元素化合价升高的变化,即肯定是氧化反应。H2SSO2,S元素被氧化,需加入氧化剂(如O2);AsOAsO,As元素被还原应加入还原剂;Cl2NaClO可通过Cl2与NaOH反应,属于自身氧化还原反应,不需加氧化剂;H2O2O2,H2O2自身分解生成O2。8一定条件下氨气和氧化铜可以发生如下反应:2NH33CuO3CuN23H2O,对此反应的分析合理的是()A该反应属于置换反应BNH3被氧化为N2C反应体现了金属铜的还原性D每生成1 mol H2O就伴随着1 mol电子转移BA项,单质与化合物反应生成新的单质和新的化合物的反应是置换反应,该反应不是置换反应;B项,在反应中NH3中3价的N元素变为N2中0价的N元素,化合价升高被氧化;C项,在反应中CuO中2价的Cu元
3、素变为单质Cu中的0价,化合价降低被还原,CuO作氧化剂,体现了CuO的氧化性;D项,在反应2NH33CuO3CuN23H2O中,每生成3 mol H2O转移6 mol电子,故生成1 mol H2O时转移2 mol电子。9已知反应:Cl22KBr=2KClBr2,KClO36HCl(浓)=3Cl2KCl3H2O,2KBrO3Cl2=Br22KClO3。下列说法正确的是()A反应都有单质生成,所以都是置换反应B氧化性由强到弱的顺序为KBrO3KClO3Cl2Br2C反应中还原剂与氧化剂的物质的量之比为61D中1 mol还原剂反应则氧化剂得到电子的物质的量为2 molB一种单质与一种化合物反应生成另一种单质和另一种化合物的反应称为置换反应,故反应不是置换反应,A项错误;根据氧化剂的氧化性强于氧化产物的氧化性,由题意可知,氧化性的强弱顺序为KBrO3KClO3Cl2Br2,B项正确;反应中参加反应的HCl为6 mol,其中作还原剂的HCl为5 mol,故还原剂HCl与氧化剂KClO3的物质的量之比为51,C项错误;在氧化还原反应中得失电子守恒,反应中还原剂为Cl2,根据反应前后氯元素化合价的
《高中化学 课时分层作业10 溴、碘的提取 苏教版必修1》由会员cl****1分享,可在线阅读,更多相关《高中化学 课时分层作业10 溴、碘的提取 苏教版必修1》请在金锄头文库上搜索。

烟花爆竹相关安全管理制度标准模板(七篇)
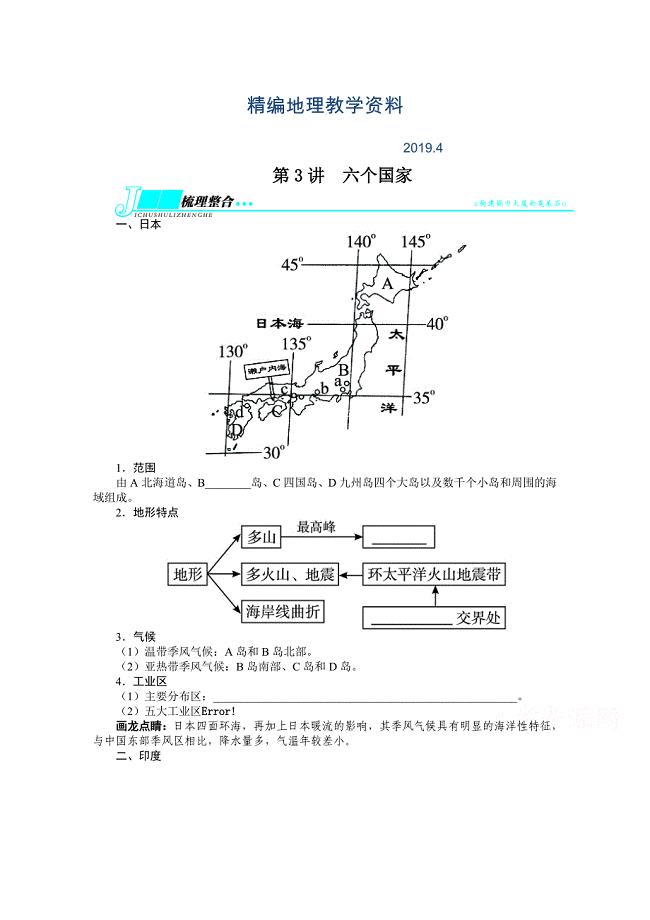
精编人教版高考地理一轮教学案:第17章第3讲六个国家含答案

保育员工作职责范文(10篇)

新目标英语七年级英语上册期末测试题

立法法基本知识测试题库

中级会计师预习财务管理判断题专练题

2023年市场营销学电大春会专

大学生向老师自我介绍(五)

心理咨询师简答题

物流实习自我鉴定15篇

超级稻—再生稻高产栽培技术 再生稻高产栽培技术

大学生家教实习报告
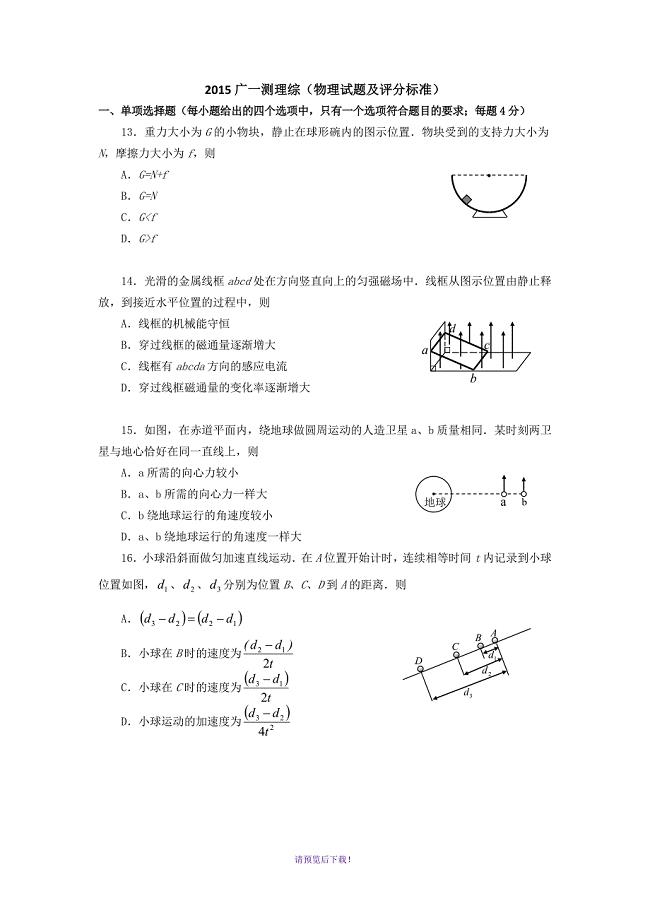
广州一模理综物理试题及答案

7年级上学期期中英语复习试题

2015年上半年北京企业法律顾问:宪法的指导思想考试题

【精品】陕旅版英语四年级上册 Unit 6 What Subjects Do They Have单元测试卷

汕尾电池精密结构件项目投资计划书【模板范本】

精品一设置中医临床科室达到综合医院中医临床科室基本标准国...

高中化学老师工作总结模板(二篇).doc

大班体育游戏教案《好玩的竹竿》
 炼钢厂实习工作总结
炼钢厂实习工作总结
2022-09-29 5页
 数电期末练习题参考
数电期末练习题参考
2023-04-11 30页
 一年级数学小学上学期第二次月考考试必考题青岛版
一年级数学小学上学期第二次月考考试必考题青岛版
2023-10-12 7页
 心理咨询师考试三级基础知识模拟试题及答案
心理咨询师考试三级基础知识模拟试题及答案
2023-08-05 30页
 年产10万吨石灰生产项目可行性研究报告
年产10万吨石灰生产项目可行性研究报告
2023-01-27 37页
 煤矿供电课程设计华康
煤矿供电课程设计华康
2023-03-24 14页
 八年级物理下册液体的压强练习无答案新人教版试题
八年级物理下册液体的压强练习无答案新人教版试题
2022-09-15 5页
 新制氢乏汽回收装置
新制氢乏汽回收装置
2022-11-19 7页
 中小企业贷款借款申请书
中小企业贷款借款申请书
2023-02-06 11页
 平安创建责任状2022年综治维稳责任书
平安创建责任状2022年综治维稳责任书
2022-08-09 3页

