
晶体的类型与性质课件课件1
42页1、思考 1、标准状况下氯化钠和氯化氢均不能导电,为什么熔融的氯化钠能导电,而液态氯化氢却不行? 2、二氧化碳和二氧化硅都是第四主族元素的最高价氧化物,为什么标准状况下二氧化碳呈气态而二氧化硅呈固态? 3、金刚石和红磷均是非金属单质,金刚石的硬度很大而红磷却质地较软。,明矾晶体,金刚石,红宝石(Al2O3),食盐晶体,冰晶,天然水晶,结论 决定晶体熔点、沸点、硬度、溶解性、导电性等的高低、大小、强弱的因素,主要是和构成晶体的粒子种类、粒子间的相互作用不同有关。,晶体的类型 分类依据:根据构成晶体粒子的种类、性质和粒子间的相互作用的大小分类。,一、离子晶体 定义:阴、阳离子间通过离子键结合而成的晶体叫离子晶体。,1、离子晶体的结构 在离子晶体中,阴、阳离子是按一定规律在空间排列的,因此离子晶体有一定的几何外型,这也决定了离子晶体中的阴、阳离子按照一定比例排列的。 实例分析:NaCl、CsCl,食盐晶体,食盐晶体结构模型,氯化铯晶体结构模型,2、离子晶体的性质 (1)在溶于水或熔化时,能电离出自由移动的阴、阳离子,可导电。 (2)硬度较大,难压缩,且较脆。 (3)具有较高的熔、沸点,原因是离子
2、键较强。,观察思考:请从离子键强弱的角度分析下表,结论:离子的电荷越高,半径越小,离子键就越强,熔、沸点也就越高。,二、分子晶体 思考: 碘晶体、二氧化碳晶体(干冰)、雪花晶体,这些常见的晶体是不是离子晶体?为什么?,1、 定义:分子间通过分子间作用力相互结合而成的晶体。 如:含氧酸、气态氢化物、大多数非金属氧化物(除SiO2)以及大多数非金属单质、稀有气体、大多数有机物等,在固态时都属分子晶体。,干冰晶体结构模型,2、分子晶体的性质 (1) 在固态和熔融状态时都不导电,只有那些极性很强的分子构成的晶体(如HCl等)溶解在极性溶剂(如水)中,因发生电离而导电。 (2)由于分子间作用力比共价键、离子键弱得多,所以分子晶体一般具有较低的熔点、沸点和较小的硬度。,实例分析:找出卤素单质、四卤化物的熔、沸点与相对分子质量的关系的规律,能否举出例子?,结论: 组成结构相似的分子,相对分子质量越大,分子间作用力越强,分子晶体的熔沸点就越高。,(3)“相似相溶”原理:非极性溶质一般能溶于非极性 溶剂;极性溶质一般易溶于极性溶剂。如HCl、NH3等易 溶于水中,而 Br2、I2 等易溶于苯、四氯化碳中
《晶体的类型与性质课件课件1》由会员n****分享,可在线阅读,更多相关《晶体的类型与性质课件课件1》请在金锄头文库上搜索。

项目二财务管理价值观念

山东省安全生产风险分级管控与隐患排查治理信息化系统交流材料-2018.9.26

人教版高中地理必修3第一章地理环境与区域发展第二节《地理信息技术在区域地理环境研究中的应用》

第三章2房地产抵押贷款-固定利率抵押贷款
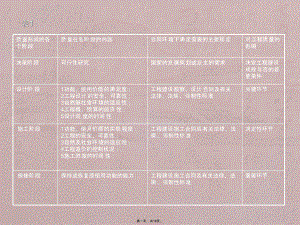
第八章工程质量法律制度

第25讲家庭电路与安全用电

餐厅点餐系统项目

项目7水箱水位控制

框架完整个人年度工作总结范文模板

科目名称-国土交通省

金融工程09课件

高校自主招生之结构化面试

房地产私募股权投资基金(PE)专题研究.

房地产基础知识培训2012

第一章食品检测技术基础知识

第10章网站设计与建设综合实例

第5章尝试迷人的机器人项目机器人灭火项目

自考英语二unit3

企业人力资源管理师第六章劳动法与劳动关系管理

第三章市场营销宏观环境分析
 就业能力适应能力
就业能力适应能力
2024-04-09 27页
 少儿美术绘画课件(5-6岁)可爱的小兔子
少儿美术绘画课件(5-6岁)可爱的小兔子
2024-04-09 29页
 就业能力探索
就业能力探索
2024-04-09 27页
 少儿创意美术-胡桃夹子
少儿创意美术-胡桃夹子
2024-04-09 27页
 少儿美术课件启蒙班7漂亮的瀑布
少儿美术课件启蒙班7漂亮的瀑布
2024-04-09 27页
 尺寸精度设计基础
尺寸精度设计基础
2024-04-09 28页
 少儿创意美术-威尼斯贡多拉
少儿创意美术-威尼斯贡多拉
2024-04-09 27页
 少儿创意美术-海中的鲸鱼
少儿创意美术-海中的鲸鱼
2024-04-09 34页
 少儿创意美术-冰糖葫芦
少儿创意美术-冰糖葫芦
2024-04-09 27页
 少儿创意美术-古埃及壁画
少儿创意美术-古埃及壁画
2024-04-09 27页

