
化工热力学复习习题
48页1、实验得(实测),一p、V、T、CP是流体的最基本性质,是热力学计算基础,查找文献,计算 (由第二章介绍方法计算),二pVT数据的计算,1理想气体:pV=RT (1mol)低压、高温 2真实气体:主要有两种计算方法,一种EOS法,另一种普遍化关系法。,第二章 流体的pVT关系,EOS法:Virial,VDW,RK,SRK,PR Eq 。有关真实气体计算的状态方程式很多,目前已提出的不下300种,实际应用的也有150种之多,我们主要介绍以上这些,重点掌握Virial Eq,Virial Eq,球形分子(Ar,Ke,Xe) =0,普遍化关系式法, 两参数通用Z图, pitzer三参数通用关系式,由Tr,Pr查图得Z值,A 普维法: 以两项维里方程为基础,图29曲线上方,或Vr2时用,,pitzer提出的三参数通用关系式有两个 普维法 普压法,运用三参数普遍化关系式计算时,一定是要注意普维法和普压法的应用条件。,B. 普压法:图29曲线下方,或Vr2时用,Z0,Z1,2-7 2-8,图,查值,普遍化关系式法重点是三参数,判断、选择、填空题,1、纯物质的饱和液体的摩尔体积随着温度升高而增大,饱和
2、蒸汽的摩尔体积随着温度的升高而减小。 2、物质的偏心因子是由蒸气压定义的,此具有压力的单位。 3、纯物质的三相点温度随着所处压力的不同而改变。 4、纯物质由液体变成蒸气,必须经过汽化的相变化过程。 5、纯物质的Virial系数,如B、C等,仅是温度和压力的函数。 6、Virial方程中B12反映了异分子间的相互作用力,因此B12=0的气体必定是理想气体混合物。 7、偏心因子是从( )定义的。 (A)分子的对称性 (B)蒸气压性质(C)分子的极性 8、T温度下的过热纯蒸汽的压力p( )。 (A)大于该温度下的饱和蒸气压 (B)小于该温度下的饱和蒸气压 (C)等于该温度下的饱和蒸气压,B,B,1、纯物质的临界点关系满足( ),( )。 2、正丁烷的偏心因子=0.193,临界压力pC=3.797MPa,则在Tr=0.7时的蒸气压为(0.243 MPa)。 3、写出你所知道的气体状态方程的名称( 4个即可)。 4、维里系数B的物理意义是(两分子间的相互作用力),它的数值通常与(系统的温度)有关。 5、对比态原理是指(任何气体或液体的对比体积(或压缩因子)是相同,同时其他对比热力学性质之间也存在
3、着较简单的对比态关系)。,第三章 流体的热力学性质,一.基本概念 1强度性质 2广度性质(容量性质) 广度性质若为单位质量的性质,则为强度性质,如mol热力学能能,偏mol性质。 3偏微分、全微分、点函数、状态函数的概念 4剩余性质的定义式,原始函数关系式 四大微分方程式 Maxwell关系式,二.热力学关系式,热力学性质的关系式,最基本的是四大微分方程,由四大微分方程式,据数学关系推导出的Maxwell关系式。,dG=-SdT+Vdp,dU=TdS-pdV,H=U+pV,G=H-TS,dH=TdS+Vdp,A=U-TS,dA=-SdT-pdV,第一、二关系式,热一、二律, 推导过程能看懂会推导,计算方法要掌握,基本微分方程式必须牢记。 热力学图表要求能认识图,会查找数据,特别是TS图。,三热力学图表,pT图,TS图, lnpH图,HS图 水蒸汽表 会查用。,要求:,的变化规律,等V线,TS图,VLE区来历,三相线来历,等p线,等H线,M=Mgx+(1-x)Ml,S=Sgx+(1-x)Sl,H=Hgx+(1-x)Hl,判断、选择、填空题,1、对于混合系统,偏离函数中的参考态是(与研究态
4、同温、同组成的理想气体混合物)。 2、偏离函数是两个等温状态的性质之差,因而不能用来计算性质随着温度的变化。 3、偏离函数法计算热力学性质的方便之处在于利用了理想气体的性质。 4、偏离函数是指(气体在真实状态下的热力学性质与相同温度下,当气体处于理想气体状态下热力学性质之差,表达为:MR=M-Mig其中M=U、V、H、A、G、S等)。,C,p,V,1,3(T降低),4,2,5,1)过热蒸汽等温冷凝为过冷液体; 2)过冷液体等压加热成过热蒸汽; 3)饱和蒸汽可逆绝热膨胀; 4)饱和液体恒容加热; 5)在临界点进行的恒温膨胀,C,T,S,1,3(T降低),4,2,5,1)过热蒸汽等温冷凝为过冷液体; 2)过冷液体等压加热成过热蒸汽; 3)饱和蒸汽可逆绝热膨胀; 4)饱和液体恒容加热; 5)在临界点进行的恒温膨胀,第四章 流体混合物(溶液)的热力学性质,一. 基本概念 1偏mol性质定义 2化学位 3混合性质变化: 4超额性质: 5混合过程的超额性质变化 6恒T、P下,GD Eq,化学位,偏摩尔性质,偏摩尔内能:在T、P和其它组分量nj均不变情况下,向无限多的溶液中加入1mol的组分i所引起
《化工热力学复习习题》由会员n****分享,可在线阅读,更多相关《化工热力学复习习题》请在金锄头文库上搜索。

项目二财务管理价值观念

山东省安全生产风险分级管控与隐患排查治理信息化系统交流材料-2018.9.26

人教版高中地理必修3第一章地理环境与区域发展第二节《地理信息技术在区域地理环境研究中的应用》

第三章2房地产抵押贷款-固定利率抵押贷款
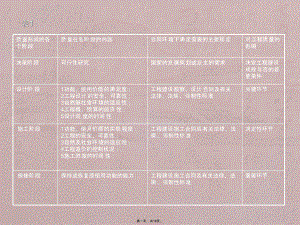
第八章工程质量法律制度

第25讲家庭电路与安全用电

餐厅点餐系统项目

项目7水箱水位控制

框架完整个人年度工作总结范文模板

科目名称-国土交通省

金融工程09课件

高校自主招生之结构化面试

房地产私募股权投资基金(PE)专题研究.

房地产基础知识培训2012

第一章食品检测技术基础知识

第10章网站设计与建设综合实例

第5章尝试迷人的机器人项目机器人灭火项目

自考英语二unit3

企业人力资源管理师第六章劳动法与劳动关系管理

第三章市场营销宏观环境分析
 就业能力适应能力
就业能力适应能力
2024-04-09 27页
 少儿美术绘画课件(5-6岁)可爱的小兔子
少儿美术绘画课件(5-6岁)可爱的小兔子
2024-04-09 29页
 就业能力探索
就业能力探索
2024-04-09 27页
 少儿创意美术-胡桃夹子
少儿创意美术-胡桃夹子
2024-04-09 27页
 少儿美术课件启蒙班7漂亮的瀑布
少儿美术课件启蒙班7漂亮的瀑布
2024-04-09 27页
 尺寸精度设计基础
尺寸精度设计基础
2024-04-09 28页
 少儿创意美术-威尼斯贡多拉
少儿创意美术-威尼斯贡多拉
2024-04-09 27页
 少儿创意美术-海中的鲸鱼
少儿创意美术-海中的鲸鱼
2024-04-09 34页
 少儿创意美术-冰糖葫芦
少儿创意美术-冰糖葫芦
2024-04-09 27页
 少儿创意美术-古埃及壁画
少儿创意美术-古埃及壁画
2024-04-09 27页

