
初级中学化学基础知识资料预习复习提纲
15页1、初中化学基础知识复习提纲一、应掌握的知识点1、 分子是保持化学性质的最小微粒。原子是化学变化中的最小微粒。2、 元素是具有相同核电荷数(即质子数)的同一类原子的总称。3、 分子和原子的主要区别是在化学反应中,分子可分,原子不可分。4、 元素的化学性质主要决定于原子的最外层电子数。5、 在原子中,质子数 = 核电荷数 = 核外电子数。6、 相对原子质量 = 质子数 + 中子数7、 镁离子和镁原子具有相同的质子数或核电荷数。8、 地壳中含量最多的元素是氧元素。最多的金属元素是铝元素。9、 决定元素的种类是质子数或核电荷数。10. 空气是由几种单质和几种化合物组成的混合物。11. 石油、煤、天然气都是混合物。 (天然气主要成分CO 和CH4)12. 溶液都是混合物。例如:稀硫酸、食盐水、石灰水等。(溶液的质量等于溶质的质量加上溶剂的质量)13. 氧化物是由两种元素组成的,其中一种是氧元素的化合物。(氧化物是纯净物)14. 化学变化的本质特征是有新物质生成。15. 燃烧、铁生锈、食物变质等都是化学变化。16. 化学反应的基本类型是化合反应、分解反应、置换反应、复分解反应。 (基本类型不包括氧化
2、和还原反应)17. 金属活动性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Ag Pt Au18. 具有还原性的物质是H2、C、CO。其中属于单质的是C、H2。属于化合物的是CO。(单质、化合物都是纯净物)19. 燃烧、缓慢氧化、自燃的相同点是都是氧化反应。20. 在化学反应前后,肯定不变的是原子的种类和数目、元素的种类、反应前后物质的总质量。肯定变化的是物质的种类和分子的种类。21. 2H2表示两个氢分子;2H表示两个氢原子;2H+表示两个氢离子。22. 溶液都是均一、稳定的混合物。溶液中各部分的性质相同。溶液不一定是无色的。23. 溶液在稀释前后保持不变的是溶质的质量。(溶解度 =溶质的质量/溶剂的质量注:不是溶液的质量*100%,质量分数=溶质的质量/溶液的质量)24. 酸的pH7;如:NaOH、Ca(OH)2中性溶液pH=7。如:水、NaCl25. Mg原子的原子结构示意图 +12 2 8 2 ,该原子中的质子数为12,核电荷数为12,核外电子数为12,最外层电子数为2,该原子在化学反应中易失电子,成为阳离子。(最外层电子小于4易失电子是阳离子,
3、反正是阴离子。最外层等于4的既易得也易失电子,要根据情况而定)26. 可燃物燃烧的两个条件是(1)可燃物与氧气充分接触;(2)温度达到或超过可燃物的着火点。27. 构成物质的基本微粒是分子、原子、离子。28. 酸有盐酸HCl、硫酸H2SO4、硝酸HNO3。29. 碱有氢氧化钠NaOH、氢氧化钙Ca(OH)2等。30. 化合价口诀:一价氢氯钾钠银,二价氧钙钡镁锌,三铝四硅五价磷;碳二四,铁二三,二四六硫都齐全,铜汞二价最常见。(其他口诀也可)31. 空气中的污染性气体有一氧化碳CO、二氧化碳CO2、二氧化氮NO2。32. 氢气在空气中燃烧的产物对空气没有污染。(2H2+O2=2H2O水不是污染物,所以没污染)33. 空气中按体积分数计算,最多的气体是氮气,占78%,其次是氧气,占21%。34. 可以使带火星的木条复燃的是氧气O2。(这也是检验收集氧气是否满了,用一根带火星的木条放入瓶口,看是否会复燃,若复燃说明收集满了。)35. 氧气是无色无味的气体,比空气略重,不易溶于水,液态氧和固态氧均为淡蓝色。(因为相对原子质量32比空气的相对原子质量29大,所以密度比空气的大)36. 硫在氧气中
4、燃烧发出蓝紫色火焰。硫在空气中燃烧发出淡蓝色火焰。37. 铁丝在氧气中燃烧火星四射,生成黑色固体。在做此实验时,应预先在瓶底放水或细砂,原因是防止熔融的生成物溅落,炸裂瓶底。38. 磷在氧气中燃烧,呈黄色火焰,生成大量的白烟。烟是固体。 (烟是固体小颗粒,雾是液体小液滴)39. 镁在氧气中燃烧发出耀眼的白光,生成白色固体。40实验室制取氧气所用的药品是(1)氯酸钾(白)和二氧化锰(黑色用来做催化剂)的混合物KCLO3=KCI+O2(2)高锰酸钾:其中在反应中二氧化锰做催化剂:2KMnO4=K2MnO4+MnO2+O2(3)双氧水的分解和二氧化锰2H2O2=2H2O+O241.水是由氢元素和氧元素组成的纯净物, 注意:组成和构成的区别42.氢气的用途有(1)治炼金属(还原性)(2)焊接金属(可燃性)(3)探空气球(比专轻)43实验室制取氢气所送用的药品是锌和稀硫酸44.实验室制取二氧化碳所选用的药品是石灰石和稀盐酸45.在天然物质中,硬度最大的是金刚石,可用来切割玻璃46所学物质中为黑色的是木炭c,氧化铜Cuo,二氧化锰MnO2,四氧化三铁Fe3O447.用墨书写的字画常年不色,是因为碳
《初级中学化学基础知识资料预习复习提纲》由会员不***分享,可在线阅读,更多相关《初级中学化学基础知识资料预习复习提纲》请在金锄头文库上搜索。
![电力设备预防性试验规章制度[2017年]](https://union.02img.goldhoe.com/2019-11/16/4667be4f-7732-484e-a02e-4246affcb5f8/pic1.jpg)
电力设备预防性试验规章制度[2017年]

电力设备预防性试验规章制度(2016)

电力设备销售技巧大全

电力行业项目工程设计资质分级

电力管线施工专项计划方针
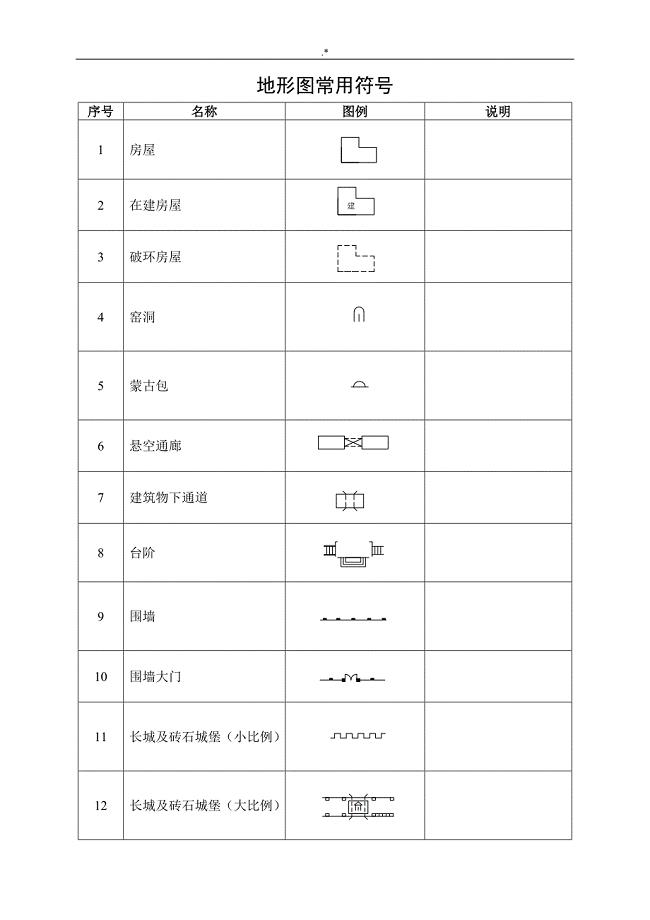
地形图普通符号(整编汇总)

地坪拆除修复施工方案方针

SL223-2008水利水电建设项目工程验收规章制度

RBT214-2017检验检测机构通常要求新编内审检查表

QUIC协议合约介绍

钢材采购招投标材料

风冷模块维护介绍资料

风控介绍资料(定版)

风景园林项目工程试题及其答案解析

电力设备采购合同协议文本范文样式(最佳)

电力设备安装项目工程投标书

电力三级及其以上施工安全风险识别,评估和预控清册

电力浅沟专项施工方案方针

电力设备交接和预防性试验规章制度

2017新课标全国卷3语文试题及其答案解析
 医用高等数学课件4-导数与中值定理练习-答案-(2012)
医用高等数学课件4-导数与中值定理练习-答案-(2012)
2023-02-28 2页
 共产党宣言稿子
共产党宣言稿子
2022-11-14 8页
 社会学概论00034密训资料(最新版)
社会学概论00034密训资料(最新版)
2022-11-08 12页
 马克思主义基本原理概论03709密训资料
马克思主义基本原理概论03709密训资料
2022-11-09 12页
 社会学概论00034考前资料
社会学概论00034考前资料
2022-11-08 16页
 社会学概论00034主观题汇总
社会学概论00034主观题汇总
2022-11-08 17页
 马克思主义基本原理概论03709主观题汇总
马克思主义基本原理概论03709主观题汇总
2022-11-08 15页
 英语(二)必备词汇表-4500单词
英语(二)必备词汇表-4500单词
2022-11-02 39页
 领导科学00320主观题汇总(最新版)
领导科学00320主观题汇总(最新版)
2022-11-02 17页
 行政管理学00277密训资料(最新版)
行政管理学00277密训资料(最新版)
2022-11-02 12页

