
化学反应原理方程式及重点
8页1、实用标准文案一、电解1.电解池两极放电顺序:阳极:活性电极S2-I-Br-Cl-OH-含氧酸根 阴极:Ag+Hg2+Fe3+Cu2+H+(酸)Sn2+Fe2+Zn2+H+(水)Al3+Mg2+Na+Ca2+K+2.用惰性电极电解硫酸、NaOH溶液、KNO3溶液阳极: 4OH- O2+2H2O+4e- 阴极:2H+2e-H2 总反应:2H2O 2H2+ O23.用惰性电极电解盐酸阳极:2Cl- Cl2+2e-阴极:2H+2e-H2 总反应:2HCl H2+ Cl24.用惰性电极电解饱和食盐水阳极:2Cl- Cl2+2e-阴极:2H+2e-H2 总反应:2NaCl+2H2O 2NaOH+H2+ Cl25.用惰性电极电解CuSO4溶液阳极:4OH- O2+2H2O+4e- 阴极:Cu2+2e-Cu总反应:2CuSO4+2H2O 2Cu+O2+ 2H2SO46.用惰性电极电解熔融Al2O3阳极:2O2- O2+4e-阴极:Al3+3e-Al总反应:2Al2O3 4Al+3O27.给铜钉镀铁,设计电池,指明电极材料,写出电极反应式阳极( 铁 )Fe Fe2+2e-阴极( 铜钉 )Fe2+2e-
2、Fe8.设计电池Cu+2H2O=Cu(OH)2+H2(用铜作阳极电解硫酸)阳极( 铜 )Cu Cu2+2e-阴极( 石墨 )2H+2e-H2总反应:Cu+2H2OCu(OH)2+H29、用铁作阳极电解NaCl溶液阳极:Fe Fe2+2e-阴极:2H+2e-H2总反应:Fe+2H2OFe(OH)2+H210、用银作阳极电解盐酸阳极:2Ag2Ag+2e-阴极:2H+2e-H2总反应:2Ag+2HCl2AgCl+H2二、电池1.铅蓄电池(硫酸为电解液)负极:Pb+SO42-PbSO4+2e-正极:PbO2+2e-+4H+ SO42-PbSO4+2H2O总反应:Pb+ PbO2+4H+2SO42-=2PbSO4+2H2O 2.氢氧燃料电池:硫酸电解液 KOH溶液 负极: H22H+2e- 负极:H2+2OH-2H2O+2e- 正极: O2+4H+4e-2H2O 正极:O2+2H2O+4e- 4OH- 总反应: 2H2+ O2=2H2O 总反应:2H2+ O2=2H2O 3.钢铁析氢腐蚀负极:Fe Fe2+2e-正极:2H+2e-H2总反应:Fe+2H+= Fe2+ H24.钢铁吸氧腐蚀负极:F
3、e Fe2+2e-正极:O2+2H2O+4e- 4OH-总反应:2Fe+ O2+2H2O=2Fe(OH)2其它反应:4Fe(OH)2 +O2+2H2O=4Fe(OH)35.MgAl硫酸负极(Mg):Mg Mg2+2e-正极(Al):2H+2e-H2总反应:Mg+2H+=Mg2+H26.MgAlNaOH溶液负极(Al):2Al2Al3+6e-正极(Mg):6H2O+6e-3H2+6OH-总反应:2Al+2OH-+6H2O=2Al(OH)4-+3H27、CH4O2硫酸负极:CH4+2H2OCO2+8H+8e-正极:2O2+8H+8e-4H2O总反应:CH4+2O2=CO2+2H2O8、CH4O2NaOH溶液负极:CH4+10OH-CO32-+7H2O+8e-正极:2O2+4H2O+8e-8OH-总反应:CH4+2O2+2OH-=CO32-+3H2O9、CH3OHO2硫酸负极:2CH3OH+2H2O2CO2+12H+12e-正极:3O2+12H+12e-6H2O总反应:2CH3OH+3O2=2CO2+4H2O10、CH3OHO2NaOH溶液负极:2CH3OH+16OH-2CO32-+12H2
《化学反应原理方程式及重点》由会员jiups****uk12分享,可在线阅读,更多相关《化学反应原理方程式及重点》请在金锄头文库上搜索。

建立安全生产长效机制-共创和谐平安输气管道

土石方爆破工程设计方案

康师傅百货商场制度汇编之退换货管理办法

庙头中学2012年中考百日誓师大会学生代表发言稿

围堰拆除爆破工程

华能洱源马鞍山风电场工程土石方爆破管理制度

国资委:全面开展管理提升活动-为培育世界一流企业奠定坚实基础

《专业技术人员职业发展与规划》电子书

应收票据审计方案
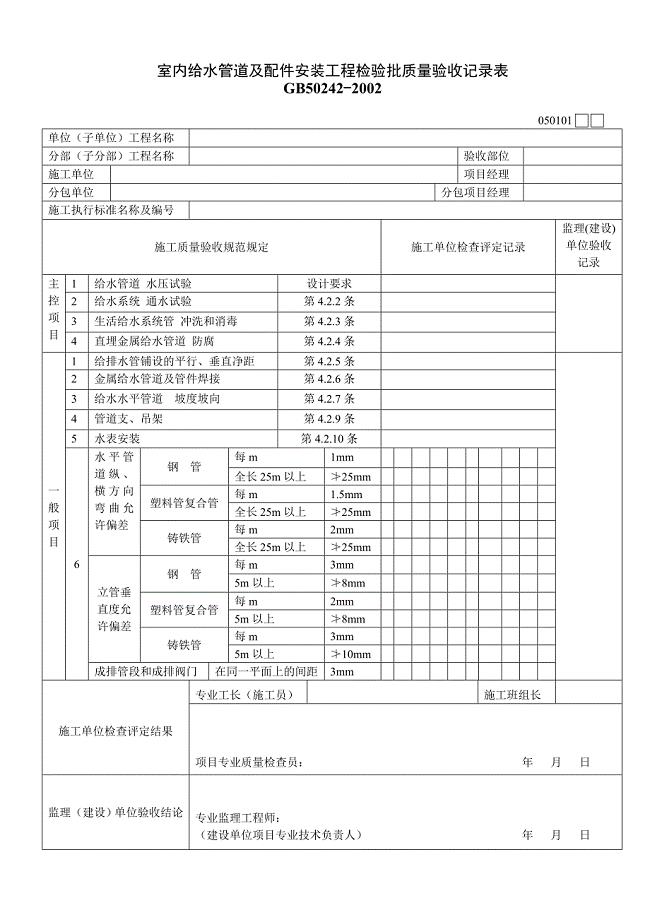
建筑给水排水与采暖工程质量验收用表

广播电视管理条例行政处罚裁量标准

广东电力系统调度运行操作管理规定

建筑给排水工程名词解释

幼儿园小班安全健康活动教案:宝宝误食后的急救

建业集团房屋建筑工程交房标准内容技术交底

建筑心理学论文(1)

康师傅百货商场制度汇编之工服管理程序009

建筑工程专业一级建造师继续教育培训结业报告20

廉洁风险防控回头看工作汇报材料

平台工作人员服务规范
 2024年安徽省芜湖市中考二模语文试卷【含答案】
2024年安徽省芜湖市中考二模语文试卷【含答案】
2024-04-24 10页
 2024届河北省邯郸市中考一模语文试题【含答案】
2024届河北省邯郸市中考一模语文试题【含答案】
2024-04-24 10页
 2024年(6月份)中考数学押题试卷【含答案】
2024年(6月份)中考数学押题试卷【含答案】
2024-04-24 25页
 2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024-04-24 10页
 辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
2024-04-23 4页
 第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
2024-04-23 10页
 江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
2024-04-23 19页
 江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
2024-04-23 10页
 江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
2024-04-23 16页
 小学六年级体育与健康测试题【含答案】
小学六年级体育与健康测试题【含答案】
2024-04-23 5页

