
化学药品注射剂与塑料包装材料(1)
23页1、化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)一、概述包装系统是指容纳和保护药品的所有包装组件的总和,包括直接接触药品的包装组件和次级包装组件,后者用于药品的额外保护。本指导原则主要针对直接接触药品的包装系统进行阐述。包装系统一方面为药品提供保护,以满足其预期的安全有效性用途;另一方面还应与药品具有良好的相容性,即不能引入可引发安全性风险的浸出物,或引入浸出物的水平符合安全性要求。是否需要进行相容性研究,以及进行何种相容性研究,应基于对制剂与包装材料发生相互作用的可能性以及评估由此可能产生安全性风险的结果。与口服制剂相比,吸入气雾剂或喷雾剂、注射液或注射用混悬液、眼用溶液或混悬液、鼻吸入气雾剂或喷雾剂等制剂,由于给药后将直接接触人体组织或进入血液系统,被认为是风险程度较高的品种;另外,大多液体制剂在处方中除活性成分外还含有一些功能性辅料(助溶剂、防腐剂、抗氧剂等),这些功能性辅料的存在,可促进包装材料中成分的溶出,因此与包装材料发生相互作用的可能性较大;按照药品给药途径的风险程度及其与包装材料发生相互作用的可能性分级,这些制剂被列为与包装材料发生相互作用可能性较高的高风险制
2、剂。对上述制剂必须进行药品与包装材料的相容性研究,以证实包装材料与制剂具有良好的相容性。本指导原则主要针对注射剂与塑料包装材料的相容性研究进行阐述,内容包括相容性研究的基本思路、相容性研究的主要内容、相容性试验内容与分析方法,以及试验结果分析与安全性评价等,旨在指导药品研发及生产企业系统、规范地进行药品与包装材料的相容性研究,在药品研发初期对包装材料进行选择,并在整个研发过程中对包装系统适用性进行确认,以有效避免包装材料可能引入的安全性风险,从而选择使用与药品具有良好相容性的包装材料。本指导原则主要阐述注射剂与塑料包装材料的相容性研究,其他剂型与包装材料的相容性研究不在本指导原则中详述,药品研发及生产企业可参照本指导原则的基本思路及主要研究内容,开展其他剂型与包装材料的相容性研究。本指导原则是基于直接接触药品的包装材料和容器管理办法(局令第13号),借鉴国外相关的指导原则及有关专著,同时根据我国药物研发的实际情况制定的;并将随着相关法规的不断完善以及药物研究技术要求的提高而进一步修订完善。二、相容性研究的基本思路对药品来说,包装应适用于其预期的临床用途,并应具备如下特性:保护作用、相容
3、性、安全性与功能性。相容性是药品包装必须具备的特性之一;相容性研究则是证明包装材料与药品之间没有发生严重的相互作用,并导致药品有效性和稳定性发生改变,或者产生安全性风险的过程;研究内容应包括包装材料对药品的影响以及药品对包装材料的影响。药品与包装材料的相容性研究,应在药品研发初期或是包装材料的选择时就开始进行,并贯穿于药品研发的整个过程。首先,应对包装组件所用材料以及添加剂等进行分析,然后通过初步的稳定性试验、加速试验和长期稳定性试验考察包装材料对药品稳定性的影响,并通过药物与包装材料的相容性研究考察包装材料中成分迁移进入药品的程度、包装材料对制剂中活性成分与功能性辅料的吸附程度,确认包装材料可以保证药品质量稳定,并与药品相容性良好。上市后,如需变更包装,则应评估该变更对药品质量可能产生的影响,并根据影响程度设计相关的试验进行研究,特别是应进行变更后包装材料与药品的相容性研究,证明这种变更不足以对药品质量以及包装材料功能性产生不可接受的变化,即不会导致安全性风险。除药品对包装材料产生影响并导致其功能性改变需要更换包材的情况外,相容性研究主要是针对包装材料对药品的影响进行。相容性研究过程
4、主要分为如下六个步骤:1)确定直接接触药品的包装组件;2)了解或分析包装组件材料的组成、包装组件与药品的接触方式与接触条件、生产工艺过程;3)分别对包装组件所采用的不同包装材料进行提取试验,对可提取物进行初步的风险评估并预测潜在的浸出物;4)进行制剂与包装容器系统的相互作用研究,包括迁移试验和吸附试验,获得包装容器系统对主辅料的吸附及在制剂中出现的浸出物信息;5)对制剂中的浸出物水平进行安全性评估;6)对药品与所用包装材料的相容性进行总结,得出包装系统是否适用于药品的结论。三、相容性研究的主要内容药品与包装材料相容性研究的内容主要包括三个方面:提取试验、相互作用研究(包括迁移试验和吸附试验)和安全性研究。相容性研究的试验材料可能是塑料材料,或者塑料组件,也可能是塑料包装容器。1. 提取试验提取试验是指采用适宜的溶剂,在较剧烈的条件下,对包装组件材料进行的提取试验研究;目的是通过提取试验,对可提取物(包装材料中溶出的添加物、单体及其降解物等)进行初步的风险评估并明确潜在的目标浸出物,并依据提取试验研究中获得的可提取物种类和水平信息,建立灵敏的、专属的分析方法,以指导后续的浸出物研究(迁移
《化学药品注射剂与塑料包装材料(1)》由会员jiups****uk12分享,可在线阅读,更多相关《化学药品注射剂与塑料包装材料(1)》请在金锄头文库上搜索。

建立安全生产长效机制-共创和谐平安输气管道

土石方爆破工程设计方案

康师傅百货商场制度汇编之退换货管理办法

庙头中学2012年中考百日誓师大会学生代表发言稿

围堰拆除爆破工程

华能洱源马鞍山风电场工程土石方爆破管理制度

国资委:全面开展管理提升活动-为培育世界一流企业奠定坚实基础

《专业技术人员职业发展与规划》电子书

应收票据审计方案
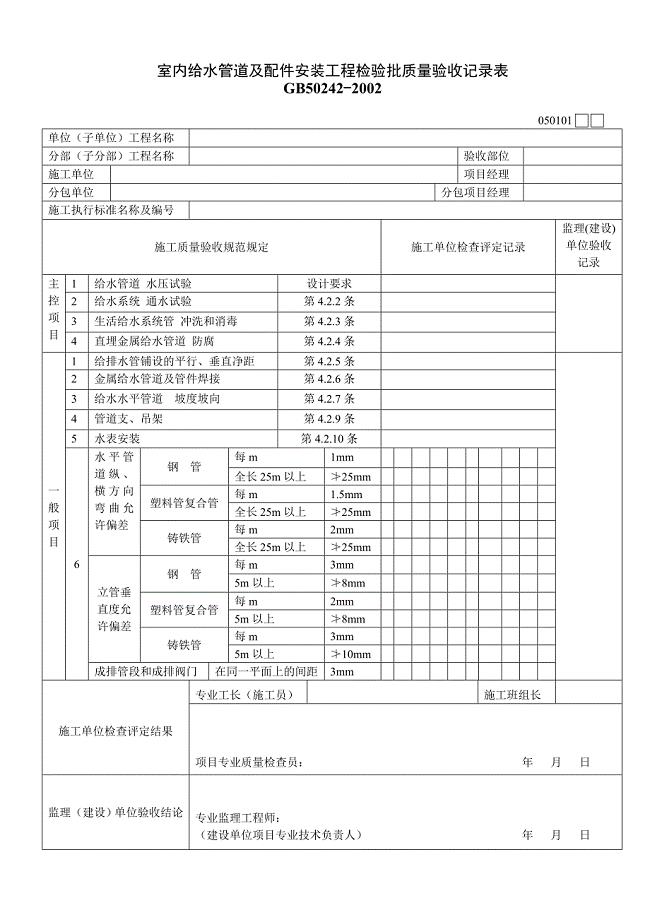
建筑给水排水与采暖工程质量验收用表

广播电视管理条例行政处罚裁量标准

广东电力系统调度运行操作管理规定

建筑给排水工程名词解释

幼儿园小班安全健康活动教案:宝宝误食后的急救

建业集团房屋建筑工程交房标准内容技术交底

建筑心理学论文(1)

康师傅百货商场制度汇编之工服管理程序009

建筑工程专业一级建造师继续教育培训结业报告20

廉洁风险防控回头看工作汇报材料

平台工作人员服务规范
 2024年安徽省芜湖市中考二模语文试卷【含答案】
2024年安徽省芜湖市中考二模语文试卷【含答案】
2024-04-24 10页
 2024届河北省邯郸市中考一模语文试题【含答案】
2024届河北省邯郸市中考一模语文试题【含答案】
2024-04-24 10页
 2024年(6月份)中考数学押题试卷【含答案】
2024年(6月份)中考数学押题试卷【含答案】
2024-04-24 25页
 2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024年江苏省扬州市宝应县中考一模语文试题【含答案】
2024-04-24 10页
 辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
辽宁省本溪市2022-2023学年高中下学期学业水平考试美术试题【含答案】
2024-04-23 4页
 第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
第六单元 正比例和反比例 (单元测试卷)苏教版数学六年级下册【含答案】
2024-04-23 10页
 江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
江苏省无锡市2024年七年级下学期期中数学调研试卷【含答案】
2024-04-23 19页
 江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
江苏省江阴市华士片2022-2023学年七年级下学期期中语文试题【含答案】
2024-04-23 10页
 江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
江苏省泰州兴化市2023-2024学年高一下学期期中考试语文试题【含答案】
2024-04-23 16页
 小学六年级体育与健康测试题【含答案】
小学六年级体育与健康测试题【含答案】
2024-04-23 5页

