
反应原理好题精选
110页1、21已知NO2和N2O4可以相互转化:2NO2N2O4(正反应为放热反应)。现将一定量NO2和N2O4的混合气体通入一体积为2L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。根据下图,回答下列问题:图中共有两条曲线X和Y,其中曲线 表示NO2浓度随时间的变化;a、b、c、d四个点中, 表示化学反应处于平衡状态的点是 。前10min内用NO2表示的化学反应速率(NO2) mol/(Lmin);15min时,反应2NO2N2O4在b点的浓度平衡常数Kb 反应进行至25min时,曲线发生变化的原因是 。35min时,反应2NO2N2O4在d点的浓度平衡常数Kd Kb(填、或)若要达到与最后相同的化学平衡状态,在25min 时还可以采取的措施是 。A加入催化剂 B缩小容器体积 C升高温度 D加入一定量的N2O4若在35min时,保持温度不变,快速缩小容器的体积至1L,气体的颜色变化过程是 21(1)X ; b和 d(2)0.04 10/9 充入了0.8mol NO2 (3)BD 先变深再变浅23(7分)某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。所查资料如下:碲(Te)
2、为固体,H2Te为气体,Te和H2不能直接化合生成H2Te等物质的量氧气、硫、硒、碲与H2反应的焓变情况如图所示:请回答下列问题: H2与硫化合的反应 热量(填“放出”或“吸收”)。 已知H2Te分解反应为熵增反应,请解释为什么Te和H2的反应不能自发发生 。在容积均为1 L(容器体积不可变)的甲、乙两个容器中,分别加入2 mol SO2、1 mol O2 和4 mol SO2、2 mol O2,在相同温度、催化剂下使其反应。最终达到平衡后,两容器中SO2转化率分别为甲、乙,甲容器中平衡常数表达式为 (用含甲的代数式表示),此时甲 乙(填“大于”、“小于”或“等于”)。23放出(1分);题中已知H2Te分解反应熵增反应,那么碲与氢气如果反应则其熵减小;由图可知:H2和Te的反应是一个吸热反应,即H0 。所以该反应不能自发发生。(3分)K = 甲2/(1甲)3(2分);小于(1分)25合成氨工业对化学工业和国防工业具有重要意义,对我国实现农业现代化起着重要作用。根据已学知识回答下列问题:已知:N2(g)+3H2(g)2NH3(g);H= 92.4kJ/mol合成氨工业中采取的下列措施不可
3、用勒沙特列原理解释的是 BC (填序号)。A. 采用较高压强(20Mpa50Mpa) B. 采用500的高温 C. 用铁触媒作催化剂 D. 将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2合成氨工业中采用了较高压强(20Mpa50Mpa),而没有采用100MPa或者更大压强,试解释没有这么做的理由:采用更大压强会要求使用能耐更大压强的设备,从而增加生产成本。随着合成氨研究的发展,希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),吸附在SCY内外表面上的金属钯多晶薄膜作为两个电极实现了常压、570条件下高转化率的电化学合成氨。其实验装置如图。在该装置中是将电能 能转化为化学 能。钯电极A的的名称是 阴极 。电极反应方程式为 。N2H4可以看做是NH3中的一个氢原子被氨基取代的产物。请写出N2H4的电子式_NH+ 2HCl NHCl_ ; 请写出和足量盐酸的反应化学方程式_已知:N2H4 (l) + O2(g) = N2(g) + 2H2O(g) ; H=621.74kJ/mol 2H2O2(l) = 2H2
《反应原理好题精选》由会员n****分享,可在线阅读,更多相关《反应原理好题精选》请在金锄头文库上搜索。

项目二财务管理价值观念

山东省安全生产风险分级管控与隐患排查治理信息化系统交流材料-2018.9.26

人教版高中地理必修3第一章地理环境与区域发展第二节《地理信息技术在区域地理环境研究中的应用》

第三章2房地产抵押贷款-固定利率抵押贷款
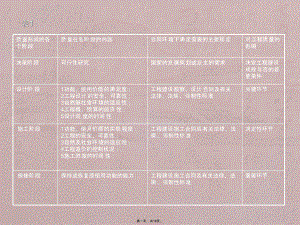
第八章工程质量法律制度

第25讲家庭电路与安全用电

餐厅点餐系统项目

项目7水箱水位控制

框架完整个人年度工作总结范文模板

科目名称-国土交通省

金融工程09课件

高校自主招生之结构化面试

房地产私募股权投资基金(PE)专题研究.

房地产基础知识培训2012

第一章食品检测技术基础知识

第10章网站设计与建设综合实例

第5章尝试迷人的机器人项目机器人灭火项目

自考英语二unit3

企业人力资源管理师第六章劳动法与劳动关系管理

第三章市场营销宏观环境分析
 学校食堂管理方案
学校食堂管理方案
2022-12-12 6页
 三八妇女节教师代表演讲稿
三八妇女节教师代表演讲稿
2023-04-15 6页
 2022关于护士述职报告锦集7篇
2022关于护士述职报告锦集7篇
2023-03-08 21页
 2023年新郎婚礼答谢词通用15篇
2023年新郎婚礼答谢词通用15篇
2022-07-30 12页
 中华魂演讲稿模板集合5篇
中华魂演讲稿模板集合5篇
2023-01-18 13页
 (可编辑)大学生专业实习报告10篇
(可编辑)大学生专业实习报告10篇
2023-08-01 34页
 从青啤的发展战略调整看中国啤酒工业未来发展方向(阅)
从青啤的发展战略调整看中国啤酒工业未来发展方向(阅)
2023-06-04 7页
 2023年季运动会广播稿集锦15篇(可编辑)
2023年季运动会广播稿集锦15篇(可编辑)
2022-11-17 29页
 实用的开学典礼主持词3篇
实用的开学典礼主持词3篇
2023-11-13 12页
 天的风筝小学作文5篇
天的风筝小学作文5篇
2022-12-07 6页

