
化学二轮复习 元素及其化合物最佳复习策略
60页1、元素及其化合物最佳复习策略,一 如何记忆和运用知识 从实践中来,到实践中去。,例1、有下图所示的反应关系,A是中学常见的无机物, A、B、C中含有同一种元素R,不含R的产物已 经略去。 (1)A与NaOH溶液反应,既可只生成B,又可只生成C, 还可生成B+C。写出符合上述反应关系的A的两种不 同类物质的分子式_; (2)若A与NaOH无论以何种物质的量之比反应,其产物 必有B+C,则A的分子式可能是_, R在A、B、C中的化合价必须满足的条件是_。,分析: 此题学生思维的重点是考虑A是什么?苦思冥想,物质一个一个的从脑子里向外崩。,本质: 学生没有掌握元素化合物的学法,没有掌握物质通性的学法!,金属,非金属,酸性 氧化物,碱性 氧化物,碱,酸,盐,盐,盐,盐+水,盐+碱,盐+酸,盐+盐,盐+金属,盐+氢气,八点图,金属,碱氧,碱,盐,非金属,酸氧,酸,盐,盐+金属,盐+非金属,盐,盐+水,盐+碱,盐+酸,盐+盐,水,本图蕴含着: 5个五(5种物质有五条通性) 2个三(2种物质有三条通性),本图蕴含着: 5个五(5种物质有五条通性) 2个三(2种物质有三条通性),金属 非金属 酸 碱 盐
2、,酸性氧化物 碱性氧化物,如:非金属具有五条通性:,1、与金属:,2Na + Cl2 2NaCl,点燃,H2 + Cl2 2HCl,点燃,H2O+Cl2 HCl+HClO,2、与非金属:,3、与水:,4、与碱:,5、与盐:2NaBr+Cl2=2NaCl+Br2 2KI+Cl2=2KCl+I2,金属有五条通性 1.与非金属 如Na 2.与金属 3.与水 4.与酸 如Na 5.与盐 如 Na与CuSO4溶液 先与水反应,再与盐与反应,酸有五条通性 1.指示剂 2.与金属 3.与碱性氧化物 Na2O 4.与碱 5.与盐 如AgNO3,碱有五条通性:,1、指示剂: 2、与非金属: 3、与酸氧:如CO2 4、与酸:H3PO4 H2S 5、与盐:如AlCl3 NaH2PO4,盐有五条通性 1.与金属 如Fe与CuSO4溶液反应 2.与非金属(如NaBr溶液与Cl2 )反应 3.与酸 4.与碱(如NaOH溶液与NaHCO3)反应 5.与盐反应 如NaAlO2与AlCl3溶液,碱性氧化物有三条通性 1.与水 如Na2O 2.与酸性氧化物(如CO2、SO2 )反应 3.与酸 酸性氧化物有三条通性 1.与
3、水 如CO2 2.与碱性氧化物(如Na2O )反应 3.与碱反应,例1、有下图所示的反应关系,A是中学常见的无机物, A、B、C中含有同一种元素R,不含R的产物已 经略去。 (1)A与NaOH溶液反应,既可只生成B,又可只生成C, 还可生成B+C。写出符合上述反应关系的A的两种不 同类物质的分子式_; (2)若A与NaOH无论以何种物质的量之比反应,其产物 必有B+C,则A的分子式可能是_, R在A、B、C中的化合价必须满足的条件是_。,第一问可选:酸性氧化物、 多元弱酸、 盐(如铝盐); CO2、SO2 H2S AlCl3 第二问可选:非金属(如S、Cl2) R元素在A中的化合价处于B、C中化合价之间(岐化反应) 启示: 学习元素化合物必须掌握物质的通性: 八点图、氧化还原等。,例1、有下图所示的反应关系,A是中学常见的无机物, A、B、C中含有同一种元素R,不含R的产物已 经略去。 (1)A与NaOH溶液反应,既可只生成B,又可只生成C, 还可生成B+C。写出符合上述反应关系的A的两种不 同类物质的分子式_; (2)若A与NaOH无论以何种物质的量之比反应,其产物 必有B+C,则A
4、的分子式可能是_, R在A、B、C中的化合价必须满足的条件是_。,CO2或SO2 H2S AlCl3,S、Cl2,R元素在A中的化合价处于B、C化合价之间,例2 X、Y、Z是主族元素的单质,U、V是化合物。 它们会有如下反应(式中的反应系数和条件均已略去): X+UV+Y X+ZV Y+ZU (1)若X、Y的组成元素不是同一族,请写出符合式 的3个不同的化学方程式,并要求3个式子中的3种X 和3种Y,全部由不同族的元素组成。 _。 (2)今有某化合物W,它跟化合物U或CO2反应,都能 生成单质Y。符合题设的3个反应式关系的单质X是_,单质Y是_,单质Z是_,化合物 W为_。,例2 X、Y、Z是主族元素的单质,U、V是化合物。 它们会有如下反应(式中的反应系数和条件均已略去): X+UV+Y X+ZV Y+ZU (1)若X、Y的组成元素不是同一族,请写出符合式 的3个不同的化学方程式,并要求3个式子中的3种X 和3种Y,全部由不同族的元素组成。 _。 (2)今有某化合物W,它跟化合物U或CO2反应,都能 生成单质Y。符合题设的3个反应式关系的单质X是_,单质Y是_,单质Z是_,化合物 W
《化学二轮复习 元素及其化合物最佳复习策略》由会员n****分享,可在线阅读,更多相关《化学二轮复习 元素及其化合物最佳复习策略》请在金锄头文库上搜索。

项目二财务管理价值观念

山东省安全生产风险分级管控与隐患排查治理信息化系统交流材料-2018.9.26

人教版高中地理必修3第一章地理环境与区域发展第二节《地理信息技术在区域地理环境研究中的应用》

第三章2房地产抵押贷款-固定利率抵押贷款
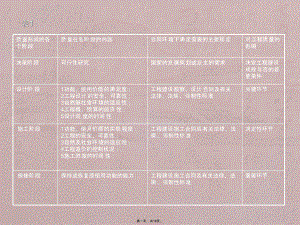
第八章工程质量法律制度

第25讲家庭电路与安全用电

餐厅点餐系统项目

项目7水箱水位控制

框架完整个人年度工作总结范文模板

科目名称-国土交通省

金融工程09课件

高校自主招生之结构化面试

房地产私募股权投资基金(PE)专题研究.

房地产基础知识培训2012

第一章食品检测技术基础知识

第10章网站设计与建设综合实例

第5章尝试迷人的机器人项目机器人灭火项目

自考英语二unit3

企业人力资源管理师第六章劳动法与劳动关系管理

第三章市场营销宏观环境分析
 优质护理培训课件
优质护理培训课件
2023-12-11 28页
 怎么练好护理操作课件
怎么练好护理操作课件
2023-12-11 28页
 面瘫的治疗与护理课件
面瘫的治疗与护理课件
2023-12-11 27页
 脑卒中患者护理课件模板
脑卒中患者护理课件模板
2023-12-11 31页
 护理反向交班课件
护理反向交班课件
2023-12-11 27页
 护理案例比赛课件题目
护理案例比赛课件题目
2023-12-11 27页
 医院icu护理课件
医院icu护理课件
2023-12-11 33页
 乙肝的护理课件
乙肝的护理课件
2023-12-11 28页
 中药坐浴护理课件
中药坐浴护理课件
2023-12-11 26页
 口腔护理课件题目
口腔护理课件题目
2023-12-11 29页

