
上市后药物安全性及疗效评估相关活动 -1
21页1、上市后药物安全性及疗效评估相关活动上市后药物安全性及疗效评估相关活动上市后药物安全性及疗效评估相关活动上市后药物安全性及疗效评估相关活动 - - 法律法规及如何遵循 Anders Dejgaard MD. , 医学博士, 副总裁, 首席医学官 诺和诺德总部 全球研发部 内容概要内容概要 为什么进行上市后研究 方法学 指南及法规 制药业如何执行 临床经验临床经验 对新上市药物而言 1期临床试验:10-100名健康受试者,暴露时间一般1个月或更短 2期临床试验:200-300名患者,暴露时间一般3个月或更短 3期临床试验:3000-4000名患者,暴露时间1-2年 1-3期临床试验中暴露人群 年龄,性别,种族,共患疾病均有一定限制,因而不能代表可能接受该 药治疗的全部人群 来自不同地区 一些特殊人群被排除在外(如:儿童,孕妇) 伴有某些合并疾病的人群被排除在外 接受某些合并用药的人群被排除在外 临床研发的改进临床研发的改进 3期临床研究的入选条件更加宽泛 更多合并疾病 合并用药 全球入选 个体化治疗 更加灵活的设计以包括更多“相关”受试者及不同剂量,如:适应性设 计 很早期阶段即关注风险问
2、题- 甚至在临床前阶段 从2期-3期以及3期-4期的无缝连接 在制药企业内部及企业之间更为开放地分享关于安全性的经验 要求要求 暴露时间 患者人数 药物批准 上市后 1-3期临床 然而然而 - 我们需要上市后研究我们需要上市后研究 “没有任何一种活性药 物完全没有风险。这 些与药物的治疗作用 相关联的风险可能并 不是至关重要的或者 是在可以被接受的范 围内。而且,并非这 些风险在药物上市前 即能够被认知。” 英国药物安全委员会,1970年报道 进行上市后研究的原因进行上市后研究的原因 对有条件获得批准上市的承诺 新的适应症 产品线延伸 新的疾病 新的适用人群:儿童,孕妇,老年人 产品定位相关研究 药物警戒 药物警戒药物警戒 - 发现,评价,理解以及预防不良反应或其他医学相关问题 的科学及活动 发现,评价,理解以及预防不良反应或其他医学相关问题 的科学及活动 欧洲制药工业协会联合会欧洲制药工业协会联合会(EFPIA)法规法规 干预性研究干预性研究ICH GCP指南指南 非干预性研究:非干预性研究: 科学目的科学目的 根据指南制定方案根据指南制定方案 酬劳酬劳 伦理委员会审阅伦理委员会审阅
《上市后药物安全性及疗效评估相关活动 -1》由会员n****分享,可在线阅读,更多相关《上市后药物安全性及疗效评估相关活动 -1》请在金锄头文库上搜索。

项目二财务管理价值观念

山东省安全生产风险分级管控与隐患排查治理信息化系统交流材料-2018.9.26

人教版高中地理必修3第一章地理环境与区域发展第二节《地理信息技术在区域地理环境研究中的应用》

第三章2房地产抵押贷款-固定利率抵押贷款
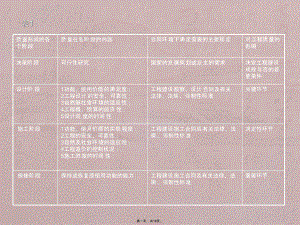
第八章工程质量法律制度

第25讲家庭电路与安全用电

餐厅点餐系统项目

项目7水箱水位控制

框架完整个人年度工作总结范文模板

科目名称-国土交通省

金融工程09课件

高校自主招生之结构化面试

房地产私募股权投资基金(PE)专题研究.

房地产基础知识培训2012

第一章食品检测技术基础知识

第10章网站设计与建设综合实例

第5章尝试迷人的机器人项目机器人灭火项目

自考英语二unit3

企业人力资源管理师第六章劳动法与劳动关系管理

第三章市场营销宏观环境分析
 差不多先生传 展练案
差不多先生传 展练案
2024-02-03 3页
 东北农业大学21春《证券投资学》离线作业一辅导答案84
东北农业大学21春《证券投资学》离线作业一辅导答案84
2024-01-19 11页
 2014年全国高校移动互联网应用开发创新大赛
2014年全国高校移动互联网应用开发创新大赛
2023-11-19 14页
 北京语言大学22春《高级写作》离线作业一及答案参考75
北京语言大学22春《高级写作》离线作业一及答案参考75
2023-10-06 15页
 中国医科大学21秋《护理中的人际沟通学》平时作业一参考答案10
中国医科大学21秋《护理中的人际沟通学》平时作业一参考答案10
2022-08-13 15页
 高中化学推断题(经典)
高中化学推断题(经典)
2023-04-04 37页
 南开大学21春《广告学原理》离线作业一辅导答案62
南开大学21春《广告学原理》离线作业一辅导答案62
2024-01-13 11页
 吉林大学21春《行政组织学》离线作业一辅导答案88
吉林大学21春《行政组织学》离线作业一辅导答案88
2023-02-22 11页
 内容为王语境下我国手机电视发展现状与对策的思考
内容为王语境下我国手机电视发展现状与对策的思考
2023-11-20 5页
 福建师范大学22春《运动生理学》离线作业一及答案参考36
福建师范大学22春《运动生理学》离线作业一及答案参考36
2022-10-07 13页

