
高考化学专题复习:碱金属
6页1、高考化学专题复习:碱金属一、考纲要求一、考纲要求 1.掌握钠的重要性质,了解钠的保存和重要用途. 2.掌握钠的氧化物的性质,钠的重要化合物的用途及 Na2CO3与 NaHCO3的联 系与区别. 3.掌握碱金属的性质,理解碱金属原子结构与性质递变规律,掌握用焰色反应 检验金属钠和钾及其离子的操作技能. 二、知识结构二、知识结构 1.碱金属元素原子结构、单质性质、制法: 名称和符号锂(Li)钠(Na)钾(K)铷(Rb)铯 Cs 原子序数311193755 原子结构简 图电子式LixNaxKxRbxCsx 主要化合价+1+1+1+1+1 相同点最外层电子数相同,都是 1 个电子 不同点原子核外电子层灵敏不同,依次增多 原子半径依次递增 离子半径依次递增 金属活动性 依次递增 单质还原性 依次递增结构阳离子氧化 性依次递减颜色和状态 银白色固体 密度0534/cm31.97/cm30.86g/cm31.532g/cm31.879g/cm3 熔点依次递减物 理 性 质沸点依次递减跟氧气反应2Li+O2 2LiO4Na+O2 2Na2O 2Na+O2 Na2O22K+O2 K 2O2 K+O2 K
2、O2Rb+O2 RbO2Cs+O2 CsO2跟卤素反应 2M+X2 2MX(M、X2表示碱金属、卤素) 跟硫反应2M+S M2S 与水反应2M+2H2O 2MOH+H2 反应剧烈程度:Li 与酸反应2M+2H+ 2M+H2 与盐溶液反 应如 (CuSO4)2M+2H2O+CuSO4 M2SO4+Cu(OH)2 +H2 化 学 性 质制法2MCl 2M+Cl2 (K:Ka+KCl 850 K+NaCl )2.钠的氧化物和氢氧化物的性质和制法: 名称和化 学式氧化钠(Na2O)过氧化钠(Na2O2)氢氧化钠(NaOH)颜色和状 态白色固体淡黄色固体无色固体类别碱性氧化物 离子化合 物过氧化物 离子化合物 碱 离子化合物电子式Na+ Na+Na+ 2Na+Na+ H- 氧元素化 合价-2-1-2化学键离子键离子键 非极性键离子键 极性键 稳定性不稳定比 Na2O 稳定离子键 极性键与水反应Na2O+H2O 2NaOH 2Na2O2+2H2O 4NaOH+ O2 不反应与酸反应Na2O+2HCl 2NaCl +H2O2NaO2+4HCl 4NaCl +O2 +2H2ONaOH+HCl NaCl
3、 +H2O与酸酐反 应Na2O+CO2 Na2CO32Na2O2+2CO2 2Na2 CO3+O2 2NaOH+CO2 Na2CO3 +H2O NaOH+CO2 NaHCO3与盐溶液 反应Na2O+2NaHSO4 2N aSO4+H2O Na2O+H2O+CuSO4 Cu(OH)2 +Na2SO42Na2O2+4NaHSO4 4 Na2SO4+O2 +2H2O 2Na2O2+H2O+CuSO4 Cu(OH)2 +2Na2SO4+O2 NaOH+NaHSO4 Na2 SO4+H2O 2NaOH+CuSO4 Cu( OH)2 +Na2SO4制法2Na+Na2O2 2Na2O 6Na+2NaNO2 N2+4Na2O2Na+O2 Na2O2Na2O+H2O 2NaOH 2NaCl+2H2O 2NaOH+ Cl2 +H2 用途制氢氧化钠漂白剂、供氧剂、氧化 剂化工原料、制纸浆、 肥皂 3.碳酸钠和碳酸氢钠的性质和制法: 名称和化学式碳酸钠(Na2CO3)碳酸氢钠(NaHCO3) 俗名纯碱、苏打小苏打 颜色和状态白色晶体白色粉末 水中溶解性易溶易溶(比 Na2CO3)小 热稳定性稳定不稳定 2Na
4、HCO3 Na2CO3+CO2 +H2O 与酸反应CO2-3+H+ HCO-3HCO-3+H+ CO2 +H2OHCO-3+H+ H2O+CO2 与某些碱反应Ca(OH)2+Na2CO3 CaCO3 +2 NaOHNaHCO3+Ca(OH)2 CaCO3 +NaOH+H2O 2NaHCO3+Ca(OH)2 CaCO3 +Na2CO3+2H2O 与某些盐反应BaCl2+Na2CO3 BaCO3 +2NaClNaHCO3+NaHSO4 Na2SO4+ H2O+CO2 与 CO2反应Na2CO3+CO2+H2O 2NaHCO3不反应相互转化Na2CO3 NaHCO3 制法NaOH+CO2 NaHCO3 2NaHCO3 2Na2CO3+H2O+OC2 NaOH+CO2 NaHCO3鉴别加酸产生 CO2加热难分解加酸产生 CO2较 Na2CO3 快加热分解出 CO2 用途制玻璃、肥皂、造纸、纺织发酵粉、治胃酸过多三、知识点、能力点提示三、知识点、能力点提示 1.通过钠的化学性质的学习,能正确分析钠长久露置于空气中发生的一系列变 化的现象和原理. 2.通过钠与水反应的现象及实质的学习,能正确分析钠
《高考化学专题复习:碱金属》由会员jiups****uk12分享,可在线阅读,更多相关《高考化学专题复习:碱金属》请在金锄头文库上搜索。

建立安全生产长效机制-共创和谐平安输气管道

土石方爆破工程设计方案

康师傅百货商场制度汇编之退换货管理办法

庙头中学2012年中考百日誓师大会学生代表发言稿

围堰拆除爆破工程

华能洱源马鞍山风电场工程土石方爆破管理制度

国资委:全面开展管理提升活动-为培育世界一流企业奠定坚实基础

《专业技术人员职业发展与规划》电子书

应收票据审计方案
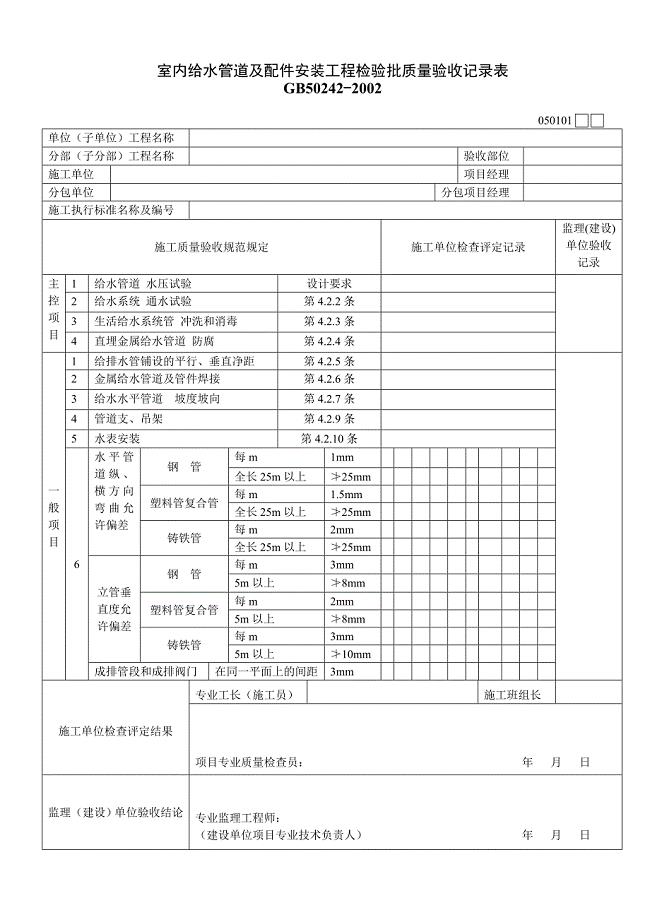
建筑给水排水与采暖工程质量验收用表

广播电视管理条例行政处罚裁量标准

广东电力系统调度运行操作管理规定

建筑给排水工程名词解释

幼儿园小班安全健康活动教案:宝宝误食后的急救

建业集团房屋建筑工程交房标准内容技术交底

建筑心理学论文(1)

康师傅百货商场制度汇编之工服管理程序009

建筑工程专业一级建造师继续教育培训结业报告20

廉洁风险防控回头看工作汇报材料

平台工作人员服务规范
 我为家乡小笼包代言英语作文
我为家乡小笼包代言英语作文
2024-04-17 4页
 熊猫的外貌英语作文三年级
熊猫的外貌英语作文三年级
2024-04-17 3页
 在学校的一天时间都在干嘛英语写作文
在学校的一天时间都在干嘛英语写作文
2024-04-17 4页
 高中英语作文马拉松
高中英语作文马拉松
2024-04-17 3页
 赏桃花日英语作文
赏桃花日英语作文
2024-04-17 3页
 home home为题的英语作文
home home为题的英语作文
2024-04-17 3页
 我的家乡在广东阳春英文作文
我的家乡在广东阳春英文作文
2024-04-17 3页
 想加入足球俱乐部的英文作文
想加入足球俱乐部的英文作文
2024-04-17 4页
 关于压岁钱习俗的作文
关于压岁钱习俗的作文
2024-04-17 3页
 我最喜欢的奥运项目游泳,英语作文
我最喜欢的奥运项目游泳,英语作文
2024-04-17 4页

