
化学选修三 第一章 第二节 原子结构与元素的性质课件
41页1、第二节 原子结构与元素的性质 (原子核外电子排布的周期律),原子结构与元素的性质,已学过的元素周期律知识回顾,核外电子周期性排布,周期,7,族,18,同周期18(K层例外),横减竖增(不包括稀有气体),同周期+1+7(F、O例外);-4 -1,同周期金属性递减、非金属性递增,同周期碱性递减、酸性递增,左右渐易、上下渐难,左右渐强、上下渐弱,元素周期表概念,19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Cs Ba 57-71 At 85 Fr Ra 89-103 107 * *,VIII,Li Be,B C N O F Ne,0,123,4 5 6,周期表与周期律,H,He,IIIA IVA VA VIA VIIA,IA,IIIB IVB VB VIB VIIB,IIA,Al Si P S Cl Ar,IB IIB,Na Mg,催化剂、耐高温、耐腐蚀,元素周期表意义,非金属性逐渐增强,非金属性逐渐增强,金属性逐渐
2、增强,金属性逐渐增强,7,按照电子排布,可把周期表的元素划分为5个区:s区、d区、ds区、p区、f区。划分区的依据是什么? s区、d区、p区分别有几个纵列?,区的名称来自按照构造原理最后填充的能级的符号,思考与探究,最后1个电子填充在ns轨道上,价电子的构型是ns1或ns2,位于周期表的左侧,包括A和A族,它们都是活泼金属,容易失去电子形成+1 或+2价离子。,s区元素,s区和p区的共同特点是:最后1个电子都排布在最外层,最外层电子的总数等于该元素的族序数。s区和p区就是按族划分的周期表中的主族0族。,最后1个电子填充在np轨道上,价层电子构型是ns2np16,位于周期表右侧,包括AA族元素。大部分为非金属。0族稀有气体也属于p区。,p区元素,它们的价层电子构型是(n1)d19ns12,最后1个电子基本都是填充在倒数第二层 (n1)d轨道上的元素,位于长周期的中部。这些元素都是金属,常有可变化合价,称为过渡元素。它包括B族元素。,d区元素,价层电子构型是(n1)d10ns12,即次外层d轨道是充满的,最外层轨道上有12个电子。它们既不同于s区,也不同于d区,故称为ds区,它包括B和B族
3、,处于周期表d区和p区之间。它们都是金属,也属过渡元素。,ds区元素,最后1个电子填充在f轨道上,价电子构型是:(n2)f 014ns2,或(n 2)f 014 (n1)d 02ns2,它包括镧系和锕系元素(各有14种元素)。,f区元素,五个区:s、p、d、ds、f,A 0,s区,d 区,ds区,p区,ns2np1-6,(n-1)d10 ns1-2,(n-1)d1-8ns2 (有例外),B B,A A,A,ns1,ns2,BB ,f 区镧系、锕系 (n-2)f1-14ns2(有例外),镧 锕,A、A族,AA族,B族,B、B族,镧系和锕系,ns1、ns2,ns2np16,(n1)d19ns12,(n1)d10ns12,(n2)f 014ns2,各区元素特点,活泼金属,大多为非金属,过渡元素,过渡元素,小结,思考:为什么s区、d区、ds区的元素都是金属(除H外)?,s区、d区、ds区的元素最外层电子数为1-2个电子,在反应中易失去,所以都是金属。,1. 为什么副族元素又称为过渡元素?,2.为什么在元素周期表中非金属元素主要集中在右上角三角区内(如图)?处于非金属三角区边缘的元素常被称为半金
《化学选修三 第一章 第二节 原子结构与元素的性质课件》由会员我***分享,可在线阅读,更多相关《化学选修三 第一章 第二节 原子结构与元素的性质课件》请在金锄头文库上搜索。

2020届中考英语备考复习-作文课件

2019年中考英语复习-专题十五-交际运用(试卷部分)课件
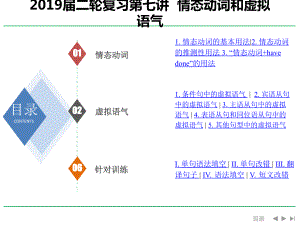
2019届二轮复习-高中英语-情态动词和虚拟语气课件

2019届一轮复习苏教版物质的跨膜运输课件

2019年北师大版英语单元复习课件::Unit17Laughter课件北师大版选修6

2021届新中考物理冲刺备考复习-力-弹力-重力课件

2019届一轮复习人教版种群的特征和数量变化课件

2020年高考地理一轮复习--等高线地形图-课件

2019版高考英语一轮复习-Unit-1-Living-well课件

2019届一轮复习人教版孟德尔的遗传定律——基因分离定律课件

2019届高三第二轮复习专题二万有引力定律及其应用课件

2020最新部编版语文五年级上册23-鸟的天堂课件含课后练习

2020版高考(浙江)一轮复习:第7讲-细胞呼吸课件

2020年新教材高中英语UNIT4HISTORYANDTRADITIONSSectionⅢDiscoveringUsefulStructures课件必修第二册

2019届高考历史二轮复习阶段三专题十三罗斯福新政与当代资本主义的新变化课件2

2019版高考生物二轮复习-专题三-细胞的生命历程-考点9-细胞分裂过程图像和坐标曲线的识别课件

(通史版)2021版高考历史一轮复习第4部分高考讲座(三)2高考非选择题(12分开放探究题)规范答题讲练课件

2019届高三地理复习第五讲--《区际联系与区域协调发展》课件

2021人教部编版历史九年级上册习题课件:第18课美国的独立

2020学年新教材高中英语Unit1FoodforthoughtPeriodTwoStartingout课件
 基层党支部党委2024党建工作总结PPT
基层党支部党委2024党建工作总结PPT
2024-04-18 25页
 基层党建述廉报告PPT模板
基层党建述廉报告PPT模板
2024-04-18 29页
 2024基层党建工作总结PPT模板
2024基层党建工作总结PPT模板
2024-04-18 38页
 强化组织工作培育栋梁之才培训课件PPT
强化组织工作培育栋梁之才培训课件PPT
2024-04-18 16页
 红蓝色简约病区安全管理医疗护理PPT模板
红蓝色简约病区安全管理医疗护理PPT模板
2024-04-09 21页
 黄色卡通重阳节传统节日主题班会通用PPT模板
黄色卡通重阳节传统节日主题班会通用PPT模板
2024-04-09 26页
 红色党政风党风廉政建设
红色党政风党风廉政建设
2024-04-09 28页
 彩色卡通励志主题班会PPT
彩色卡通励志主题班会PPT
2024-04-09 19页
 中秋古诗词鉴赏ppt模板
中秋古诗词鉴赏ppt模板
2024-04-09 26页
 粉色清新风我们结婚了
粉色清新风我们结婚了
2024-04-09 23页

