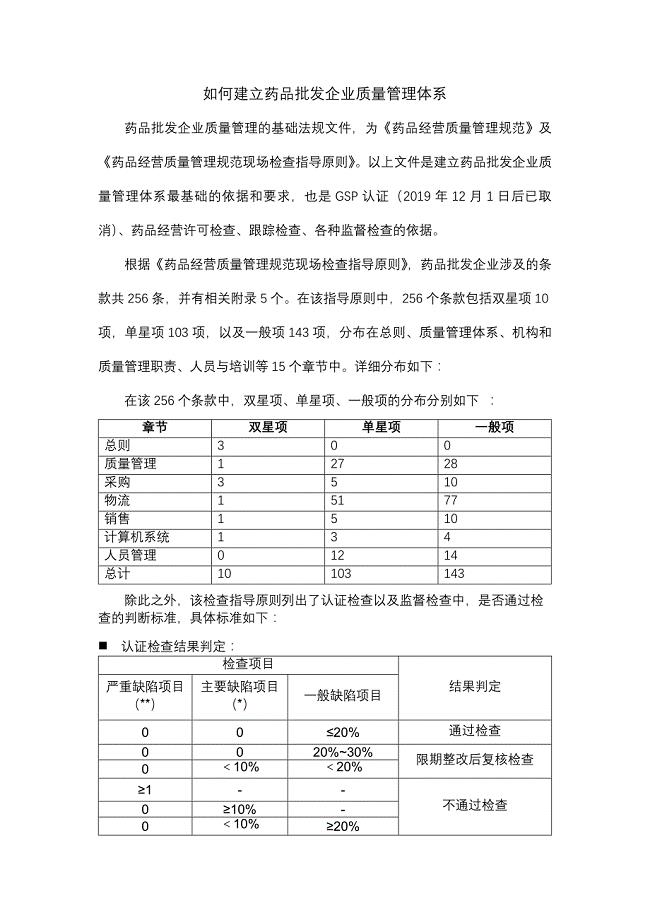
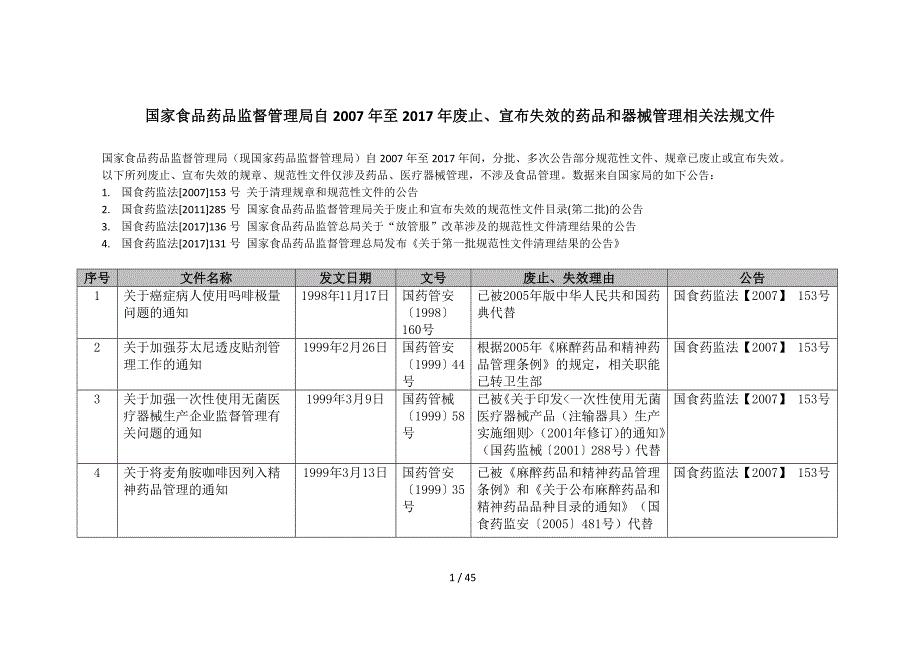
药品经营企业质量文件管理操作规程
5页1、药品经营企业质量文件管理操作规程文件编号:CZ-XXXX文件起草与审批人员签名及日期起草人李一审核人张三审核人张四审核人张五审核人张六批准人李梅执行日期年 月 日文件分发部门 质量部 采购部 销售部 信息管理部 物流部 财务部1、 目的:制订本操作规程的目的是建立质量文件的规程,规范本企业质量文件的管理工作。2、 依据:药品经营质量管理规范及其现场检查指导原则。3、 责任:质量负责人、质量部、各部门负责人负责确保本操作规程的实施。4、 操作规程内容1. 本操作规程所称的质量文件包括质量管理制度、质量管理操作规程、各部门各岗位的质量管理职责及质量管理记录、报告、档案等。2. 质量文件的起草质量部依据药品管理相关法律法规和质量管理工作需要,组织制定质量文件,确定文件题目、编号等。其他部门根据日常工作需要,提出质量文件的编制要求,审核质量文件内容是否符合企业实际情况。质量文件的编号固定如下:文件类型-四位流水号,如:质量管理制度:ZD-0001;操作规程:CZ-0001;部门及岗位职责:ZZ-0001;质量管理记录和档案:JL-00013. 质量文件的审核质量部、质量负责人、文件相关部门负责
2、文件的审核工作。质量文件的审核主要关注如下:(1) 符合药品管理法及其他相关法规。(2) 符合国家药品标准及其他行业标准。(3) 符合公司实际运行情况。(4) 和公司其他质量文件内容之间是否存在冲突。(5) 文件的可操作性。(6) 文件的格式、编号、内容等的规范性。4. 文件的批准。质量部和各相关部门审核确认无误的质量文件,由质管员打印并交由起草人、各审核人签名。最后,由质量负责人批准定稿。质量负责人并同时确定文件的执行时间。5. 文件的培训经质量负责人批准后,起草人应确保在规定的执行时限前,组织文件的培训,保证有关执行或操作人员明确文件的各项要求。6. 文件执行文件自执行之日起开始执行,旧版文件自动作废。7. 文件的分发(1) 文件原稿由质量部存档。质管员负责按照文件分发列表的要求复印文件原告,并将文件复印件分发至相应部门。负责将旧版文件收回。各部门文件签收人员在文件分发记录签收。8. 文件的复审(1) 质量部负责组织文件的定期复审,最少每2年复审1次。(2) 文件复审工作由质量部和文件相关部门共同完成,由质量部负责整合所有部门的复审意见,形成复审结果并提交质量负责人审批。(3) 综
《药品经营企业质量文件管理操作规程》由会员药***分享,可在线阅读,更多相关《药品经营企业质量文件管理操作规程》请在金锄头文库上搜索。
 护士执业资格考试试题第三章第十二节 细菌性肝脓肿病人的护理
护士执业资格考试试题第三章第十二节 细菌性肝脓肿病人的护理
2023-09-11 1页
 低体重新生儿麻醉指南
低体重新生儿麻醉指南
2023-05-28 11页
 员工医疗期满通知
员工医疗期满通知
2022-10-03 2页
 中药熏洗技术操作规范
中药熏洗技术操作规范
2024-01-06 3页
 糖尿病治疗用药
糖尿病治疗用药
2023-07-03 14页
 古诗鉴赏之形象与情感习题
古诗鉴赏之形象与情感习题
2023-10-18 10页
 西班牙移民和西班牙留学的区别
西班牙移民和西班牙留学的区别
2023-06-24 1页
 选购抽屉锁本卷须知 怎么安装抽屉锁
选购抽屉锁本卷须知 怎么安装抽屉锁
2024-01-10 3页
 物联网与智慧医疗峰会
物联网与智慧医疗峰会
2022-11-02 2页
 塞药法技术操作规范
塞药法技术操作规范
2024-02-13 3页